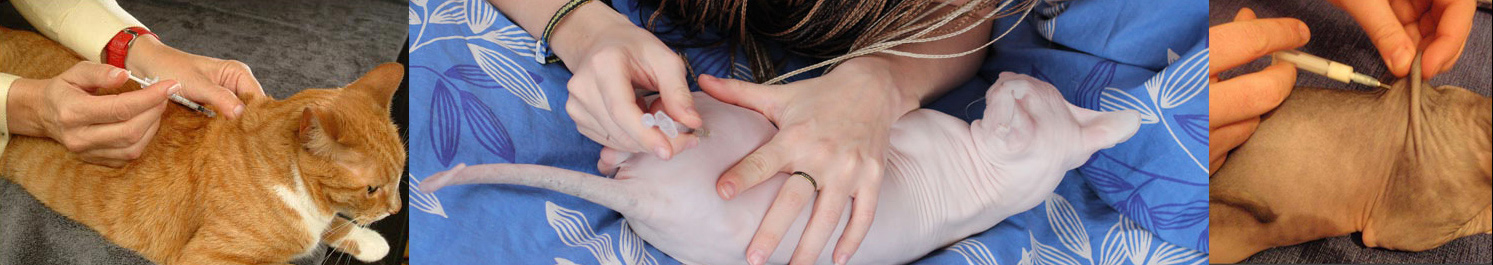
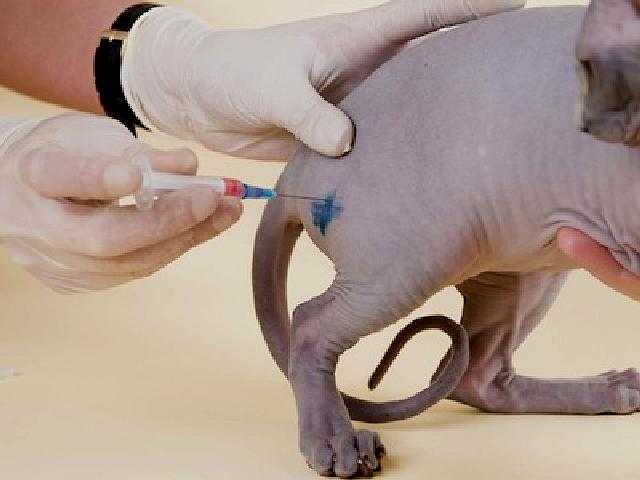
Как сделать укол кошке внутримышечно в бедро правильно: инструкция и советы
Статья проверена главным ветеринарным врачом Кончевой Елизаветой Сергеевной
Содержание
- В каких случаях уколы кошке ставят внутримышечно?
- Особенности внутримышечных инъекций
- Отличия подкожных и внутривенных уколов
- Куда делают укол кошке внутримышечно?
- Подготовка к инъекции
- Как выбрать шприц и иглу
- Подготовка лекарства
- Как зафиксировать питомца?
- Как поставить укол коту внутримышечно – пошаговая инструкция
- Внутримышечный укол котенку
- Возможные осложнения
- Ответы на часто задаваемые ветеринарам вопросы
В каких случаях уколы кошке ставят внутримышечно?
Такие ситуации, как отравление, болевой синдром, травма, укусы насекомого или змеи, острая аллергическая реакция требуют незамедлительной помощи. Также внутримышечная инъекция бывает необходима кошке в случаях, когда она получает длительное лечение, или у животного есть хроническое заболевание, требующее регулярного введения лекарственных препаратов.
Особенности внутримышечных инъекций
При проведении внутримышечной инъекции лекарственный препарат доставляется напрямую в глубину мышечной ткани.
У любой медицинской процедуры есть определенные недостатки и преимущества.
К очевидным плюсам можно отнести следующие:
-
Внутримышечную инъекцию можно сделать самостоятельно любому человеку, не обладающему специальными медицинскими или ветеринарными навыками.
-
Медленное, постепенное поступление лекарственного препарата создает возможность дозировано доставлять лекарство в кровеносное русло и поддерживать стабильную концентрацию лекарственных веществ в организме животного.
К недостаткам можно отнести болезненность при введении в мышцу большого количества препаратов, которые обладают раздражающим действием. Ткани мышц достаточно хорошо иннервируются из-за развитой системы кровообращения, поэтому укол может быть достаточно болезненным для питомца.
Отличия подкожных и внутривенных уколов
Самыми распространенными способами введения лекарственных препаратов в ветеринарной практике являются подкожные, внутримышечные и внутривенные техники.
Подкожные инъекции отличаются от внутримышечных глубиной проникновения иглы в ткани и возможным допустимым объемом вводимых препаратов и растворов. Область холки у кошки, в отличие от других мест на теле питомца, обладает наименее выраженной болезненностью, так как в ней сосредоточено не так много нервных окончаний. И, в отличие от тканей мышц бедра, введение препаратов в эту область не вызывает выраженной болезненности у питомца. Подкожно можно ввести намного больший объем жидкости, чем внутримышечно, так как подкожная клетчатка у животных достаточно эластична и позволяет вместить относительно большие количества лекарственных препаратов и растворов.
Внутривенные инъекции должны выполняться только ветеринарными специалистами, так как такая процедура требует профессиональных навыков и строгого соблюдения правил и техники выполнения процедуры.
Куда делают укол кошке внутримышечно?
Далее рассмотрим подробнее, как и куда колоть укол кошке внутримышечно.
Вводить препараты можно в строго определенные части тела животного.
Для внутримышечных инъекций подходят крупные бедра и мышцы плеча. Для самостоятельных внутримышечных уколов использовать область плеча не рекомендуется, так как там сосредоточено очень много нервных окончаний, и мышцы недостаточно крупные. Вводить препараты самостоятельно рекомендуется только в область холки — для подкожных инъекций, в мышцы бедра — для внутримышечных.
Подготовка к инъекции
Для того, чтобы процедура прошла максимально комфортно и быстро для вас и пушистого пациента, важно заранее подготовиться.
-
Перед процедурой тщательно вымойте руки с мылом и продезинфицируйте их спиртом.
-
Успокойте кошку, погладьте ее, угостите лакомством и приготовьте место, где планируете сделать укол. Поверхность, на которой будет располагаться кошка во время процедуры, должна быть не скользкой, ровной, а главное — удобной для вас (можно использовать стол, тумбу или диван).
-
Подготовьте все необходимое для инъекции: спирт (или другое дезинфицирующее средство), шприц с предварительно набранным лекарством, вату или ватные диски, средства для фиксации, мягкий плед. Используйте стерильные одноразовые шприцы.
-
Успокоив и подготовив животное, нужно осмотреть кожу в области постановки укола, там не должно быть раздражений, покраснений и воспаленных участков.
-
Если длинная шерсть затрудняет проведение процедуры, ее можно постричь в области введения лекарства.
Как выбрать шприц и иглу
Выбор шприца для инъекции зависит от следующих факторов: какая инъекция планируется — подкожная или внутримышечная, какой объем препарата необходимо ввести, какой возраст и размер питомца, какой вязкостью (тягучестью) обладает препарат, какова степень болезненности при его введении.
При выборе шприца, исходите из условия, что укол нужно сделать как можно быстрее. Для этого стоит обратить внимание на консистенцию препарата – если жидкость густая, вязкая, тягучая, маслянистая или имеет свойства суспензии, игла должна быть толще. Такой раствор может забить тонкую иглу, и инъекция будет длиться дольше, что впоследствии только увеличит стресс животного. И наоборот, стоит выбрать иглу тоньше для негустых препаратов — так неприятные ощущения от инъекции будут сведены к минимуму.
Для этого стоит обратить внимание на консистенцию препарата – если жидкость густая, вязкая, тягучая, маслянистая или имеет свойства суспензии, игла должна быть толще. Такой раствор может забить тонкую иглу, и инъекция будет длиться дольше, что впоследствии только увеличит стресс животного. И наоборот, стоит выбрать иглу тоньше для негустых препаратов — так неприятные ощущения от инъекции будут сведены к минимуму.
Самостоятельно внутримышечные уколы кошкам наиболее безопасно выполнять инсулиновыми шприцами или шприцами объемом 2 мл.
Если препарат неболезненный, на водной основе, желательно использовать шприц с максимально тонкой иглой. Так, инъекция будет наименее болезненной и минимально травмирует мышечную ткань. Для дозировок 1 мл или менее можно использовать инсулиновый шприц с короткой и тонкой иглой. Инсулиновые шприцы наиболее безопасно применять для уколов маленьким котятам.
Подготовка лекарства
Перед тем, как приступить к набору лекарства, важно внимательно прочитать инструкцию к препарату и назначения врача.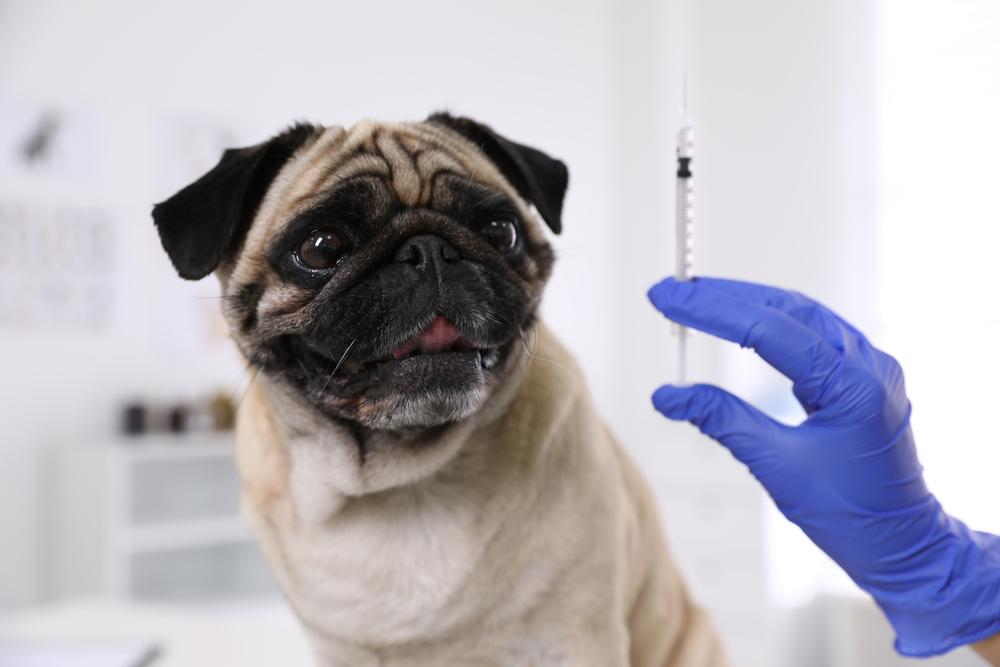
Удостоверьтесь, что способ введения препарата соответствует описанию производителя. Лекарства могут использоваться для подкожных, внутримышечных, внутривенных инъекций, и важно точно знать, что препарат можно вводить тем или иным способом. Некоторые препараты при неправильном способе введения могут вызвать некроз тканей и абсцесс на месте введения.
Если в инструкции к препарату указан только внутривенный способ введения, то такие лекарства нельзя вводить ни подкожно, ни внутримышечно, даже в самых минимальных дозировках.
Соблюдайте дозировку и разметку делений на шприце. Проверьте срок годности препарата. Согрейте набранный в шприц препарат в руке, если он хранился в холодильнике.
Если препарат выпускается в консистенции порошка, его предварительно разводят в растворителе, который прилагается к препарату, физиологическом растворе или новокаине. Уточните возможные способы растворения у врача, либо следуйте инструкции к препарату.
Уточните возможные способы растворения у врача, либо следуйте инструкции к препарату.
Если препарат находится во флаконе с резиновой крышкой, для удобства набора препарата можно вставить дополнительную иглу для выхода воздуха из флакона. Этот прием поможет облегчить набор лекарства.
После того как лекарство набрано, нужно освободить шприц от пузырьков воздуха. Поверните шприц вертикально, аккуратно постучите по содержимому шприца, поднимая пузырьки воздуха наверх, выпустите в воздух несколько капель препарата.
Набирайте лекарство в шприц непосредственно перед уколом. Снимайте защитный колпачок иглы перед инъекцией, не раньше. Не держите иглу без защитного колпачка на воздухе, так как игла может загрязниться микрофлорой, что чревато воспалениями в месте инъекции.
Отзывы питомцев
@lil.tom
Мейнкун, г. Москва
Я новый член семьи и мой новый друг Шарик не хотел со мной дружить. 😿 Благо хозяйка быстро заметила проблему и купила нам страховку.
@barney_goodboy Доберман, г. Саратов Я случайно съел носок своей хозяйки и у меня разболелся животик. 💩🤢😭 День был испорчен. Хорошо, что моя страховка покрывает консультацию и лечение в клинике. Настроение и семейный бюджет не пострадали!
@mini_ralf Лабрадор, г. Тула Я еще совсем щенок, и большие собаки постоянно задирают меня во дворе. Домой я возвращаюсь побитый и покусанный 🤕. Но я не унываю, потому что в любой непонятной ситуации мне помогает мой онлайн-ветеринар 💫🩺
Подробнее
Позаботьтесь о здоровье питомца
Как зафиксировать питомца?
Для безопасной и быстрой процедуры постановки укола важно надежно, но при этом мягко и аккуратно, зафиксировать животное. Чтобы правильно зафиксировать кошку для укола, нужно держать ее очень аккуратно. Помните, что нельзя грубо и сильно удерживать питомца — это может привести к физической травме и сильному стрессу. Нельзя удерживать кошку за холку, так как это не приводит к надежной фиксации животного, но может привести к тяжелым травмам — повреждению шейных мышц и трахеи, смещению позвонков.
Чтобы правильно зафиксировать кошку для укола, нужно держать ее очень аккуратно. Помните, что нельзя грубо и сильно удерживать питомца — это может привести к физической травме и сильному стрессу. Нельзя удерживать кошку за холку, так как это не приводит к надежной фиксации животного, но может привести к тяжелым травмам — повреждению шейных мышц и трахеи, смещению позвонков.
Специальные сумки-фиксаторы можно использовать лишь в случае, если помещение кошки в сумку не вызывает у нее негативной реакции.
Для фиксации кошек рекомендуется использовать метод мягкого пеленания или накрывания мягким полотенцем в позе сфинкса. Такой деликатный и не пугающий кошку подход снижает риск получения травмы и делает возможным сделать серию уколов, в случае длительного курса лечения.
Старайтесь не причинять кошке дополнительного стресса во время процедуры. Если она боится, не применяйте силу удерживая ее. Кошка испугается еще больше и будет с большим усилием вырываться. Отпустите питомца, дайте ему успокоиться и понять, что ничего страшного не происходит, повторите процедуру. Если кошка спокойно реагирует на манипуляции, то не применяйте силу, действуйте уверенно, но мягко. Во время фиксации следите за тем, чтобы не причинить ей боль.
Если кошка спокойно реагирует на манипуляции, то не применяйте силу, действуйте уверенно, но мягко. Во время фиксации следите за тем, чтобы не причинить ей боль.
При проведении процедуры очень важно разговаривать с питомцем спокойным голосом, успокаивать его, а после окончания процедуры угостить вкусным лакомством.
Правильная и уверенная фиксация пушистого пациента помогает снизить риски травматизации и для кошки, и для человека, выполняющего процедуру.
Теперь, когда все готово, можно приступать непосредственно к уколу.
Как поставить укол коту внутримышечно – пошаговая инструкция
Для того, чтобы правильно поставить укол кошке в бедро внутримышечно, иглу колют в мышцу между коленным и тазобедренным суставами. На ощупь это самое мягкое место в треугольнике, который образуют суставы (отмечено зеленым на фото ниже).
Итак, как сделать внутримышечный укол коту – пошагово:
-
Погладьте и зафиксируйте питомца самостоятельно или при помощи помощника.
 Если укол выполняется с помощником, то можно положить кошку на бок, чтобы ассистент смог зафиксировать и придерживать лапы.
Если укол выполняется с помощником, то можно положить кошку на бок, чтобы ассистент смог зафиксировать и придерживать лапы. -
Найдите самое мягкое место в области задней поверхности бедра и расслабьте конечность слегка помассировав мышцу, зафиксируйте ее.
-
Определите, нащупывая пальцами, где расположена кость для того, чтобы не задеть ее иглой. Не сжимайте мышцу кошки во время инъекции.
-
Для того, чтобы избежать попадания иглы в седалищный нерв или сустав, необходимо двумя пальцами — большим и указательным, зафиксировать мышцы бедра с двух сторон и ввести иглу в мышцу в область между пальцами.
-
Аккуратно и быстро введите иглу в середину бедра кошки примерно под углом в 45 градусов на глубину около 1 см.
-
Не вводите лекарство резко и слишком быстро, чтобы не травмировать мышечную ткань, кожу и не причинить животному дополнительных болевых ощущений.
 Объем препарата в 1 мл вводим не менее трех секунд.
Объем препарата в 1 мл вводим не менее трех секунд. -
Аккуратно, плавно вынимайте иглу под таким же наклоном, под каким она была введена.
-
Не вводите большие объемы препаратов кошке одновременно. Если это необходимо, то нужно сделать несколько инъекций в разные места.
-
Если выступит капля крови, аккуратно прижмите место укола ватным тампоном с антисептиком и подержите несколько минут.
-
Похвалите и успокойте любимца, угостите лакомством по окончании процедуры.
Внутримышечный укол котенку
Желательно, чтобы медицинские манипуляции и процедуры малышам проводили ветеринарные специалисты, так как риски нанести травму маленькому пациенту самостоятельно очень высоки. Если ситуация требует срочной помощи, придется сделать укол самостоятельно.
Для того, чтобы сделать укол котенку внутримышечно, нужно учитывать особенности анатомического строения маленьких животных. Мышцы и подкожная клетчатка котят еще недостаточно развиты, сосуды и нервы не защищены объемом мышечной ткани и находятся достаточно близко к поверхности тела.
Мышцы и подкожная клетчатка котят еще недостаточно развиты, сосуды и нервы не защищены объемом мышечной ткани и находятся достаточно близко к поверхности тела.
Поэтому важно использовать тонкие иглы, контролировать глубину ее введения и не допускать попадания иглы в область кости. Для малышей наиболее безопасны инсулиновые шприцы и шприцы объемом 1 мл. Если лекарство негустое, тонкая игла позволит беспрепятственно ввести препарат. Также, если необходимо ввести густой препарат, можно использовать шприцы на 2 мл с иглой минимального диаметра.
Важно учитывать хрупкость маленького пациента и аккуратно фиксировать котенка, не сжимая сильно при удерживании и не пугая его. После процедуры успокойте малыша и угостите его чем-то вкусным. Так, укол не покажется маленькому пациенту страшным.
Возможные осложнения
Как правило, инъекции не вызывают негативных последствий. Но иногда они могут возникнуть не только у неопытного владельца, но и у специалиста. Знать о возможных осложнениях важно для того, чтобы вовремя оказать питомцу необходимую помощь.
Если сделать укол кошке неправильно, например, ввести препарат не в то место, повредить сосуд или попасть в нерв, проблемы могут быть следующими:
-
Если на месте укола после извлечения иглы выступили капли крови, то это свидетельствует о повреждении стенки кровеносного сосуда. Если выделилось несколько капель крови, то для остановки кровотечения достаточно приложить холод на 10—15 минут к месту инъекции (лед или замороженный продукт из морозильной камеры, обернутые в чистую ткань или влажное холодное полотенце).
-
Инфильтрат или уплотнение (шишка, припухлость) в месте инъекции указывает на то, что введенное лекарство не всасывается в кровоток, либо в травмированной ткани или в окружающих тканях начался воспалительный процесс. Причинами возникновения инфильтрата могут быть: введение сразу слишком большого объема препарата, попадание инфекции вместе с ним, очень быстрое введение лекарства, аллергическая реакция тканей, применение препаратов без предварительного согревания до температуры тела.

-
Длительно не рассасывающиеся инфильтраты и уплотнения могут привести к возникновению абсцессов. В полости инфильтрата или на месте уплотнения формируется гнойное воспаление, место инъекции может опухнуть, стать горячим и болезненным. Кошка может отказываться от еды, станет вялой, апатичной, повысится температура тела. Такое состояние опасно и в тяжелых случаях может привести к сепсису и гибели животного. Важно как можно скорее обратиться за хирургической помощью.
-
Хромота после инъекции. Причин возникновения хромоты может быть несколько. Одна из них — повреждение мышц вследствие использования раздражающих ткани растворов, антибиотиков и густых, трудно рассасывающихся препаратов, приводящих к сильной болезненности на месте инъекции.
 Хромота может возникнуть вследствие неудачной постановки укола, либо в результате попадания иглы в нерв. Как правило, хромота проходит в течение часа после укола. Если хромота усиливается, не проходит в течение нескольких дней, конечность потеряла подвижность и не разгибается, а кошка не опирается на нее при ходьбе, необходимо показать питомца врачу.
Хромота может возникнуть вследствие неудачной постановки укола, либо в результате попадания иглы в нерв. Как правило, хромота проходит в течение часа после укола. Если хромота усиливается, не проходит в течение нескольких дней, конечность потеряла подвижность и не разгибается, а кошка не опирается на нее при ходьбе, необходимо показать питомца врачу. -
Повышение температуры. Такая реакция организма может быть вызвана аллергией на введенный препарат, либо служить симптомом воспалительного процесса в месте инъекции. Это может произойти, если при проведении процедуры не была соблюдена стерильность.
-
Тяжелая реакция на стресс. Кошки являются очень чувствительными животными. Они тяжело переносят длительный хронический стресс, боль и дискомфорт. Если питомец слишком тяжело переносит уколы, прячется после процедур, становится пугливым и нервным, отказывается от еды, не позволяет прикоснуться к себе, забивается в укромные места и подолгу из них не выходит, то, по согласованию с лечащим врачом, желательно как можно скорее перейти на другие формы дачи препаратов.
 Например, на таблетки или суспензии. Для снижения уровня стресса можно воспользоваться специальными успокаивающими синтетическими лицевыми кошачьими феромонами в форме диффузора.
Например, на таблетки или суспензии. Для снижения уровня стресса можно воспользоваться специальными успокаивающими синтетическими лицевыми кошачьими феромонами в форме диффузора.
Обращайте пристальное внимание на самочувствие и изменение в поведении питомца. При отказе от еды, апатии, температуре, болезненности в месте укола или появлении кровянистых или гнойных выделений в месте инъекции незамедлительно покажите питомца ветеринарному специалисту.
В следующем видео рассмотрено, как правильно сделать инъекцию кошке внутримышечно.
Ответы на часто задаваемые ветеринарам вопросы
Статья не является призывом к действию!
Для более детальной проработки проблемы рекомендуем обратиться к специалисту.
Спросить ветеринара
Статья была полезна?
Спасибо, давайте дружить!
Подписывайтесь на наш Инстаграмм
Спасибо за обратную связь!
Давайте дружить — скачайте приложение Petstory
как сделать внутримышечно в холку / БиоВет
БиоВет » 📚ЭНЦИКЛОПЕДИЯ » 🐱Кошки » Болезни🐱
Содержание:
Наши питомцы тоже болеют, а инъекции – нередко единственный способ доставить в организм необходимое лекарство.Если нужен один укол, можно свозить кошку в клинику, но когда требуется целый курс лечения, можно научиться делать уколы самостоятельно. Разумеется, если речь не идет о внутривенных инъекциях, которые должен делать только специалист.
Подходящие для уколов места
Теоретически уколы можно ставить во многие места на теле, но наиболее подходящими считаются холка (между лопаток) и мышца бедра. Внутримышечные инъекции имеют ограничение по объему вводимой жидкости, их можно выбирать для безболезненных препаратов.
Кошкам, которые весят до 4 кг, внутримышечно можно вводить не более 1,5 мл раствора.
Сначала следует найти мышцу на задней лапе около коленного сгиба. Нужно соблюдать осторожность, чтобы случайно не попасть в сустав. Игла вводится на глубину 1–1,5 см под углом 45°.
Подкожно в холку стоит делать более болезненные лекарства и вводить растворы больших объемов, но не более 90 мл на 1 кг массы тела.Следует собрать кожу между лопатками в складку и подтянуть ее вверх. Игла вводится в основание холки на глубину 1–2 см под углом 45°.
Прежде чем делать укол кошке нужно как можно надежнее ее зафиксировать, чтобы животное не дергалось. Желательно попросить кого-то помочь придерживать питомца.
Несколько важных правил
- Делать уколы кошке можно только по назначению врача, точно соблюдая режим дозирования.
- Перед введением препарата следует мыть руки. Но даже чистыми руками нельзя касаться стерильной иглы.
- Дезинфицировать место укола нет необходимости.
- Укол можно делать только стерильным шприцем, каждый раз используя новый.
- Нельзя делать инъекции, если на коже в месте введения имеется раздражение или воспаление.
- Если лекарство хранится в холодильнике, перед введением его следует согреть в руках до комнатной температуры.
- Нельзя смешивать в одном шприце несколько препаратов, если это не предписано врачом.

- Набирать лекарство в шприц следует непосредственно перед введением. До момента укола игла должна быть закрыта защитным колпачком.
- Из шприца перед введением препарата обязательно нужно выпускать воздух.
Возможные проблемы после укола
В месте инъекции может появиться кровь. Если это пара капель, ничего страшного нет. Если кровопотеря более значительна, рекомендуется приложить обернутый тканью лед.
После укола в мышцу бедра иногда кошка в течение 2–3 дней может прихрамывать. Рекомендуется периодически массировать конечность, чтобы облегчить самочувствие питомца. Если животное вовсе не может стать на лапку или волочит ее за собой, возможно, задет седалищный нерв. В этом случае стоит обратиться к ветеринару.
Если вы боитесь самостоятельно делать своему питомцу уколы, стоит доверить это специалисту.В клинике «БиоВет» работают квалифицированные ветеринары, готовые принять животное в любое время суток или приехать к вам домой. Наши филиалы находятся во всех районах Москвы, в Реутове и Люберцах. Доверяйте здоровье своего любимца профессионалам!
Все наши Ветклиники:
| 🏥 Клиника | 🗺️ Адрес | 🕔 |
|---|---|---|
| 🏥 Алтуфьево | Алтуфьевское шоссе д 56 | 24/7 |
| 🏥 Бабушкинская | Менжинского 29 | 24/7 |
| 🏥 Беляево | Миклухо Маклая, д 18 к1 | 24/7 |
| 🏥 Бутово Северное | Куликовская, 3Д | 24/7 |
| 🏥 Домодедовская | Ясеневая 28 | 24/7 |
| 🏥 Калужская | Воронцовские пруды д. 3 | 24/7 |
| 🏥 Каховская | Болотниковская, 21с8 | 24/7 |
| 🏥 Марьино | Перервинский Бульвар д. 21/1 | 24/7 |
| 🏥 Медведково | Малыгина 9 стр. 2 2 | 24/7 |
| 🏥 Митино | Генерала Белобородова, 30 | 24/7 |
| 🏥 Новогиреево | Новогиреевская д 53 | 24/7 |
| 🏥 Первомайская | Нижняя Первомайская улица, 12А | 24/7 |
| 🏥 Печатники | Гурьянова д. 4 к.1 | 24/7 |
| 🏥 Преображенская площадь | Халтуринская 18 | 24/7 |
| 🏥 Реутов | Реутов, Калинина, 12 | 24/7 |
| 🏥 Саперный | Саперный проезд д6 к1 | 24/7 |
| 🏥 Селигерская | Дмитровское ш., 107Ак3 | 24/7 |
| 🏥 Солнцево | Главмосстроя дом 12 | 24/7 |
| 🏥 Спортивная | Доватора, д.3 | 24/7 |
| 🏥 Тёплый стан | Теплый Стан 5, к4 | 24/7 |
| 🏥 Тульская | Мытная, 23 | 24/7 |
| 🏥 Хорошево-Мневники | Народного Ополчения 29к1 | 24/7 |
| 🏥 Щелковская | Алтайская 17А | 24/7 |
ЗАПИСЬ В КЛИНИКУ
ВЫЗОВ НА ДОМ
Костенюк Ольга Николаевна
Специальность: Анестезиолог-Реаниматолог / Главный врач / Дерматолог / Диетолог / Рентгенолог / Стоматолог / УЗИ / Хирург
Как сделать укол кошке в домашних условиях?🐱 Делаем укол кошке внутримышечно, в холку или бедро
4. 8/5 — (22 голоса)
8/5 — (22 голоса)
Кошки тоже болеют, и нередко для оказания помощи и облегчения их состояния приходится проводить инъекции. Если ветеринаром был назначен 1 укол, то можно отвезти животное в клинику, но когда для лечения нужен целый курс из уколов, то лучше научиться их делать самостоятельно.
Оглавление
- Виды уколов для кошек
- Разновидности шприцев для инъекций котам
- Как правильно сделать укол кошке?
Виды уколов для кошек
Домашним животным для лечения/профилактики развития болезней или поддержания состояния назначают лечение в виде уколов. Инъекции для котов делятся на несколько разновидностей, с особенностями каждой стоит ознакомиться более детально.
| Разновидность инъекции | Описание |
|---|---|
| Внутривенные | Особенность проведения заключается в том, что лекарственный препарат вводится непосредственно в вену. Провести процедуру непросто, человек должен иметь определенные знания и навыки. В противном случае есть вероятность, что вена будет проткнута насквозь и лекарство не будет введено должным образом. Провести процедуру непросто, человек должен иметь определенные знания и навыки. В противном случае есть вероятность, что вена будет проткнута насквозь и лекарство не будет введено должным образом. |
| Внутримышечные | Лекарство вводится в ткани мышцы. Преимущественно такие уколы котам делают во внешнюю часть бедра. Укол кошке в бедро доставляет болезненные ощущения, поэтому животное нужно надежно и крепко зафиксировать. |
| Подкожные | Лекарственный препарат вводится иглой под кожу. Эта процедура довольно проста в реализации, и при соблюдении четких указаний справиться с ней по силам даже неопытному человеку. Важно! При течении тяжелых дерматологических недугов у животного уколы можно ставить в любом месте на теле, где отсутствуют раны. |
Разновидности шприцев для инъекций котам
Укол кошке подкожно, внутривенно и внутримышечно проводится с использованием обыкновенного человеческого шприца. Приобрести их можно в любой аптеке. Важно, чтобы игла в шприце имела маленький диаметр, иначе болезненные ощущения будут более выраженными, а также игла не должна быть тугой.
Важно, чтобы игла в шприце имела маленький диаметр, иначе болезненные ощущения будут более выраженными, а также игла не должна быть тугой.
Обратите внимание! Некоторые лекарства набираются через резиновую крышку, как следствие – игла шприца тупится. Поэтому рекомендуется либо приобретать шприц с очень острой иглой, либо же менять ее на другую.
Если лекарство имеет не масляную основу, и объем не превышает 1 мл, то предпочтительнее использовать инсулиновый шприц. Если объем препарата превышает 1 мл, то стоит отдать предпочтение 2-5 кубовым шприцам.
Как правильно сделать укол кошке?
Многие владельцы домашних питомцев, столкнувшись с подобной проблемой, задаются вопросом – как поставить кошке укол. Если строго придерживаться нижеописанных рекомендаций, то вероятность развития осложнений существенно сократиться.
Итак, основные рекомендации, как сделать укол кошке в домашних условиях:
- Нельзя своему питомцу назначать лекарственные препараты самостоятельно.
 Делать инъекции можно только по назначению ветеринара, со строгим соблюдением всех предписаний.
Делать инъекции можно только по назначению ветеринара, со строгим соблюдением всех предписаний. - В процессе подготовки и непосредственно во время введения препарата нельзя на питомца кричать, напротив нужно проявить терпимость и быть ласковым.
- Прежде чем ставить укол, человеку необходимо тщательно вымыть руки с использованием антибактериального мыла.
- Движения руки должны быть правильными и точными. Жалость и сомнения делают процедуру более продолжительной, что еще хуже сказывается на эмоциональном состоянии животного.
- Если домашний питомец с характером, то проводить процедуру рекомендуется в паре – один человек делает, второй крепко держит животное.
- Места укола предварительно можно не обрабатывать антисептиком, но шприцы и иглы всегда должны быть одноразовыми.
- Прежде чем вводить препарат в организм, из шприца нужно вытравить весь воздух.
Видео
Обратите внимание! Перед использованием лекарства нужно обязательно убедиться, что не истек его срок годности, а также герметичность емкости для хранения не была нарушена.
Подготовка кошки к предстоящей инъекции
Инструкция по подготовке кошки к уколу выглядит следующим образом:
- Владелец животного предварительно должен подготовить антисептик, чистую вату, шприц и ампулу с лекарством.
- Перед использованием лекарства рекомендуется внимательно изучить инструкцию по эксплуатации. Если возникли вопросы, лучше позвонить ветеринару и проконсультироваться.
- Тщательно вымыть руки с мылом. Вскрыть флакон с лекарством при помощи специальной пилочки. Все содержимое флакона должно находиться в нижней части ампулы. Если же оно расположено в горлышке, то достаточно просто постучать пальцами по его стенкам. В завершении иглу вставляют в емкость через подпиленное горлышко и набирают жидкость в шприц.
- Далее, шприц необходимо повернуть иглой вверх и, медленным нажатием на поршень, убрать со шприца весь воздух.
- Теперь следует взять кошку и погладить ее, чтобы она успокоилась.
Выполнив все подготовительные действия, не нужно медлить, рекомендуется сразу же приступить к введению лекарства.
Куда кошке можно делать уколы?
Прежде чем выяснить, как ставить укол кошке, необходимо выяснить куда предпочтительнее его ставить и, напротив, не рекомендуется. Теоретически ввести лекарство можно через любое место, но есть участки на теле менее чувствительные. Котам рекомендуется вводить инъекции подкожно между лопаток, в области называемой «холкой».
Также можно сделать кошке укол внутримышечно в бедро. Дело в том, что в мышечной части этого участка тела сосредоточена высокая концентрация сосудов, благодаря чему лекарство быстро распространяется по телу и начинает действовать. Рекомендуется ставить укол в это место, если препарат не болезненный.
Важно! Делать укол внутримышечно можно в том случае, если объем препарата не большой. Дело в том, что жидкость, введенная в мышечные ткани, приводит к их расслоению.
Как правильно сделать укол кошке в холку?
Холка имеет слабую чувствительность, ведь не зря мама кошка переносит своих детенышей, ухватившись за их загривок зубами. Кожный покров там толстый и грубый, нарушить его целостность довольно непросто.
Кожный покров там толстый и грубый, нарушить его целостность довольно непросто.
Инструкция, как делать укол кошке подкожно в холку:
- Процедура не из приятных, поэтому кот будет пытаться вырваться. Чтобы это предотвратить, нужно его надежно зафиксировать в одном положении, далее сформировать на холке небольшую складку.
- У основания складки следует сделать прокол. Если применяется инсулиновый шприц, то игла под кожу должна зайти на всю длину. Поначалу будет ощущаться сопротивление, но по достижении нужной глубины сопротивление исчезнет.
- Медленно и без резких движений начать вводить препарат коту под кожу. Параллельно не будет лишним успокаивать своего любимца.
Важно! Если в процессе введения препарата шерсть стала мокрой, значит, игла насквозь проткнула складку. Процедуру нужно повторить с самого начала.
Как сделать кошке укол внутримышечно?
Инструкция, как сделать укол кошке внутримышечно в бедро:
- Домашнего питомца следует надежно зафиксировать на ровной поверхности.
 Удерживать рекомендуется за голову и конечности.
Удерживать рекомендуется за голову и конечности. - Наметить наиболее подходящее место для прокола в области бедра. Укол должен ставиться приблизительно под углом в 45 градусов относительно кожи.
- Чтобы животное не чувствовало боли и процедура прошла быстрее, оно должно расслабить лапку. Если же она напряжена, нужно ее помассировать спокойными движениями.
- Осторожно и медленно ввести иглу, начать вводить препарат.
После введения лекарства шприц осторожно извлекают из тела кота. Животное отпускают.
Как сделать укол кошке внутримышечно?Возможные последствия после укола
Животное может несколько дней прихрамывать, если питомцу уколы делают в бедро. Для облегчения состояния питомца не будет лишним осторожными и плавными движениями массировать эту область.
Важно! Если введения лекарственного препарата в мышцу бедра питомец не может встать на заднюю лапку, то вполне вероятно, что был поврежден седалищный нерв. Потребуется обязательный осмотр ветеринаром.
Из статьи удалось узнать, как правильно сделать укол кошке в бедро, холку или внутривенно. Важно помнить, что если показаны внутривенные уколы, то без помощи квалифицированного специалиста не обойтись. Если же удалось ограничиться подкожными или внутримышечными, то следует строго придерживаться вышеописанных инструкций.
Как сделать укол коту: внутримышечно, подкожно
Содержание
- 1 Зачем уметь правильно делать питомцу уколы?
- 2 Виды инъекций
- 2.1 Внутримышечно
- 2.2 Введение инъекции подкожно
- 3 Правила и техника постановки инъекций
- 3.1 Выбор инструмента инъекции
- 3.2 Куда колоть?
- 3.3 Как вводить лекарство?
- 3.4 Осложнения от процедуры
Хозяева котиков часто предпочитают научиться делать своему любимцу инъекции самостоятельно. Укол коту в холку является самой простой процедурой, которая проходит безболезненно для животного. Внутримышечное введение приносит питомцу болезненные ощущения, поэтому кота приходится крепко фиксировать, чтобы выполнить инъекцию без негативных последствий. Капельница или внутривенный укол может выполняться только ветеринаром в клинике. Если процедура проведена неправильно, появляются симптомы серьезных осложнений и нужно обращаться к врачу.
Капельница или внутривенный укол может выполняться только ветеринаром в клинике. Если процедура проведена неправильно, появляются симптомы серьезных осложнений и нужно обращаться к врачу.
Места для лучшего введения лекарства в холку и внутримышечно
Зачем уметь правильно делать питомцу уколы?
Когда больному любимцу ветеринар выписывает медикамент в инъекционной форме, у владельца возникает необходимость учиться колоть кота самостоятельно. Этот навык избавит от необходимости постоянных поездок в клинику или вызова врача на дом, сократит затраты на инъекции. К тому же питомец легче перенесет процедуры в домашних условиях, под опекой любимого человека, чем в незнакомом кабинете с чужими людьми. Это позволит избежать стресса у кота. Когда животному требуется неотложная помощь, умение владельца правильно делать уколы может спасти жизнь питомцу. Возможно, понадобится оказать помощь другим котам и их хозяевам. Чтобы научиться всем нюансам проведения инъекции, нужно попросить ветеринарного врача показать правильное выполнение, а потом поставить укол под его наблюдением.
Вернуться к оглавлению
Виды инъекций
Выбор разновидности инъекционного введения лекарства выбирает врач. Одни медикаменты требуют накопления, а другие действуют быстро. От этого зависит как именно и куда нужно вводить препарат. Чаще всего выписывается укол в холку или в мышцу бедра, их хозяева могут делать дома сами. Если питомец в тяжелом состоянии и ему нужна капельница — следует доставить его в клинику. Виды уколов для котов:
Одним из распространенных мест для инъекций является мышца бедра, куда укол могут сделать и хозяева.- внутримышечный;
- подкожный;
- внутривенный;
- внутриартериальный;
- внутрикостный.
Постановка уколов внутрь кости или в вену требует профессионализма, делать их котам дома опасно.
Вернуться к оглавлению
Внутримышечно
Инъекции в мышцу назначаются, чтобы лекарство постепенно попадало в русло крови.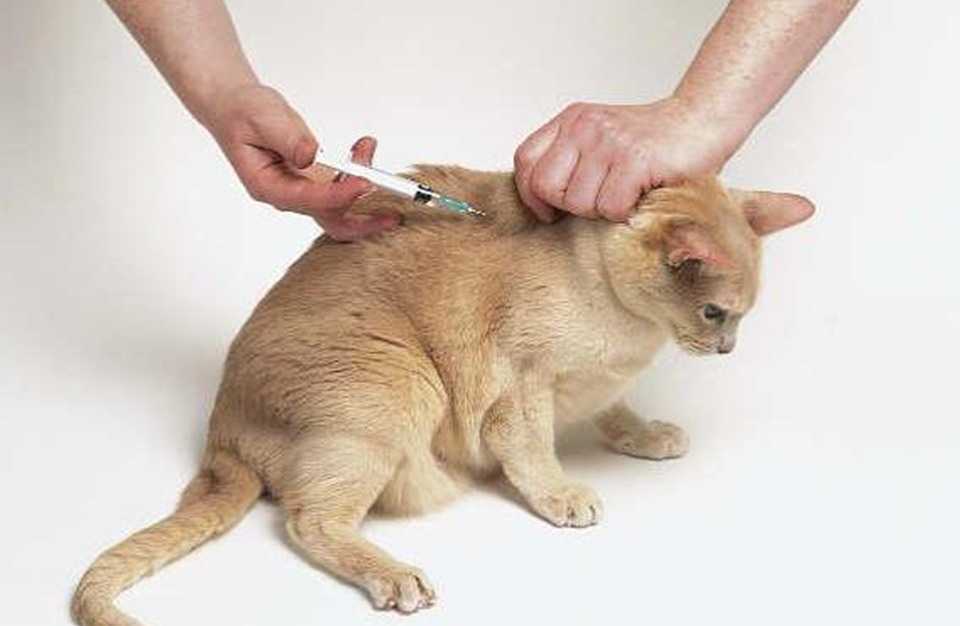 Так можно колоть нейролептическое средство, антибиотик или препарат, создающий инфильтраты после введения под кожу. Из лекарственного раствора формируется депо с медленным высвобождением действующего вещества. Благодаря этому необходимая лечебная концентрация препарата сохраняется надолго. Также преимуществом внутримышечных инъекций является быстрое всасывание. Эффект от лекарств начинается спустя 10 минут после инъекции. Уколы в мышцу болезненны для кошек, а превышение дозы медикамента расслаивает и травмирует мускулы.
Так можно колоть нейролептическое средство, антибиотик или препарат, создающий инфильтраты после введения под кожу. Из лекарственного раствора формируется депо с медленным высвобождением действующего вещества. Благодаря этому необходимая лечебная концентрация препарата сохраняется надолго. Также преимуществом внутримышечных инъекций является быстрое всасывание. Эффект от лекарств начинается спустя 10 минут после инъекции. Уколы в мышцу болезненны для кошек, а превышение дозы медикамента расслаивает и травмирует мускулы.
Вернуться к оглавлению
Введение инъекции подкожно
Укол кошке между лопаток назначается чаще всего. Подкожное пространство пронизано сеткой сосудов, поэтому лекарство быстро всасывается. Эта манипуляция несложная для хозяев животного. Подкожный укол не приносит сильных болезненных ощущений даже котенку. Существуют препараты, предназначенные исключительно для введения под кожу, например, гормональные медикаменты для кошек от течки.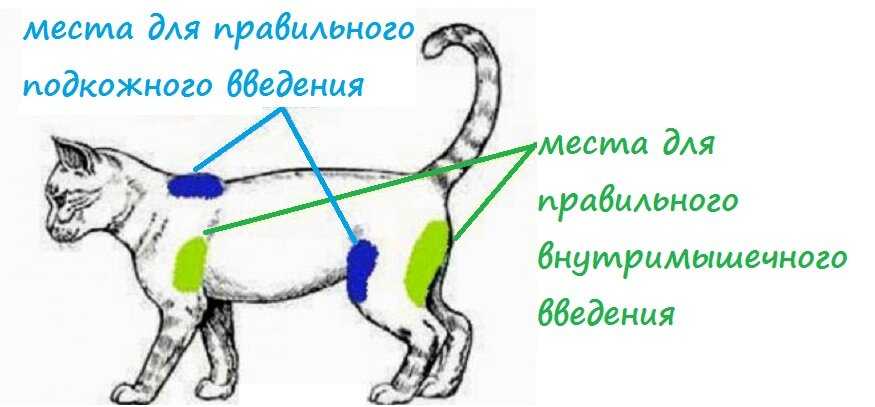 Доза лекарств может быть больше, чем при внутримышечном уколе.
Доза лекарств может быть больше, чем при внутримышечном уколе.
Вернуться к оглавлению
Правила и техника постановки инъекций
Перед процедурой необходимо тщательно вымыть руки и продезинфицировать место введения лекарства.Прежде чем ставить укол, нужно обязательно хорошо помыть руки, подготовить стерильные шприцы, ампулы или флаконы с медикаментами. Место инъекции не должно быть грязным, раздраженным или воспаленным, шерсть в этой зоне желательно выстричь. Если медикамент хранился в холодильнике, его необходимо подогреть, зажав в руке или поместив в теплую воду. Обязательно следует проверить наименование и срок годности препарата. Набирать раствор и снимать с иголки колпачок нужно непосредственно перед уколом.
Как правильно и как неправильно
Нельзя смешивать несколько препаратов, если это не указал врач. Ветеринар может набрать лекарства в несколько шприцов, которые хранятся в холодильнике не более 3 дней. Важно, чтобы владелец не испытывал страха, жалости, неуверенности, поскольку это отразится на поведении питомца. Лучше привлечь напарника, который будет держать и успокаивать кота. Техника выполнения уколов:
Лучше привлечь напарника, который будет держать и успокаивать кота. Техника выполнения уколов:
- Вскрыть ампулу или флакон и разбавить порошковое лекарство растворителем.
- Надеть иголку.
- Набрать нужную дозу лекарства.
- Удалить воздух, удерживая шприц в вертикальном положении и выпустив капельку лекарства.
- Зафиксировать кота на руках, чтобы зона инъекции была доступна, а движения питомца ограниченными.
- Уверенным, но не резким движением ввести иголку под определенным углом.
- После инъекции похвалить питомца и поощрить вкусненьким, а место прокола легко помассировать.
Вернуться к оглавлению
Выбор инструмента инъекции
Для проведения инъекции в небольших дозах или маленьким котятам рекомендовано использовать инсулиновый шприц.Чтобы сделать кошке укол на дому, подойдут аптечные шприцы с тонкими иголками и не слишком тугим поршнем. Если животному нужно ввести дозу менее 1 мл, лучше брать инсулиновый. Его используют для инъекций котятам. Для большей дозировки нужен объем 2—5 кубиков, а для введения физраствора либо глюкозы — 10. Иголка должна быть тонкой и острой. После прокола резинового флакона иглы затупляются, поэтому для инъекции нужно брать новые.
Его используют для инъекций котятам. Для большей дозировки нужен объем 2—5 кубиков, а для введения физраствора либо глюкозы — 10. Иголка должна быть тонкой и острой. После прокола резинового флакона иглы затупляются, поэтому для инъекции нужно брать новые.
Вернуться к оглавлению
Куда колоть?
Внутримышечный укол кошке делается в бедро или плечо. Чтобы правильно выявить зону введения иголки, нужно положить кота на бок, завернув в полотенце и оставив его попу в доступе. Затем следует ощупать заднюю лапу. Мышца бедра будет перекатываться между пальцами. Если мускулы кота напряжены, перед инъекцией их нужно расслабить легким массажем. Укол кошке подкожно ставится в холку или колено. Нужно взять любимца за загривок и слегка потянуть, формируя кожную складку. В ее основание вводится иголка до ощущения провала и пустоты.
Если питомцу назначили много инъекционных медикаментов, необходимо менять места уколов, а часть препаратов по возможности заменить пероральными.
Вернуться к оглавлению
Как вводить лекарство?
Внутримышечные уколы делаются под прямым углом, при этом большой объем лекарства вводить надо медленно.В мышцу игла вставляется под прямым углом, в кожную складку — под наклоном 45°, параллельно ходу позвоночника. Инсулиновый шприц можно вводить до упора, а глубина иголки для подкожных и внутримышечных инъекций не превышает 1—1,5 см. Если объем лекарства большой — вводить его нужно медленно, на протяжении 2—4 секунд. Для малых доз достаточно одной. Уколоть болезненный антибиотик, разбавив его анестетиком, можно только с разрешения ветеринара.
Вернуться к оглавлению
Осложнения от процедуры
Неправильный выбор зоны введения иголки провоцирует появление у питомца хромоты, которая проходит через несколько дней после инъекции. Если кот не способен стать на ногу более недели или волочит ее за собой, вероятно поврежден нерв и нужно показать питомца врачу. На месте прокола может выступить кровь. Необходимо остановить ее ватным диском, смоченным в перекиси водорода, приложить завернутые в полотенце кусочки льда.
На месте прокола может выступить кровь. Необходимо остановить ее ватным диском, смоченным в перекиси водорода, приложить завернутые в полотенце кусочки льда.
Если кровотечение продолжается — стоит немедленно отправляться в ветклинику. Процедура инъекции может вызвать местную реакцию в форме уплотнений на коже. К пораженному месту можно прикладывать нагретые мешочки с солью или песком. Но если у питомца поднялась температура, он стал отказываться от еды, а зона укола размягчилась — возможно развитие абсцесса или флегмоны.
Необходимость укола для питомца и техника инъекции: внутримышечно и подкожно
Содержание:
- Куда делать укол кошке
- Подкожно в холку или коленную складку
- Внутримышечно в ткани бедра или плеча
- Внутривенно в кровеносные сосуды передних или задних конечностей
- Внутрикостное в губчатую ткань
- Внутрибрюшинное в середину живота
- Правила выполнения
- Как подготовить кошку
- Как подготовить инструменты, шприц
- Правила ввода лекарства
- Укол в холку
- Массаж места укола
Регулярное посещение ветеринарного кабинета для постановки необходимого укола не всегда представляется возможным. Тем более, что некоторые процедуры можно проводить самостоятельно в домашних условиях. Существует два типа уколов, которые хозяин может сделать сам дома: внутримышечный и подкожный. В данной статье будет рассмотрен последний вариант и в частности, как делать инъекцию коту под холку.
Тем более, что некоторые процедуры можно проводить самостоятельно в домашних условиях. Существует два типа уколов, которые хозяин может сделать сам дома: внутримышечный и подкожный. В данной статье будет рассмотрен последний вариант и в частности, как делать инъекцию коту под холку.
Куда делать укол кошке
Перед тем как сделать укол коту, необходимо четко определить место для введения инъекции. В домашних условиях это делается только внутримышечно или подкожно. Все прочие варианты, такие как внутрикостное, внутрикожное, внутривенное, внутриартериальное — проводятся исключительно специалистами в ветеринарной клинике.
Какие поверхности выбираются для постановки укола в домашних условиях:
- при подкожном уколе выбирается холка или складка кожи колена;
- внутримышечная инъекция может быть поставлена в бедро или плечо животного.
Подкожно в холку или коленную складку
Для подкожного введения лекарства, больше всего подходят шприцы объемом на 2 или 3 мл. Если введение медикамента установлено в меньшей дозе (до 1 мл.), можно использовать шприц для введения инсулина, предварительно сменив иглу.
Если введение медикамента установлено в меньшей дозе (до 1 мл.), можно использовать шприц для введения инсулина, предварительно сменив иглу.
Укол в бедро
Инсулиновая игла является слишком тонкой и короткой. В данном случае, для проведения инъекции кошке, подойдет иголка от двухграммового шприца. Перед тем как ставить укол, необходимо провести все установленные предварительные процедуры.
Для справки: при подкожном введении, чаще выбирают холку, поскольку данный участок тела наименее восприимчив к болевым ощущениям.
Внутримышечно в ткани бедра или плеча
Подкожная инъекция является одной из самых простых, однако животным нередко выписывают препараты, которые вводятся исключительно внутримышечно. Объясняется это достаточно просто. Ряд лекарств плохо растворяется при подкожном введении, раздражая ткани.
Подготовка перед введением препарата, будет стандартной. Предпочтительнее вводить иглу в область бедра, постольку она является более мясистой и даже неопытный человек с малой долей вероятности сможет повредить внутренние структуры.
При постановке укола в мышцу ноги, лучше всего использовать инсулиновый шприц и иглу от него. Диаметр иголки значительно меньше, а значит и шансы навредить животному невелики. Такой вариант подходит для большинства лекарств, кроме густых, на масляной основе.
Внутривенно в кровеносные сосуды передних или задних конечностей
Внутривенные инъекции делаются только в ветеринарной клинике, специалистом. Также врач может провести процедуру в домашних условиях. Подобные уколы нельзя выполнять самостоятельно. Укол в вену обычно необходим, если требуется максимально быстрая реанимация.
Чаще всего, при внутривенных уколах, для большего удобства используются катетеры. Постановка катетера также актуальна, если необходимо провести серию уколов, например до и после операции.
Внутрикостное в губчатую ткань
Уколы подобного типа делают животным, если у них наблюдается падение артериального давления, имеется деформация конечностей или сильные ожоги. Подобный род инъекций также не производится в домашних условиях.
Правильно поставить внутрикостный укол в губчатую ткань способен только профессиональный врач ветеринар.
Внутрибрюшинное в середину живота
Подобный способ введения препарата используется, если у животного имеется обезвоживание организма, но при этом внутривенное введение вещества невозможно, по каким-либо причинам. Еще один тип укола, который делается только в ветеринарной клинике.
Правила выполнения
Как сделать клизму коту в домашних условиях
Как сделать укол кошке в холку? Прежде всего, к процедуре необходимо заранее подготовиться. Лучше всего хозяину животного придерживаться основных правил, которые помогут повести процедуру без вреда для животного.
Уколы котенку делаются аккуратно
Основные правила, проведения процедуры:
- Назначение лекарственно средства проводится только лечащим врачом. Нельзя самостоятельно выбирать и по своему усмотрению вводить препараты питомцу.
- Перед тем, как ставить укол, человеку необходимо хорошо помыть руки.
 Шерсть и кожа животного не обрабатываются.
Шерсть и кожа животного не обрабатываются. - Нельзя выбирать для укола участок кожи на котором имеются какие либо повреждения (царапины, ожоги, укусы).
- Большинство препаратов, в том числе и антибиотики, хранятся в холодильнике, но вводить их животному при такой температуре нельзя. Поэтому, перед тем как ставить укол, лекарство заблаговременно вынимается из холодильника и согревается в ладони на протяжении 2-3 минут.
- Нельзя вводить питомцу просроченные медикаменты. Предварительно проверяется их срок годности.
- Одним шприцом может вводиться только один медикамент. Нельзя вводить разные препараты единым шприцом, невозможно предсказать химическую реакцию и как это в последующем скажется на состоянии питомца.
- Если животному вводится препарат на масляной основе, стоит особенно внимательно следить за тем, чтобы он не попал в кровеносные сосуды. В противном случае, это может привести к смерти.
- В шприц набирается только одна доля вещества, рассчитанная на конкретную инъекцию.
 Оставлять лекарственные препараты «про запас» категорически запрещается.
Оставлять лекарственные препараты «про запас» категорически запрещается. - Перед тем как вводить вещество из шприца выпускается воздух.
Не стоит ставить укол самостоятельно, если есть сомнения в правильности действий или страх причинить животному боль. Также лучше доверить процедуру профессионалу, если питомец активно сопротивляется.
Как подготовить кошку
Самый лучший вариант — это привлечь помощника, который смог бы удержать животное на месте. Очень важно надежно зафиксировать питомца, чтобы исключить резкие движения и рывки. В противном случае, в момент прокалывания игла может войти слишком глубоко в мышцу.
Как можно подготовить животное:
- зафиксировать питомца в положении лежа, удерживая задние и передние лапы;
- надежно запеленать кошку в полотенце, оставив открытым только место для укола.
Если процедуру приходится проводить самостоятельно, лучше всего положить кота на плоскую поверхность и упереться предплечьем одной руки в корпус животного, а другой ставить укол.
Очень важно самому сохранять спокойствие и действовать уверенно, поскольку животные хорошо чувствуют страх и другие негативные эмоции, исходящие от хозяина. Можно гладить кота по голове и разговаривать с ним ласково.
Важно! Колоть котенка следует особенно аккуратно, чтобы не допустить травмы.
Как подготовить инструменты, шприц
Перед тем, как делать укол кошке или коту в холку, следует подготовить медикаменты и шприц. Обязательно следует проверить срок годности вводимого вещества. Следует помнить о том, что нельзя вводить животному слишком холодный препарат (который только что достали из холодильника), его необходимо согреть в руке в течение 2-3 минут.
Убираем воздух из шприца
Шприц выбирается исходя из количества вводимой дозы. Предварительно человеку потребуется помыть и высушить руки.
Далее следует провести следующие манипуляции:
- Отломить наконечник ампулы или снять защитный колпачок.
- Распаковать шприц, вставить иглу.

- Вытолкнуть весь воздух.
- Набрать лекарство в шприц, потребуется чуть больше, чем нужно для укола.
- Держа шприц вертикально, надавить на поршень, чтобы из иглы вышел небольшой фонтанчик. Так исключается наличие оставшихся пузырьков воздуха.
- До того, как кошка будет подготовлена, шприц с иглой помещается на чистую салфетку, при этом игла закрывается защитным колпачком. Нельзя трогать или снимать колпачок непосредственно до самой постановки инъекции.
Правила ввода лекарства
Перед тем как непосредственно вводить препарат в организм животного, следует ознакомиться с некоторыми правилами, касающимися скорости введения лекарства и объемами.
Прежде всего, о скорости — она зависит не только от количества используемого вещества, но и от его консистенции.
Раствор на водной основе вводится достаточно быстро. Скорость примерно 1 мл за 1 секунду. Вещества на масляной основе более густые и поэтому время ввода увеличивается в 2-3 раза.
Если вещество вводится под кожу, то допускается использование большего объема. Тем не менее количество не должно превышать показателя в 90 мл на 1 килограмм животного. Для такого количества используются стандартные шприцы по 10 мл, но их набирают сразу и используют, не вынимая иглы из животного. Просто опустевшие сменяются новыми.
Укол в холку
Как измерить температуру кошке в домашних условиях
Укол в холку считается наиболее безболезненным вариантом введения лекарственного вещества. Кроме того, данный способ лучше всего подходит для неопытного хозяина. В холке очень мало нервных окончаний, а значит животное будет меньше дергаться и нервничать.
Сама схема введения инъекции достаточно проста.
Пошаговая инструкция:
- Кожа на холке оттягивается вверх. Для питомца это совершенно безболезненно, кожа спокойно поднимается на 3-4 сантиметра.
- Оттянув кожу, на нее следует слегка нажать пальцами, чтобы получился небольшой кармашек. В него и будет вставляться игла.

- Шприц должен держаться параллельно позвоночнику. Не следует пытаться протыкать шприц слишком глубоко, нужно всего на 1-2 сантиметра.
- После того, как игла будет помещена в тело животного, можно постепенно вводить лекарственный препарат. Лучше всего не торопиться и делать все медленно. Так можно почти исключить возникновение неприятных ощущений у питомца.
- Стоит внимательно следить за местом введения инъекции. Если шерсть становится мокрой, значит прокола нет, а вещество не поступает в организм кошки.
- После завершения процедуры, следует аккуратно извлечь иглу. Не нужно сразу отпускать животное с рук. Лучше всего подержать его, погладить и успокоить.
- Для того, чтобы медикамент быстрее разошелся по организму, место укола следует немного помассировать.
В отличие от людей, место будущего прокола у животных не обрабатывается никакими обеззараживающими веществами, поэтому готовить ватку со спиртом не нужно.
Шприц с веществом готовится заранее. Как уже говорилось, вещество вводится в чуть большем количестве, чтобы можно было легко выпустить оставшийся в колбе воздух. Не стоит также забывать про чистоту. Подготовленный шприц остается лежать на чистой салфетке, непосредственно до момента использования.
Как уже говорилось, вещество вводится в чуть большем количестве, чтобы можно было легко выпустить оставшийся в колбе воздух. Не стоит также забывать про чистоту. Подготовленный шприц остается лежать на чистой салфетке, непосредственно до момента использования.
Шприц держится вдоль позвоночника
Лучше всего расположить кошку в так называемой позе сфинкса. Так будет значительно удобнее вводить вещество ей под кожу. Хорошо, если есть кто-то готовый помочь в проведении процедуры и надежно фиксирующий питомца.
Тем не менее, уложить кошку в позу сфинкса можно и самостоятельно, аккуратно ее придавив к поверхности и поставить инъекцию. Если не получается, не стоит мучить себя и животное. Кошку с норовом лучше всего завернуть в полотенце и надежно зафиксировать.
Правила ввода шприца:
- Игла вводится под кожу под углом в 45 градусов к позвоночнику котенка, а не перпендикулярно. Вводится аккуратными, плавными движениями на расстояние не более 1-2 сантиметров. Если используется инсулиновый шприц, игла войдет полностью из-за ее небольших размеров.

- После введения препарата, игла осторожно вынимается из тела животного. До окончания процедуры кожа придерживается все в том же приподнятом положении.
Не стоит беспокоиться, если после завершения процедуры, на месте укола появилось небольшое количество крови. Лучше всего смочить ватный тампон дезинфицирующим средством и протереть ранку.
Массаж места укола
Как помочь кошке при родах в домашних условиях
Обычно, если все сделать правильно, после укола животное не испытывает никаких неприятных ощущений. Тем не менее, можно немного облегчить состояние питомца и сделать ему легкий массаж.
Для этого место укола немного проглаживается пальцами руки. В особенности данная процедура подходит после того, как была сделана внутримышечная инъекция.
Также небольшой массаж в месте прокола делается для того, чтобы введенное вещество быстрее разошлось по организму. Специалисты рекомендуют некоторое время подержать питомца на руках и растирать кожу на протяжении 1-2 минут.
Как можно понять, процедура постановки укола в холку не относится к особенно сложным. Хозяину требуется только сохранять спокойствие самому и максимально успокоить своего любимца. Достаточно провести процедуру всего один раз, чтобы понять ее основы и уже в дальнейшем выполнять инъекции без лишней суеты и страхов.
Автор:
Мила — копирайтер и знаток животного мираКак сделать кошке укол в домашних условиях: внутримышечно, подкожно (в холку)
Многие кошачьи заболевания предполагают лечение в виде целого курса инъекций. Назначенные уколы может ставить специалист, но, имея определенные знания, эту манипуляцию вполне реально осуществить хозяину заболевшего питомца. Как сделать кошке укол, дабы не причинить вред любимцу? Немного знаний в комплексе с практическими действиями помогут провести процедуру верно и безболезненно.
Как сделать кошке укол, дабы не причинить вред любимцу? Немного знаний в комплексе с практическими действиями помогут провести процедуру верно и безболезненно.
Самостоятельно сделать укол больному усатику можно внутримышечно и подкожно. Проще всего попасть в область бедра и в холку. Другие виды уколов, такие как: внутривенные, внутрикостные и внутриартериальные – должен проводить исключительно человек с опытом.
Содержание статьи
- 1 Необходимые знания
- 2 Подготовительный этап
- 3 Как делать укол кошке подкожно (в холку)?
- 4 Как делать кошке внутримышечный укол?
- 5 Поведение кошки после инъекции
Необходимые знания
- Не нужно самостоятельно выбирать лекарства для инъекций больному усатику. Весь курс должен прописывать специалист.
- Предварительно осмотрите область кожи, куда будет вводиться укол – она должна быть здоровой, без всяких воспалений.
- Если препарат не на основе масла и не превышает в объеме 1 мл, то подойдут инсулиновые шприцы.
 В иных случаях должны применяться шприцы с объемом 2 и более мл.
В иных случаях должны применяться шприцы с объемом 2 и более мл. - Температура вводимого препарата должна быть около 37 градусов, поэтому лекарства из холодильника подогреваются.
- Не стоит соединять одновременно два и более препаратов. Исключение – назначение специалиста.
- Наилучшее решение – проводить манипуляцию вдвоем: один держит усатика, другой в быстром темпе делает подкожный укол кошке, либо какой-то другой. Предварительно необходимо настроиться и быть уверенным в своих действиях, ведь любое переживание усатик почувствует и будет тревожиться.
- Для того, чтобы больной любимец с каждым разом более благоприятно относился к процедуре, перед ней его можно немного покормить, если на это нет противопоказаний.
- Препараты на основе масла нужно вводить аккуратно – перед тем как нажать поршень шприца, следует удостовериться, что он не попал в сосуд (это очень опасно для жизни питомицы) – нужно потянуть поршень на себя и если внутри шприца окажется кровь, то обязательно нужно сделать укол в ином месте.
 При сильном беспокойстве и неуверенности, стоит обратиться к специалисту.
При сильном беспокойстве и неуверенности, стоит обратиться к специалисту.
Подготовительный этап
- Продезинфицируйте руки перед тем, как делать уколы больным кошкам. До иглы дотрагиваться не нужно, дабы избежать попадания микробов.
- Каждая последующая инъекция в обязательном порядке делается новым шприцом с одноразовой иголкой;
- Уже распечатанную ампулу, содержимое которой взаимодействовало с окружающей средой, не в коем случае использовать нельзя;
- Убедитесь, что в ампуле находиться необходимое лекарство. Обратите внимание на сроки.
- Перед тем, как извлечь лекарство, из шприца необходимо выгнать весь воздух.
- Для того, чтобы набрать лекарство, шприц нужно держать под наклоном иглой вверх.
Саму питомицу тоже следует подготовить перед манипуляцией. Самое важное – это фиксация усатого создания на одном месте и его спокойное состояние. Можно положить больную питомицу на стол, накрытый мягкой тканью. После чего, вытянуть ее задние конечности, кошка по инстинкту вцепится коготками в ткань.
Если любимица очень беспокойна, то следует завернуть ее в простыню, а место, куда будет вводиться инъекция оставить открытым.
Также, существуют специальные сумки-фиксаторы на молниях. Усатик помещается внутрь такой сумочки, фиксируется молниями, а та область тела, куда хозяин будет делать укол коту, открывается.
Как делать укол кошке подкожно (в холку)?
Делать подкожный укол можно в разные области тела – в загривок или холку, между лопатками или в место, где образуется складка на колене. Если сомневаетесь куда делать укол кошке, то остановите выбор на первом варианте, т. к. именно загривок считается наименее чувствительной областью кошачьего тела. Не зря, за это место мама кошка переносит на другой участок своих маленьких пушистиков.
Чтобы правильно научиться делать укол кошке в холку, нужно знать технику:
- следуя всем вышеперечисленным правилам, вы фиксируете питомицу. Можно придавить больное создание предплечьем левой руки, после, этой же рукой следует нащупать и сформировать складочку, которую нужно аккуратно оттянуть вверх;
- делать укол в холку кошке нужно правой рукой, соблюдая угол в 45 градусов.
 Игла вводиться в складку по одной параллели с позвоночником. При использовании инсулинового шприца, иголку нужно вести полностью, в других случаях – на глубину 1-2 см;
Игла вводиться в складку по одной параллели с позвоночником. При использовании инсулинового шприца, иголку нужно вести полностью, в других случаях – на глубину 1-2 см; - в первые минуты вы будете чувствовать некое сопротивление, но после того, как произойдет попадание препарата под кожный покров – все успокоиться, поэтому вводите лекарство без спешки;
- по окончанию всего действия, следует вынуть иголку, продолжая держать кожу оттянутой. Обязательно ласковым голосом поблагодарите питомца и погладьте.
Если после всех манипуляций, вы заметили, что шерстка усатика в области холки стала влажной, то скорее всего прокол был сделан насквозь и препарат не попал куда следует.
Как делать кошке внутримышечный укол?
Существует препараты, которое необходимо вводить исключительно внутримышечно. Также многие лекарства при подкожном введении вызывают у усатика сильные болевые ощущения, тогда выбирают внутримышечный укол кошке, когда действующее вещество из препарата высвобождается в кровяное русло не слишком быстро, т. е. концентрация остается постоянной, без скачков.
Также многие лекарства при подкожном введении вызывают у усатика сильные болевые ощущения, тогда выбирают внутримышечный укол кошке, когда действующее вещество из препарата высвобождается в кровяное русло не слишком быстро, т. е. концентрация остается постоянной, без скачков.
В экстренных случаях, когда нужен быстрый результат от лекарства, но внутривенная инъекция невозможна – вводят укол кошке внутримышечно.
Если такой укольчик вы ставите самостоятельно, то удобнее всего делать его в область бедра.
Как делать укол кошке в бедро? Чтобы манипуляция прошла успешно, следует обратить внимание на ниже перечисленные рекомендации:
- зафиксируйте усатика на твердом и устойчивом столе или положите его живот на свое колено. Лучше всего проводить процедуру с кем-то в паре;
- иголку нужно вводить в середину тазобедренного сустава – в его самую мягкую область. Сразу прощупайте, где в этом месте проходит кость и исключите попадание иголки в нее;
- обратите внимание, направление иголки должно быть с задней стороны лапки под углом 45 градусов;
- перед уколом, помассируйте всю область бедра, чтобы мышца расслабилась.
 При ее напряжении укол не нужно делать. Согните конечность и продолжайте поглаживать до тех пор, пока она не расслабиться;
При ее напряжении укол не нужно делать. Согните конечность и продолжайте поглаживать до тех пор, пока она не расслабиться; - очень важна хорошая фиксация усатика, т. к. сделанный укол вызовет неприятные ощущения у питомца, он может дернуться в определенный момент или вообще освободиться и убежать. Затягивать процедуру не стоит – все действия должны быть быстрыми и четкими;
- чтобы не попасть в костную ткань, следует вводить иголку не более чем на 1 см в мышцу.
- после введения препарата, нужно в первую очередь изъять иглу из кожи, а уже после выпустить усатика.
Если котенок или взрослый кот должны пройти длительный курс внутримышечных инъекций, то следует каждый день чередовать лапки, куда будет ставиться укол.
Если у питомицы после укола началось обильное кровотечение, то необходимо к области тела, которое кровоточит, приложить холодный компресс и поддержать его 10-15 минут. Немедленно обратитесь к специалисту, если после компресса кровь продолжает идти.
Поведение кошки после инъекции
Усатик может начать прихрамывать и это не страшно, если хромота не затянулось более чем на три дня, тогда нужно показать питомицу врачу.
Если кошечка не может опереться на лапку и волочит ее за собой, то скорей всего был поврежден нервный пучек – везите больную к врачу, где ее избавят от болевых ощущений.
При нормальном поведении кошки, обязательно обследуйте место укола – при появлении шишек или припухлости кожи, обращайтесь в ветклинику.
Похожие статьи
Ako mačke aplikovať injekciu — FIP Warriors CZ/SK®
Подготовка кошки к инъекции
Подкожная инъекция
Внутримышечная инъекция
Оригинал статьи на wikihow. com, 15.05.2019
com, 15.05.2019
Инъекции часто являются проблемой для владельцев. Техническим термином для категории инъекционных лекарственных средств является лекарство для подкожного введения , что означает, что оно применяется подкожно. Некоторые подкожные препараты просто вводятся под кожу, в то время как другие виды подкожных препаратов необходимо вводить внутримышечно (внутримышечная инъекция), а способ введения будет зависеть от желаемого места инъекции. Правильное подкожное введение может помочь снизить уровень стресса и сохранить вашу кошку счастливой и здоровой.
Подготовка кошки к инъекции
Убедитесь, что ваша кошка обезвожена. Если вы делаете кошке подкожные инъекции, важно, чтобы кошка гидратировалась до и после введения. Если ваша кошка сильно обезвожена, лекарства, которые вы даете, могут не полностью всасываться. Это не должно быть проблемой для большинства здоровых кошек, но если вы подозреваете, что ваша кошка может быть обезвожена, вам следует проконсультироваться с ветеринаром о том, как поддерживать водный баланс.
Решите, куда вы хотите сделать инъекцию. Вы можете держать свою кошку на коленях, чтобы успокоить ее во время инъекции, но это увеличивает вероятность того, что кошка может поцарапать или травмировать вас, и может вызвать у вас ассоциации пребывания на коленях с инъекциями. Если вы решите держать кошку у себя на коленях, лучше всего надеть грубое полотенце, чтобы прикрыть ноги. Однако лучше всего разместить кошку на ровной поверхности, например на столе.
Выберите подходящее место для инъекции. Место инъекции зависит от того, делаете ли вы однократную подкожную инъекцию или внутримышечную инъекцию. Слишком много приложений в одном месте может стать проблемой для вашей кошки. Это связано с тем, что кошачьему телу требуется от шести до восьми часов, чтобы полностью впитать введенную жидкость. Если вы нанесете слишком много лекарств на одно место до того, как они впитаются, это может вызвать накопление жидкости, называемое отеком. Это может раздражать вашу кошку и может помешать действию многих лекарств, которые вы даете, в организме вашей кошки.
- Вы должны быть в состоянии ввести от 10 до 20 мл лекарства на килограмм массы тела, прежде чем вам придется выбирать новое место инъекции.
- Проверьте вашу кошку, чтобы убедиться, что инъекции адекватно всасываются. Область вокруг места инъекции должна оставаться сухой.
Протрите место инъекции тампоном, смоченным спиртом. Большинству кошек этот шаг не нужен, если только у них не нарушена иммунная система. Бактерицидный эффект – лишь одно из преимуществ. Ослабив шерсть, вы сможете лучше видеть кожу при инъекции.
Используйте еду, чтобы отвлечь внимание. Непосредственно перед инъекцией дайте кошке действительно приятный вкус, например консервированный консерв или тунец. Как только он начнет есть, слегка пощипывайте кожу в месте укола. Примерно через пять секунд вы должны перестать зверствовать и взять еду. Верните еду и на этот раз пощипывайте (пощипывайте) сильнее. Повторяйте это до тех пор, пока ваша кошка не станет терпимой к укусам и не сосредоточится на еде. Это поможет ей подготовиться к инъекции и уменьшит боль и стресс, которые она испытывает во время инъекции.
Это поможет ей подготовиться к инъекции и уменьшит боль и стресс, которые она испытывает во время инъекции.
Подкожная инъекция
Найдите место с дряблой кожей. В целом области между шеей и спиной кошки являются самыми свободными и подвижными местами. Аккуратно сжимайте и растягивайте кожу там, где она наиболее рыхлая, держите ее между большим и указательным пальцами и отвлекайте кошку едой. Получившаяся форма напоминает палатку.
Вставьте иглу. Когда кожа плотно сложена между пальцами, вы должны увидеть узкую полоску кожи между большим и указательным пальцами. Вставьте иглу в эту область.
- Иглу всегда следует держать параллельно коже вдоль спины кошки. Наклон иглы может проткнуть кожу с другой стороны, и игла может уколоть палец.
- Не держите большой палец над поршнем, пока не убедитесь, что игла вставлена правильно. Удерживание поршня при введении иглы может привести к преждевременной инъекции, если кошка дернется или вы неправильно ввели иглу.

Перед инъекцией вытяните поршень. Важно, чтобы вы немного потянули поршень перед введением лекарства. Это гарантирует, что вы попали в место инъекции.
- Если кровь попадает в шприц после вытягивания поршня, это означает, что вы попали в сосуд. Вам нужно будет вытащить иглу и повторить попытку в другом месте.
- Если в шприц попадают пузырьки воздуха, это означает, что вы проткнули кожную складку и всосали воздух с другой стороны. Вам нужно будет вытащить иглу и повторить попытку.
- Если в шприц не попали кровь или пузырьки воздуха, вы попали в приемлемое место и можете продолжать инъекцию.
Введите содержимое шприца. Убедитесь, что вы ввели все лекарства. Когда шприц полностью опустеет, осторожно вытащите иглу и следуйте по тому же пути, которым вы вводили ее.
- Удерживая шприц между указательным, средним и большим пальцами (одной и той же рукой), нажмите на поршень.
Проверить на наличие кровотечения или утечки. Вы должны проверить место инъекции после инъекции. Если вы обнаружите, что из места инъекции вытекает кровь или лекарство, приложите чистый ватный тампон или ткань к месту инъекции, пока выделение не прекратится. Это должно занять около минуты или дольше, если кошка слишком беспокойна.
Вы должны проверить место инъекции после инъекции. Если вы обнаружите, что из места инъекции вытекает кровь или лекарство, приложите чистый ватный тампон или ткань к месту инъекции, пока выделение не прекратится. Это должно занять около минуты или дольше, если кошка слишком беспокойна.
Правильно утилизируйте использованную иглу. Не выбрасывайте шприц вместе с бытовыми отходами, так как иглы считаются биологически опасными отходами. Обратитесь к ветеринару, чтобы узнать, могут ли они утилизировать иглы. Никогда не выбрасывайте открытую иглу в мусорное ведро, так как это может привести к травме или заражению сборщика отходов или любого другого лица, имеющего дело с вашими отходами.
Внутримышечная инъекция
Найдите место инъекции. Ваш ветеринар должен дать вам конкретные инструкции о том, где вводить внутримышечное лекарство, и вы должны тщательно им следовать. Как правило, большинство ветеринаров рекомендуют внутримышечные инъекции в четырехглавую мышцу (верхняя часть бедра) или поясничные эпиксиальные мышцы позвоночника (дорсальные мышцы вдоль позвоночника).
- Будьте уверены при внутримышечных инъекциях чрезвычайно осторожны . Плохо вставленная игла может серьезно повредить нервы вашей кошки. По этой причине лучше следовать всем указаниям ветеринара. Если вы не уверены в какой-либо части инструкций вашего ветеринара или если вы не нашли рекомендуемое место инъекции дома, позвоните или посетите ветеринара для получения более подробных инструкций.
Вставьте иглу. Иглу следует вводить под углом от 45 до 90 градусов, в зависимости от места, выбранного для инъекции. Чтобы кошка не двигалась и чтобы игла правильно входила в мышцу, можно держать мышцу плоской.
- Убедитесь, что вы вводите иглу под правильным углом, как показано вашим ветеринаром. Введение иглы под слишком малым углом может помешать инъекции достичь необходимой глубины и проникнуть в мышцу.
- Не держите большой палец над поршнем шприца, пока не убедитесь, что игла вставлена правильно. Если вы коснетесь поршня во время введения иглы, это может привести к преждевременной инъекции, если кошка пошевелится или вы неправильно ввели иглу.

Перед введением потяните поршень. Как и при подкожной инъекции, перед инъекцией слегка потяните поршень. Пузырьки воздуха не должны быть проблемой при внутримышечных инъекциях, но если вы видите кровь, вы должны вытащить иглу и повторить попытку, так как это может привести к попаданию в кровеносный сосуд.
Введите содержимое шприца. Важно убедиться, что полная доза лекарства находится в шприце. Когда шприц полностью опустеет, вытащите иглу так же, как вы ее вставили.
- Удерживая шприц между указательным, средним и большим пальцами (одной и той же рукой), надавите на поршень.
Проверить отсутствие кровотечения или утечки. Проверьте место инъекции после инъекции. Если вы заметили признаки крови или вытекшего лекарства, прижмите чистую ватную палочку или тампон к месту инъекции. Кровотечение или утечка останавливаются при правильном давлении всего за одну минуту.
Утилизируйте иглу надлежащим образом. Использованные шприцы считаются биологически опасными отходами, поэтому их нельзя выбрасывать вместе с бытовыми отходами или оставлять непокрытыми в отходах. Спросите у ветеринара, утилизируют ли они использованные иглы.
Использованные шприцы считаются биологически опасными отходами, поэтому их нельзя выбрасывать вместе с бытовыми отходами или оставлять непокрытыми в отходах. Спросите у ветеринара, утилизируют ли они использованные иглы.
Кошачья саркома в месте инъекции | Сегодняшняя ветеринарная практика
На сегодняшний день среди всего спектра побочных эффектов вакцин, зарегистрированных у собак и кошек, кошачья саркома в месте инъекции (FISS) считается наиболее серьезной. Хотя это происходит нечасто, последствия злокачественной опухоли, развивающейся в месте прививки, разрушительны для пациента и владельца.
Примечание редактора: Эта статья была первоначально опубликована в июле 2013 года. Пожалуйста, используйте этот контент в справочных или образовательных целях, но обратите внимание, что он не подвергается активной проверке после публикации. Самый последний рецензируемый контент см. в нашем архиве выпусков.
Примите во внимание следующие факты:
- Опухоли, связанные с введением вакцины, представляют собой саркомы высокой степени злокачественности .

- Без лечения больные кошки умрут от осложнений, связанных с опухолью.
- Время от вакцинации до развития опухоли обычно составляет от 3 месяцев до 4 лет . Меньшее количество опухолей развивается через 5 и более лет после введения вакцины.
- Радикальное иссечение (края от 3 до 5 см и глубина 2 мышечных плоскостей) вместе с лучевой терапией рекомендуется при опухолях, возникающих на коже грудной клетки или живота. Ампутация конечности рекомендуется при опухолях в местах инъекций на конечности.
- Несмотря на агрессивную операцию, сообщается о частоте рецидивов до 50% . 1
- Местный рецидив часто возникает при попытке простого иссечения опухоли; 86% рецидивов развиваются в течение 6 мес. 1
- Легочные метастазы возникают у 21% кошек с диагнозом опухоли 3 степени.
 2
2
ИСТОРИЯ САРКОМ В МЕСТАХ ИНЪЕКЦИЙ
Связь с алюминием
Более 20 лет назад патологоанатомы из Пенсильванского университета сообщили о тревожном 61% увеличении числа фибросарком в месте инъекций среди кошачьих образцов биопсии из 19 образцов.с 87 по 1991 год. Это увеличение было эпидемиологически связано с принятием в 1987 году закона об обязательной вакцинации против бешенства домашних кошек, проживающих в Пенсильвании. 3,4
Электронно-зондовый микроанализ опухолей выявил алюминий (обычно используемый в качестве адъюванта в кошачьих вакцинах) в макрофагах, окружающих саркомы. Была выдвинута, но не доказана гипотеза, что стойкие воспалительные и иммунологические реакции на алюминиевые адъюванты могут привести к неопластической трансформации у кошек. 5
Роль адъювантов в патогенезе FISS
В 1993 г. эпидемиологическое исследование с участием 345 кошек с фибросаркомой показало, что вакцинация вирусом кошачьей лейкемии (FeLV) и вирусом бешенства вакцинами может привести к онкогенезу в месте инъекции, особенно при вакцинацию неоднократно вводили в одно и то же место. 6
6
На момент проведения исследования все вакцины против вируса FeLV и бешенства, лицензированные для кошек в США, были инактивированными продуктами с адъювантом. Этот факт вызвал обеспокоенность тем, что хроническое воспаление, вызванное вакцинами, содержащими адъювант, а не одной конкретной маркой вакцины, играет роль в патогенезе этих опухолей.
С первых дней открытия вакциноассоциированной саркомы (теперь известной как FISS) было опубликовано несколько исследований, которые характеризуют патологию опухоли, предлагают диагностические рекомендации, намечают варианты лечения пораженных кошек и оценивают показатели выживаемости.
- Понимание патогенеза FISS
- Определение истинной распространенности
- Снижение риска.
Краткая хронология FISS представлена в Таблице 1 .
| 1985 | Представлена первая FeLV-вакцина (инактивированная, с алюминиевым адъювантом) (Leukocell, Norden Laboratories). |
| 1985 | Аттенуированные вакцины против бешенства, продаваемые в США, заменены инактивированными вакцинами против бешенства с адъювантом. |
| 1987 | Пенсильвания предписывает введение вакцины против вируса бешенства домашним кошкам (в то время все вакцины против бешенства, продаваемые в США, были инактивированы и дополнены адъювантом). |
| 1991 | Письмо Университета Пенсильвании, Лаборатория хирургической патологии, опубликованное в JAVMA, указывает на значительное увеличение частоты возникновения саркомы в местах инъекций у кошек, что указывает на корреляцию между вакцинацией против бешенства и образованием опухолей. 3 |
| 1992 | Гипотеза, связывающая развитие опухоли у кошек с воспалительной реакцией на алюминий (адъювант) в местах инъекции вакцины, выдвинута, но не доказана; алюминий, обнаруженный внутри макрофагов вокруг опухолей в месте инъекции. 4 4 |
| 1993 | Доказательства связывают (инактивированные) вакцины против FeLV и вируса бешенства с онкогенезом. 4 |
| 1996 | AVMA и AAHA совместно спонсируют встречу, которая привела к созданию Целевой группы по вакциноассоциированной саркоме кошек (VAFSTF) для финансирования и планирования исследований, а также для продвижения образования и повышения осведомленности. |
| 1997 | Руководство для мест вакцинации рекомендует вводить антирабическую вакцину в дистальную часть правой задней конечности, FeLV в дистальную часть левой задней конечности и все другие вакцины в правую плечевую область. |
| 1999 | VAFSTF совместно с Ветеринарным онкологическим обществом рекомендует «Правило 3-2-1» (см. Таблицу 2) в отношении диагностики подозрений на саркомы. Таблицу 2) в отношении диагностики подозрений на саркомы. |
| 2001 | Правительственный отчет (Великобритания) о побочных реакциях на вакцины цитирует FISS, вероятность развития которых у кошек, получавших вакцины с алюминиевым адъювантом (FeLV), была в 5 раз выше, чем у кошек, получавших неадъювантные вакцины. (ПРИМЕЧАНИЕ: Великобритания свободна от бешенства, и собаки/кошки не прививаются от бешенства). 7 |
| 2004 | VAFSTF снят с производства; опубликовано обсуждение за круглым столом, посвященное разногласиям, связанным с управлением рисками FISS. 8 |
| 2009 | Опубликовано исследование со ссылкой на изменения в характеристиках FISS (392 случая) после рекомендаций для мест вакцинации VAFSTF: FISS уменьшился в межлопаточных областях, но более чем удвоился в тазовых конечностях. 9 9 |
| 2012 | В исследовании говорится, что кошки с FISS значительно реже получали рекомбинантные вакцины, чем инактивированные (адъювантные) вакцины; исследование также пришло к выводу, что ни одна вакцина не является безопасной. 10 |
ПРОБЛЕМЫ И СПОРЫ
Сегодня специалисты по-прежнему сталкиваются с неоднозначными рекомендациями и спорами по поводу управления рисками FISS.
Другие причины сарком
Большинство авторов согласны с тем, что вакцины не являются исключительно ответственными за возникновение сарком у кошек 1-3,6,8,10 ; сопутствующие причины включают:
- Репозиторий кортикостероидов
- Пенициллин пролонгированного действия
- Нейлоновая нить, оставленная на коже на длительное время
- Травма кожи.
Эти наблюдения подтверждают тот факт, что хроническое воспаление, вызванное различными причинами, может привести к онкогенезу у некоторых кошек.
Роль генетики и адъювантов
Не все кошки имеют одинаковый риск вакциноассоциированного онкогенеза, что подтверждает роль генетики в определении риска FISS. Некоторые авторы предполагают, что адъюванты, присутствующие в настоящее время во всех инактивированных кошачьих вакцинах, лицензированных в США, вызывают хроническое воспаление, которое может спровоцировать образование опухолей у генетически предрасположенных кошек. 8
Проблемы выбора вакцины
Рекомендации избегать использования инактивированных (адъювантных) вакцин у кошек встретили сопротивление со стороны промышленности. Это неудивительно, учитывая тот факт, что большинство вакцин против бешенства, продаваемых и вводимых в США, представляют собой инактивированные вакцины со сроком действия 1 и 3 года.
Кроме того, в США существует только по одной неадъювантной (рекомбинантной) вакцине против вируса FeLV и вируса бешенства (доступна только в виде вакцины со сроком действия 1 год). Эти вакцины стоят дороже за дозу, чем адъювантные (убитые) вакцины против FeLV и вируса бешенства, и этот фактор влияет на решения о покупке.
Эти вакцины стоят дороже за дозу, чем адъювантные (убитые) вакцины против FeLV и вируса бешенства, и этот фактор влияет на решения о покупке.
Термины в отношении вакцин
Адъювант : Химический, микробный компонент или белок млекопитающих, добавленный к инактивированной вирусной или бактериальной вакцине для усиления иммунного ответа на выбранный антиген
Аттенуированный иммунизирующий антиген. Вирулентность организма (антигена) снижается, но он все еще способен заражать клетки и размножаться после инокуляции. Аттенуированные вакцины не содержат адъюванта.
Инактивированная : Вакцина, содержащая убитый вирус или бактерию в качестве иммунизирующего антигена. После инокуляции антиген не способен инфицировать клетки или реплицироваться. Все инактивированные кошачьи вакцины, продаваемые в США и Канаде, содержат адъювант.
Рекомбинантная : Вакцина, изготовленная путем клонирования генов (плазмидная экспрессия) или путем рекомбинации выбранной ДНК патогенного организма с ДНК другого вируса (вирусная векторизация), что приводит к экспрессии после инокуляции только основных антигенов, необходимых для иммунизации. Рекомбинантные кошачьи вакцины, продаваемые в США и Канаде, не содержат адъюванта.
Рекомбинантные кошачьи вакцины, продаваемые в США и Канаде, не содержат адъюванта.
ЧТО ЕЩЕ НЕИЗВЕСТНО
Распространенность FISS
Опубликованные оценки распространенности FISS значительно различаются в зависимости от дизайна исследования, количества кошек в исследовании, географического местоположения кошек и того факта, что инъекции, отличные от вакцин Известно, что они вызывают саркомы.
Были приведены оценки распространенности от 1 на 10 000 кошек до 1 на 1000 кошек. Исследования, сообщающие о риске в зависимости от доз вводимой/продаваемой вакцины, также различаются (от 1 до 36 случаев на 10 000 доз). 11-16
Надежное отслеживание и отчетность о распространенности или доле кошек в популяции, у которых развились опухоли после вакцинации, имеют решающее значение для определения того, эффективны ли рекомендации по снижению или устранению риска с течением времени. Отслеживание распространенности FISS оказалось затруднительным по нескольким причинам, в том числе: низкая / непоследовательная отчетность о FISS, отсутствие централизованной базы данных и генетическое влияние.
Патогенез FISS
Несколько сложных исследований изучали клеточные и субклеточные изменения, связанные с FISS. Предлагаемые механизмы, как правило, сосредоточены вокруг:
- Хроническое воспаление
- Повышающая регуляция тромбоцитарного фактора роста и последующая пролиферация фибробластов
- Мутации в TP53 (так называемый «ген-супрессор опухоли»).
Хотя нет единого мнения относительно фактической роли этих факторов в патогенезе FISS, все согласны с тем, что явления, ведущие к образованию опухолей у кошек после введения вакцины, связаны со сложным взаимодействием: - Внутренние факторы, такие как индивидуальная генетика, природа и степень воспалительной реакции после инъекции
- Внешние факторы, такие как тип вводимой вакцины, частота введения и количество вакцин, вводимых в учреждении.
Что неизвестно, так это то, как эти факторы взаимодействуют у отдельной кошки, приводя к онкогенезу.
Прогнозирование FISS
Прогнозирование рака является важной новой областью медицины и ветеринарии. Например, способность обнаруживать мутации в генах BRCA1 и BRCA2 позволяет врачам выявлять женщин со значительным риском развития наследственного рака груди и яичников.
Например, способность обнаруживать мутации в генах BRCA1 и BRCA2 позволяет врачам выявлять женщин со значительным риском развития наследственного рака груди и яичников.
Мутации в гене TP53 у некоторых кошек с FISS были обнаружены в исследованиях, проведенных в Университете Миннесоты. Хотя эти исследования предполагают потенциал для оценки генетической предрасположенности к FISS, не существует коммерчески доступного теста, который мог бы надежно предсказать, у каких кошек разовьются опухоли.
Варианты нехирургического лечения
Если FISS подтвердится, текущие рекомендации последовательно указывают на роль радикальной хирургии с лучевой терапией для продления жизни. Именно степень «радикальности», очевидно, влияет на выздоровление пациента, послеоперационное качество жизни и стоимость (эмоциональную и финансовую) для владельца.
В связи с тем, что инъекции, отличные от вакцин, могут вызывать опухоли у кошек, становится разумным искать нехирургические варианты лечения и лечения, чтобы ограничить последствия хирургического вмешательства. В настоящее время медикаментозное лечение FISS имеет ограниченную ценность для отдельного пациента, даже в сочетании с лучевой терапией.
В настоящее время медикаментозное лечение FISS имеет ограниченную ценность для отдельного пациента, даже в сочетании с лучевой терапией.
СНИЖЕНИЕ РИСКА FISS
После более чем 20 лет причинения, диагностики и лечения сарком в месте инъекций у кошек возникает резонный вопрос: что может сделать ветеринар, чтобы снизить риск или ограничить последствия , ФИСС?
Обратите внимание, что следующий краткий обзор рекомендаций появился в литературе и был представлен на национальных конференциях за последние несколько лет; однако рекомендации не всегда подвергались научной проверке и часто представляют собой мнение экспертов, а не результаты опубликованных исследований.
Вакцины вводите только тогда, когда очевиден обоснованный риск воздействия патогенов.
Широко распространено мнение, что ограничение количества вакцин, вводимых человеку с течением времени, может снизить риск развития опухоли. По этой причине ветеринарам настоятельно рекомендуется следовать действующим рекомендациям по вакцинации кошек. 17
17
Взрослым домашним кошкам, прошедшим первую серию вакцинации, базовые вакцины (кошачий парвовирус-герпес-1-калицивирус) следует вводить с интервалом в 3 года. Вакцину против бешенства следует вводить в соответствии с государственными или местными законами и с интервалом, указанным на этикетке продукта. Вводите дополнительные вакцины только кошкам с реальным риском заражения.
Парентеральные вакцины вводите только подкожно.
Внутримышечное введение вакцин не снижает риск FISS. Кроме того, опухоль, развивающаяся в скелетных мышцах (глубокая), может быть обнаружена позже, чем опухоль, развивающаяся в коже (поверхностная).
Вводить вакцины в соответствии с действующими рекомендациями для мест вакцинации.
Необходимо пересмотреть текущие рекомендации для мест вакцинации. Хотя большинство ветеринаров, кажется, следуют рекомендациям, опубликованным VAFSTF в 1996 г. (бешенство, справа сзади; FeLV, слева сзади), FISS по-прежнему диагностируют в межлопаточной области. 9 Кроме того, похоже, что большинство ветеринаров предпочитают вводить вакцины кошкам в места выше коленного сустава, а не ниже и над правым плечом, а не ниже правого локтя, как это рекомендуется в действующих руководствах по вакцинации кошек ( Рисунок ).
9 Кроме того, похоже, что большинство ветеринаров предпочитают вводить вакцины кошкам в места выше коленного сустава, а не ниже и над правым плечом, а не ниже правого локтя, как это рекомендуется в действующих руководствах по вакцинации кошек ( Рисунок ).
Рис. Послеоперационная кошка с FISS в месте вакцинации FeLV. Опухоль развилась в коже над левой стороной таза, указывая на место инъекции высоко на левой стороне. Опухоли, которые развиваются на этом уровне, представляют серьезный риск инвазии в подвздошную кишку, если их не лечить на ранней стадии.
Очевидно, рекомендация вводить вакцины в дистальные отделы конечностей предназначена для облегчения полного удаления опухоли и сведения к минимуму риска местного рецидива после ампутации пораженной конечности.
- Однако опухоли могут развиваться и развиваются одновременно в 2 конечностях у одного и того же пациента.
- Кроме того, постоянное введение вакцины в дистальные отделы конечностей приводит к введению последующих доз вакцины в то же место, что может увеличить риск развития опухоли.

- Также была выражена озабоченность по поводу того факта, что эффективность лицензированных вакцин против бешенства никогда не проверялась у кошек, привитых ниже колена.
Проинформируйте клиентов о том, как сообщать о поствакцинальных шишках.
Чтобы способствовать ранней диагностике FISS, посоветуйте владельцам:
- Наблюдать (прикасаясь или гладя) своих кошек на предмет образования припухлостей в местах инъекций и
- Свяжитесь с врачом, если опухоль увеличивается в размерах или сохраняется более 1 месяца после вакцинации.
Обрабатывайте поствакцинальные шишки в соответствии с правилом 3-2-1 (таблица 2).
При биопсии опухоли в месте инъекции рекомендуется инцизионная, а не эксцизионная биопсия по крайней мере по 2 причинам:
- Простое иссечение небольшой опухоли (люмпэктомия) может затруднить определение исходной локализации в случае диагностированной саркомы, а владелец откладывает окончательное лечение по мере заживления разреза и отрастания волос.

- Большинство поствакцинальных шишек являются доброкачественными. Однако, если предполагается, что опухоль злокачественная, и биопсия не проводится, кошка подвергается ненужной хирургии и удалению чрезмерного количества тканей по поводу поражения, которое рассосется самопроизвольно.
| Если объемное образование соответствует одному или нескольким из следующих критериев, рекомендуется инцизионная (не эксцизионная) биопсия объемного образования. |
| 3: Известно, что масса сохраняется в течение 3 месяцев или дольше. |
| 2: Масса имеет или становится больше 2 см в диаметре. |
| 1: Масса продолжает увеличиваться в размерах через 1 месяц после инъекции. |
Выполните рутинную рентгенографию грудной клетки у кошек с подтвержденным диагнозом FISS.
Высокая частота легочных метастазов у кошек с FISS оправдывает получение рентгенограмм грудной клетки (включая левую и правую боковые проекции) перед назначением пациенту и владельцу окончательного протокола лечения.
По возможности избегайте использования адъювантных (инактивированных) вакцин.
Адъювант представляет собой химический, микробный компонент или белок млекопитающих, обычно добавляемый к инактивированной (убитой) вирусной или бактериальной вакцине для усиления иммунного ответа против выбранного патогена. Известно, что адъюванты вызывают местные реакции, характеризующиеся воспалением, гранулемами и иногда образованием стерильных абсцессов. 18 В настоящее время все инактивированные (убитые) кошачьи вакцины, продаваемые в США и Канаде, содержат адъюванты. Модифицированные живые и рекомбинантные кошачьи вакцины не являются таковыми.
Гипотеза о связи индуцированного адъювантом хронического воспаления с образованием саркомы была предложена несколькими авторами в начале 1990-х годов. 3-5 Споры о роли адъюванта в патогенезе саркомы усилились после публикации ограниченного числа исследований, предполагающих отсутствие существенной разницы в риске FISS, связанном с адъювантными и неадъювантными вакцинами. 10,11,19 Не было опубликовано ни одного исследования, в котором предполагалось бы, что вакцина с адъювантом безопаснее, чем вакцина без адъюванта, в отношении риска FISS.
3-5 Споры о роли адъюванта в патогенезе саркомы усилились после публикации ограниченного числа исследований, предполагающих отсутствие существенной разницы в риске FISS, связанном с адъювантными и неадъювантными вакцинами. 10,11,19 Не было опубликовано ни одного исследования, в котором предполагалось бы, что вакцина с адъювантом безопаснее, чем вакцина без адъюванта, в отношении риска FISS.
Споры вокруг безопасности введения неадъювантных вакцин по сравнению с адъювантными вакцинами, вероятно, продолжатся. В настоящее время просто нет научных данных, подтверждающих однозначные выводы. Следствием этого является то, что у кошек по-прежнему будет диагностироваться FISS, связанный с плановой вакцинацией.
Несмотря на продолжающиеся споры, тот факт, что диагнозы саркомы у кошек стали более распространенными по мере того, как использование адъювантных вакцин стало более распространенным, остается важной и неоспоримой информацией, которая подчеркивает потенциальную роль адъювантов в патогенезе FISS. Рекомендация по возможности избегать введения адъювантной вакцины кошкам оправдана.
Рекомендация по возможности избегать введения адъювантной вакцины кошкам оправдана.
Ссылки
- Sequin B. Саркомы в месте инъекции у кошек. Vet Clin North Am Small Anim Pract 2002; 17(4):168-173.
- Романелли Г., Марконато Л., Оливеро Д. и др. Анализ прогностических факторов, связанных с саркомами в месте инъекции у кошек: 57 случаев (2001-2007 гг.). ЯВМА 2008; 232(8):1193-1199.
- Хендрик М.Дж., Гольдшмидт М.Х. Вызывают ли реакции в месте инъекции фибросаркомы у кошек? ЯВМА 1991; 199(8):968.
- Hendrick MJ, Goldschmidt MH, Shofer FS, et al. Поствакцинальные саркомы у кошек: эпидемиологическая и электронно-зондовая микроаналитическая идентификация алюминия. Рак Res 1992; 52(19):5391-5394.
- Хендрик М.Дж., Брукс Дж.Дж. Поствакцинальные саркомы у кошек: гистология и иммуногистохимия. Вет Патол 1994; 31(1):126-129.
- Kass PH, Barnes WG Jr, Spangler WL, et al.
 Эпидемиологические доказательства причинно-следственной связи между вакцинацией и онкогенезом фибросаркомы у кошек. ЯВМА 1993; 203(3):396-405.
Эпидемиологические доказательства причинно-следственной связи между вакцинацией и онкогенезом фибросаркомы у кошек. ЯВМА 1993; 203(3):396-405. - Гаскелл Р., Геттинби Г., Грэм, Скилтон Д. Рабочая группа Комитета по ветеринарным препаратам (VPC) по вакцинации кошек и собак. Департамент окружающей среды, продовольствия и сельского хозяйства, Лондон, май 2001 г.
- Целевая группа по вакциноассоциированной саркоме кошек: обсуждение за круглым столом. Современное понимание и лечение вакциноассоциированных сарком у кошек. ЯВМА 2009; 234(3):376-378.
- Shaw SC, Kent MS, Gordon IK, et al. Временные изменения характеристик сарком в месте инъекции у кошек: 392 случая (1990–2006 годы). ЯВМА 2009; 234:376-380.
- Шривастав А., Касс П.Х., Макгилл Л.Д. и др. Сравнительный риск саркомы в месте инъекции у кошек, связанный с вакциной и другими инъекционными препаратами. ЯВМА 2012; 241(5):595-602.
- Kass PH, Spangler WL, Hendrick MJ, et al.
 Многоцентровое исследование «случай-контроль» факторов риска, связанных с развитием вакциноассоциированных сарком у кошек. ЯВМА 2003; 223:1283-1292.
Многоцентровое исследование «случай-контроль» факторов риска, связанных с развитием вакциноассоциированных сарком у кошек. ЯВМА 2003; 223:1283-1292. - Kass PH, Barnes WG Jr, Spangler WL, et al. Эпидемиологические доказательства причинно-следственной связи между вакцинацией и онкогенезом фибросаркомы у кошек. ЯВМА 1993; 203:396-405.
- Хендрик М. Исторический обзор и современные знания о факторах риска, связанных с вакциноассоциированными саркомами кошек. ЯВМА 1998; 213:1422-1423.
- Лестер С., Клеметт Т., Берт А. Саркомы, связанные с местом вакцинации у кошек: клинический опыт и лабораторный обзор (1982-1993). ДЖААХА 1996; 32:91-95.
- Мэйси Д., Хендрик М. Потенциальная роль воспаления в развитии поствакцинальных сарком у кошек. Vet Clin North Am Small Anim Pract 1996; 26:103-109.
- Gobar G, Kass P. Обзор практики вакцинации, поствакцинальных реакций и сарком, связанных с местами вакцинации у кошек, основанный на World Wide Web.
 ЯВМА 2002; 220:1477-1482.
ЯВМА 2002; 220:1477-1482. - Ричардс Дж. Р., Элстон Т. Х., Форд Р. Б. и др. Отчет Консультативной группы по вакцинам против кошек Американской ассоциации практикующих врачей-фелинологов за 2006 год. ЯВМА 2006; 229(9):1405-1441.
- Спиклер А.Р., Рот Дж.А. Адъюванты в ветеринарных вакцинах: механизмы действия и побочные эффекты. J Vet Intern Med 2003; 17(3):273-281.
- Уилкок Б., Уилкок А., Боттомс К. Поствакцинальная саркома кошек: 20 лет спустя. Can Vet J 2012; 53:430-434.
Хризотерапия у кошек — лечение, процедура, эффективность, восстановление, стоимость, соображения, профилактика
Что такое хризотерапия?
Хризотерапия, также известная как терапия золотом, заключается во введении пациенту солей золота путем глубокой внутримышечной инъекции. Это малоиспользуемый метод лечения со скудными данными, чтобы подтвердить доказательства того, работает он или нет. Хризотерапия в основном является последним средством для кошек, которые не реагируют на более традиционные методы лечения, и эвтаназия может быть единственным выходом.
Это малоиспользуемый метод лечения со скудными данными, чтобы подтвердить доказательства того, работает он или нет. Хризотерапия в основном является последним средством для кошек, которые не реагируют на более традиционные методы лечения, и эвтаназия может быть единственным выходом.
Лечение включает в себя глубокую внутримышечную инъекцию солей золота один раз в неделю, и это можно сделать по первому заключению.
Процедура хризотерапии у кошек
Сначала необходимо установить окончательный диагноз пузырчатки. Обычно это делается при биопсии пораженных участков, чтобы подтвердить, что это иммуноопосредованное заболевание, а не рак или тяжелая инфекция.
Сначала предпринимаются попытки традиционного лечения, но если это не помогает, можно рассмотреть другие варианты, такие как хризотерапия. Это предполагает еженедельные внутримышечные инъекции солей золота. Миохризин производства Merck содержит ауротиомалат натрия. Доза составляет 1 мг/кг/неделю в течение 8-12 недель. Для того, чтобы заметить какое-либо улучшение, может потребоваться до 10 недель. Поэтому хризотерапию обычно начинают параллельно со стероидами, чтобы восполнить этот пробел. Однако, если к 12 нед улучшения не наблюдается, дозу солей золота можно удвоить. Терапия продолжается около 20 недель, но в случае неудачи на этом этапе ее следует прекратить.
Это предполагает еженедельные внутримышечные инъекции солей золота. Миохризин производства Merck содержит ауротиомалат натрия. Доза составляет 1 мг/кг/неделю в течение 8-12 недель. Для того, чтобы заметить какое-либо улучшение, может потребоваться до 10 недель. Поэтому хризотерапию обычно начинают параллельно со стероидами, чтобы восполнить этот пробел. Однако, если к 12 нед улучшения не наблюдается, дозу солей золота можно удвоить. Терапия продолжается около 20 недель, но в случае неудачи на этом этапе ее следует прекратить.
При эффективности хризотерапии частоту инъекций постепенно снижают. Цель состоит в том, чтобы стабилизировать состояние пациента с помощью одной инъекции каждые 2–8 недель.
Также доступны пероральные соли золота (Auranofin, SmithKline Beecham), но они менее эффективны, чем инъекционные формы.
Top
Эффективность хризотерапии у кошек
Данные об эффективности хризотерапии ограничены. Скорее всего, он будет использоваться в качестве спасательной терапии для кошек, где эвтаназия является другим вариантом из-за нечувствительности к стероидам или другим иммунодепрессантам.
Для кошек, которые реагируют, дозу стероидов, используемых в переходный период, постепенно снижают с целью полного прекращения. Кошки, которые чувствуют себя хорошо, часто получают один раз в месяц инъекцию соли золота.
Top
Хризотерапия Восстановление у кошек
Побочные эффекты возникают редко (см. : Рекомендации). Инъекцию делают находящейся в сознании кошке, поэтому, если не считать стресса от поездки в ветеринарную клинику, время восстановления незначительно. Однако глубокие внутримышечные инъекции могут быть болезненными, поэтому со временем некоторые кошки могут стать менее терпимыми к терапии.
: Рекомендации). Инъекцию делают находящейся в сознании кошке, поэтому, если не считать стресса от поездки в ветеринарную клинику, время восстановления незначительно. Однако глубокие внутримышечные инъекции могут быть болезненными, поэтому со временем некоторые кошки могут стать менее терпимыми к терапии.
Верх
Стоимость хризотерапии у кошек
Флакон миохризина стоит около 120 долларов США по себестоимости, и ваш ветеринар сделает надбавку к этой цене. За глубокую внутримышечную инъекцию также взимается плата, которая может составлять около 40 долларов. Таким образом, прогнозируемая цена каждой еженедельной инъекции, как ожидается, составит около 60 долларов.
К этому добавляется стоимость скрининга крови (от 40 до 120 долларов) и анализа мочи (от 12 до 60 долларов в зависимости от используемого теста). Имейте в виду, что изначально это еженедельно.
Имейте в виду, что изначально это еженедельно.
Вверх
Беспокоитесь о стоимости лечения хризотерапией?
Страхование домашних животных покрывает расходы на лечение многих распространенных заболеваний домашних животных. Подготовьтесь к неожиданностям, получив предложение от лучших поставщиков страховых услуг для домашних животных.
Узнать цену
Хризотерапия для кошек
Хризотерапия не является «волшебным средством», и даже для кошек, которые реагируют, это может занять несколько недель или месяцев. Владелец, рассматривающий хризотерапию для своей кошки, должен признать, что нет гарантированного результата и что традиционные методы лечения, такие как стероиды, могут потребоваться параллельно в течение переходного периода.
Хотя побочные эффекты возникают редко, они могут быть значительными. Они включают подавление продукции тромбоцитов, почечную недостаточность, образование стерильного абсцесса в месте инъекции и токсический эпидермальный некролиз (отмирание кожи).
Клиницист будет следить за побочными эффектами у кошки, сначала проводя анализы крови и мочи каждые две-три недели, а затем, как только кошка стабилизируется, проводит их два-три раза в год.
Top
Профилактика хризотерапии у кошек
Пузырчатка вызывается неадекватной реакцией иммунной системы на собственные ткани. У некоторых кошек это может быть связано с генетической предрасположенностью к пузырчатке. В других случаях триггером может быть воздействие ультрафиолета, а также некоторые лекарства.
У некоторых кошек это может быть связано с генетической предрасположенностью к пузырчатке. В других случаях триггером может быть воздействие ультрафиолета, а также некоторые лекарства.
Лекарства, вызывающие пузырчатку, включают метимазол, амоксициллин, итраконазол, сульфаниламиды и растворы серной извести, хотя следует отметить, что такие побочные эффекты возникают крайне редко.
Верх
Обработка и техника | Ключ ветерана
Методы введения
Инъекции и образцы крови следует выполнять с использованием асептических методов. Для каждого животного следует использовать новые стерильные иглы, а перед введением может потребоваться обработка места инъекции антисептическим раствором. Это особенно важно при внутривенном введении. Важно использовать оборудование, подходящее для данного вида (см. Таблицу 7.2), и использовать иглу наименьшего размера. Это определяется размерами животного и вязкостью вещества, так как густые вязкие жидкости могут не пройти через узкоколейные иглы.
Таблицу 7.2), и использовать иглу наименьшего размера. Это определяется размерами животного и вязкостью вещества, так как густые вязкие жидкости могут не пройти через узкоколейные иглы.
Таблица 7.2 (a) Рекомендуемые размеры игл для подкожных инъекций для лабораторных животных*. (b) Рекомендуемые размеры канюль для лабораторных животных.
Подкожные инъекции
Большинству видов можно делать подкожные инъекции в загривок (рис. 7.1). Складку кожи приподнимают большим и первыми двумя пальцами одной руки, и иглу проводят через кожу в основании складки параллельно телу, чтобы избежать проникновения в более глубокие ткани. Подкожные инъекции редко бывают болезненными, если инъецируемое вещество не вызывает жжения.
РИСУНОК 7.1 Подкожная инъекция мыши. Фото: Джеймс и Стив.
Некоторым животным можно также делать подкожные инъекции в бок. Животное фиксируют, как при внутрибрюшинной инъекции, и иглу вводят под кожу посередине бока (рис. 7.2). Это место иногда используется для инъекции опухолевых клеток, поскольку в этом месте можно легко оценить растущую опухоль, или для выработки антител у кроликов.
РИСУНОК 7.2 Подкожная инъекция в бок. Фото: Джеймс и Стив.
Крупным животным жидкость можно вводить под кожу над ребрами. Свиньям можно вводить небольшие объемы в кожу за ухом или в складку между ногой и животом. У свиней много подкожного жира, и инъекции, сделанные в другом месте, скорее всего, попадут в жир, где всасывание, вероятно, будет медленным.
Внутримышечные инъекции
Внутримышечные инъекции часто болезненны из-за растяжения мышечных волокон, и по возможности следует использовать альтернативный путь введения. В противном случае требуется хорошая фиксация или анестезия. Мелким животным их обычно вводят в мышцы бедра, а большие объемы следует вводить в группу четырехглавой мышцы передней поверхности бедра2. Мышца может быть иммобилизована одной рукой, а инъекция — другой. У крыс четырехглавую мышцу можно пропальпировать на передней поверхности бедра и зафиксировать большим и указательным пальцами одной руки, в то время как инъекцию делают другой (рис. 7.3). Инъекции можно делать в каудальные мышцы бедра, но, поскольку седалищный нерв проходит через эти мышцы, здесь следует соблюдать осторожность, иначе может быть поврежден нерв. Риск можно свести к минимуму, введя иглу в мышечную массу с латеральной стороны и наклонив острие каудально.
7.3). Инъекции можно делать в каудальные мышцы бедра, но, поскольку седалищный нерв проходит через эти мышцы, здесь следует соблюдать осторожность, иначе может быть поврежден нерв. Риск можно свести к минимуму, введя иглу в мышечную массу с латеральной стороны и наклонив острие каудально.
РИСУНОК 7.3 Внутримышечная инъекция (квадрицепс).
У мышей, поскольку мышечная масса очень мала, требуется маленькая игла (29 или 30 G), и можно вводить только небольшой объем. Инъекции также можно делать в переднюю большеберцовую мышцу на переднебоковой стороне нижней задней конечности. Мышь держат на спине с вытянутой вперед ногой. Важно, чтобы бугристость большеберцовой кости, гребень на передней части ноги, была вертикальной. Иглу вводят под углом 45° примерно на 3 мм латеральнее бугристости, параллельно линии ножки. Иглу вводят на глубину 2–3 мм. Можно вводить до 50 мкл5.
Собак, кошек, хорьков и кроликов можно с осторожностью вводить в мышцы по обе стороны от позвоночника, а у крупных животных используются ягодичные мышцы над крупом. У взрослых свиней уколы делают в мышцы шеи, но для проникновения в жировой слой требуется длинная игла. Поросятам можно вводить инъекцию, поднимая их за одну заднюю ногу и вводя инъекцию в каудальную мышцу бедра на этой стороне. Птицам делают внутримышечные инъекции в грудные мышцы. После инъекции следует помассировать место инъекции, чтобы разогнать дозу.
У взрослых свиней уколы делают в мышцы шеи, но для проникновения в жировой слой требуется длинная игла. Поросятам можно вводить инъекцию, поднимая их за одну заднюю ногу и вводя инъекцию в каудальную мышцу бедра на этой стороне. Птицам делают внутримышечные инъекции в грудные мышцы. После инъекции следует помассировать место инъекции, чтобы разогнать дозу.
Внутривенная инъекция
Крысам и мышам внутривенные инъекции обычно делают в боковые хвостовые вены (рис. 7.4а). Инъекцию облегчают, согревая животное в боксе при 37°С или помещая перед инъекцией хвост в теплую воду. Может потребоваться местная или общая анестезия. Животное должно быть закреплено помощником или помещено в удерживающее устройство, а вена может быть поднята путем осторожного закупоривания ее у основания хвоста. Игла должна быть выровнена параллельно вене и направлена к телу срезом вверх, прежде чем осторожно ввести ее в вену. Не должно быть сопротивления инъекции. Этот метод можно увидеть на сайте www. procedureswithcare.org.uk. Мелким животным инъекции можно делать и в подкожную вену (рис. 7.4b). Задняя конечность вытянута, а вена приподнята за счет пережатия ее в коленном суставе. Это особенно полезно для бесхвостых грызунов.
procedureswithcare.org.uk. Мелким животным инъекции можно делать и в подкожную вену (рис. 7.4b). Задняя конечность вытянута, а вена приподнята за счет пережатия ее в коленном суставе. Это особенно полезно для бесхвостых грызунов.
РИСУНОК 7.4 (a) Инъекция в хвостовую вену грызуна. (б) Подкожная вена. Фотографии: (а) MRC Harwell; (b) AstraZeneca, используется с разрешения.
У собак, кошек, приматов и хорьков можно использовать головную вену на передней поверхности передней конечности. Вену поднимают, помещая первые два пальца одной руки за локоть и надавливая большим пальцем чуть ниже передней поверхности локтя: у хорьков для этой цели лучше всего использовать жгут, так как конечности короткие (см. рис. 7.5). ). Яремную вену можно использовать у собак, кошек, хомяков и хорьков (см. рис. 7.6), и это метод выбора у жвачных животных и лошадей. Ушные вены используются у морских свинок и свиней. Птице можно вводить через плечевую вену.
РИСУНОК 7.5 (a) Быстросъемный жгут. (b) Быстросъемный жгут, используемый для венепункции головного мозга у макаки.
(b) Быстросъемный жгут, используемый для венепункции головного мозга у макаки.
РИСУНОК 7.6 Яремная венепункция у хорька. Обратите внимание, что игла была согнута под углом к концентратору, чтобы облегчить расположение в вене.
Если жидкости вводятся путем инфузии, скорость потока должна быть как можно ниже, а инфузия должна осуществляться как можно быстрее. В противном случае, если слишком быстро будет введено слишком много жидкости, кровообращение может стать перегруженным, что приведет к отеку легких. Поддерживающая потребность в жидкости составляет примерно 50–60 мл/кг в сутки у нормальных млекопитающих, и следует соблюдать осторожность, чтобы не превышать эту норму, если нет дефицита, который необходимо устранить.
Внутрикожные инъекции
Внутрикожные инъекции для большинства видов можно делать в ту же область, что и подкожные инъекции. Однако дерма большинства лабораторных животных очень тонкая, и внутрикожное введение может потребовать очень осторожного введения иглы под анестезией или седацией. Участок следует подстричь, чтобы удалить мех, и протереть антисептическим раствором, чтобы облегчить визуализацию места инъекции. Игла должна быть введена скошенным верхом на небольшое расстояние в кожу и сделана инъекция. Будет сопротивление к инъекции, и успешное введение должно привести к поднятию пузыря. Объем, который можно ввести в этот участок, невелик.
Участок следует подстричь, чтобы удалить мех, и протереть антисептическим раствором, чтобы облегчить визуализацию места инъекции. Игла должна быть введена скошенным верхом на небольшое расстояние в кожу и сделана инъекция. Будет сопротивление к инъекции, и успешное введение должно привести к поднятию пузыря. Объем, который можно ввести в этот участок, невелик.
Инъекции в подушечку лапы и основание хвоста
В подушечку лапы обычно делают инъекции для изучения иммунологических явлений у грызунов. Инъекция в подушечку лапы представляет собой комбинацию внутрикожной и подкожной инъекции. После инъекции возникает реакция гиперчувствительности замедленного типа, которую можно использовать для измерения иммунных ответов in vivo. Отток лимфы от инъекций в подушечки стопы идет сначала в подколенный лимфатический узел6, а затем в медиальный подвздошный7 и паховый узлы8. Лимфоциты могут быть собраны из этих узлов для исследования in vitro. Этот метод введения также используется в анализе подколенных лимфатических узлов, чтобы различать иммуностимулирующие и инертные химические вещества9. , 10. Иммунизация подушечки лапы с последующей ревакцинацией у основания хвоста также является широко используемым протоколом для производства антител или для индукции артрита. Однако инъекция в подушечку лапы приводит к отеку и боли и может ухудшить подвижность. Более гуманной альтернативой этому методу является иммунизация животных в латеральной области предплюсны чуть выше лодыжки. Иммунный ответ из этого места направлен на те же дренирующие лимфатические узлы с аналогичным ответом, но с минимальным влиянием на подвижность11. После инъекций в подушечки лап животным необходимо давать мягкую подстилку, а также можно давать пищу и воду в виде геля, размещенного на полу клетки, чтобы им не приходилось ходить. Социальных животных следует содержать группами, но с низкой плотностью посадки, чтобы им не приходилось перелезать друг через друга, чтобы добраться до еды или воды.
, 10. Иммунизация подушечки лапы с последующей ревакцинацией у основания хвоста также является широко используемым протоколом для производства антител или для индукции артрита. Однако инъекция в подушечку лапы приводит к отеку и боли и может ухудшить подвижность. Более гуманной альтернативой этому методу является иммунизация животных в латеральной области предплюсны чуть выше лодыжки. Иммунный ответ из этого места направлен на те же дренирующие лимфатические узлы с аналогичным ответом, но с минимальным влиянием на подвижность11. После инъекций в подушечки лап животным необходимо давать мягкую подстилку, а также можно давать пищу и воду в виде геля, размещенного на полу клетки, чтобы им не приходилось ходить. Социальных животных следует содержать группами, но с низкой плотностью посадки, чтобы им не приходилось перелезать друг через друга, чтобы добраться до еды или воды.
Внутрибрюшинные инъекции
Внутрибрюшинные инъекции грызунам можно вводить в каудальный левый или правый квадрант брюшной полости, чтобы избежать попадания в жизненно важные органы. Квадранты разграничиваются средней линией и перпендикулярной ей линией, проходящей через пупок. У мышей можно использовать оба квадранта, хотя у крыс правый квадрант животного может быть предпочтительнее, поскольку слепая кишка большего размера может занимать левый квадрант. Животное должен держать либо помощник, либо в одной руке за спину, в вертикальном положении, чтобы оно было удобно и надежно поддерживалось. Игла вводится в центр одного из квадрантов под углом к середине спинки. Иглу вводят на несколько миллиметров, достаточно, чтобы проникнуть в стенку тела, и делают инъекцию. Сопротивление инъекции отсутствует (рис. 7.7).
Квадранты разграничиваются средней линией и перпендикулярной ей линией, проходящей через пупок. У мышей можно использовать оба квадранта, хотя у крыс правый квадрант животного может быть предпочтительнее, поскольку слепая кишка большего размера может занимать левый квадрант. Животное должен держать либо помощник, либо в одной руке за спину, в вертикальном положении, чтобы оно было удобно и надежно поддерживалось. Игла вводится в центр одного из квадрантов под углом к середине спинки. Иглу вводят на несколько миллиметров, достаточно, чтобы проникнуть в стенку тела, и делают инъекцию. Сопротивление инъекции отсутствует (рис. 7.7).
РИСУНОК 7.7 Внутрибрюшинная инъекция. Фото: Джеймс и Стив.
Трансдермальное введение
Некоторые соединения могут вводиться в эпидермис путем чрескожного введения. Частицы могут быть нанесены на частицы золота или жидкости, соединенные с системами доставки лекарств, и прострелены через кожу с помощью газовой пушки. Это часто используется для вакцинации голой ДНК в иммунологических исследованиях. Преимущества этого метода заключаются в том, что он безболезненный, а хорошие иммунологические ответы можно получить с помощью небольшого количества ДНК. Однако для этого требуется специальное оборудование, а также специальная подготовка и хранение соединения5. В зависимости от вида и места введения может потребоваться легкая анестезия или седация для подготовки места и/или введения исследуемого материала. Животным с густым мехом, таким как грызуны и кролики, следует подстричь и выбрить место введения, чтобы удалить как можно больше шерсти. Устройство или систему доставки следует располагать так, чтобы они находились в тесном контакте с кожей, обычно перпендикулярно поверхности кожи. После доставки участок можно контролировать на наличие кожных реакций, включая эритему и отек.
Преимущества этого метода заключаются в том, что он безболезненный, а хорошие иммунологические ответы можно получить с помощью небольшого количества ДНК. Однако для этого требуется специальное оборудование, а также специальная подготовка и хранение соединения5. В зависимости от вида и места введения может потребоваться легкая анестезия или седация для подготовки места и/или введения исследуемого материала. Животным с густым мехом, таким как грызуны и кролики, следует подстричь и выбрить место введения, чтобы удалить как можно больше шерсти. Устройство или систему доставки следует располагать так, чтобы они находились в тесном контакте с кожей, обычно перпендикулярно поверхности кожи. После доставки участок можно контролировать на наличие кожных реакций, включая эритему и отек.
Пероральное введение
Вещества можно вводить перорально путем включения в рацион или питья воды. У них есть недостатки, заключающиеся в том, что либо вся группа должна подвергаться дозированию, либо животные должны содержаться по отдельности. Также невозможно быть уверенным, что животное получило всю дозу, и некоторые животные могут отказаться от еды и питья, если корм или вода содержат лекарство. В частности, у мышей добавление лекарств в воду может привести к обезвоживанию, поскольку отказ мыши от питья может привести к быстрому ухудшению состояния животного. При кормлении ad libitum или при увеличении скорости метаболизма животное может переесть и, таким образом, проглотить передозировку препарата. Если система полива автоматизирована, подавать соединения таким способом нельзя. Для преодоления этих проблем можно использовать интубацию желудка или желудочный зонд (рис. 7.8). Используются гибкие катетеры или иглы из нержавеющей стали с закругленными концами. Жесткие иглы могут быть прямыми или изогнутыми. Игла или катетер должны быть сначала измерены относительно животного и отмечены на длине, которая достигает мечевидного отростка. Животное фиксируют с вытянутой шеей, и иглу или катетер проводят по средней линии в верхней части рта и по задней части языка осторожно вниз по пищеводу до тех пор, пока не будет достигнута отметка на катетере.
Также невозможно быть уверенным, что животное получило всю дозу, и некоторые животные могут отказаться от еды и питья, если корм или вода содержат лекарство. В частности, у мышей добавление лекарств в воду может привести к обезвоживанию, поскольку отказ мыши от питья может привести к быстрому ухудшению состояния животного. При кормлении ad libitum или при увеличении скорости метаболизма животное может переесть и, таким образом, проглотить передозировку препарата. Если система полива автоматизирована, подавать соединения таким способом нельзя. Для преодоления этих проблем можно использовать интубацию желудка или желудочный зонд (рис. 7.8). Используются гибкие катетеры или иглы из нержавеющей стали с закругленными концами. Жесткие иглы могут быть прямыми или изогнутыми. Игла или катетер должны быть сначала измерены относительно животного и отмечены на длине, которая достигает мечевидного отростка. Животное фиксируют с вытянутой шеей, и иглу или катетер проводят по средней линии в верхней части рта и по задней части языка осторожно вниз по пищеводу до тех пор, пока не будет достигнута отметка на катетере. Необходимо соблюдать осторожность, чтобы не повредить пищевод и не ввести иглу в трахею. Должно быть минимальное сопротивление при прохождении катетера по пищеводу, хотя может быть некоторое сопротивление при прохождении катетера через сфинктер в желудок. Обычно можно наблюдать, как игла или катетер проходят по пищеводу на левой стороне шеи. Повреждения катетера при жевании можно избежать, используя оральное зеркало или используя вместо него гибкую назогастральную или фарингостомическую трубку.
Необходимо соблюдать осторожность, чтобы не повредить пищевод и не ввести иглу в трахею. Должно быть минимальное сопротивление при прохождении катетера по пищеводу, хотя может быть некоторое сопротивление при прохождении катетера через сфинктер в желудок. Обычно можно наблюдать, как игла или катетер проходят по пищеводу на левой стороне шеи. Повреждения катетера при жевании можно избежать, используя оральное зеркало или используя вместо него гибкую назогастральную или фарингостомическую трубку.
РИСУНОК 7.8 Зонд у мыши. Фото: Джеймс и Стив.
Для более крупных животных, таких как собаки и кошки, таблетки можно вводить перорально находящемуся в сознании животному, положив одну руку на макушку, поместив большой палец на спайку губ с одной стороны, а остальные пальцы — на другую , и наклон головы назад. Это заставит рот слегка приоткрыться. Таблетку можно держать между большим и указательным пальцами другой руки, а средним пальцем открывать рот. Затем таблетку можно поместить на язык как можно дальше назад, чтобы стимулировать глотательный рефлекс. Облегчить это можно, удерживая пасть животного закрытой, запрокидывая голову назад и массируя горло.
Облегчить это можно, удерживая пасть животного закрытой, запрокидывая голову назад и массируя горло.
Юридические аспекты12,13
Ветеринарные правила Великобритании регулируют введение ветеринарных препаратов животным. Эти правила ежегодно пересматриваются и поэтому незначительно меняются из года в год. Положение о ветеринарных лекарственных средствах 2011 года вступило в силу 1 октября того же года. Правила запрещают поставку лекарств для животных без соответствующего разрешения на продажу, за исключением особых обстоятельств. Регистрационные удостоверения обычно не распространяются на лабораторные виды; поэтому лекарства, используемые для лечения этих видов, обычно назначаются в порядке исключения. Поставка лекарств для лабораторных животных в первую очередь является обязанностью назначенного ветеринарного врача, и исследователям обычно приходится получать и использовать эти лекарства под руководством ветеринарного врача. Фармацевт может поставлять лицензированные лекарства для животных только по указанию или рецепту ветеринарного врача. Медицинские работники не могут на законных основаниях прописывать лекарства для животных. Поставка просроченных лекарств является правонарушением.
Медицинские работники не могут на законных основаниях прописывать лекарства для животных. Поставка просроченных лекарств является правонарушением.
Правила подразделяют ветеринарную медицину на следующие категории.
- Ветеринарные лекарства, отпускаемые только по рецепту (POM-V): эти препараты могут поставляться или назначаться только ветеринарным врачом после клинической оценки животного или группы животных под наблюдением ветеринарного врача.
- Лекарства, отпускаемые только по рецепту – ветеринар, фармацевт, лицо с соответствующей квалификацией (POM-VPS): их может выписать любое зарегистрированное квалифицированное лицо (RQP; ветеринар, фармацевт или лицо с соответствующей квалификацией, или SQP). Клиническая оценка животного не требуется, но необходимо знать достаточную информацию о животном для надлежащего назначения.
- Непищевые животные – ветеринар, фармацевт, лицо с соответствующей квалификацией (NFA-VPS): они могут быть предоставлены RQP, как указано выше, при условии соблюдения требований к поставке.
 Эти лекарства не требуют рецепта.
Эти лекарства не требуют рецепта. - Авторизованный список ветеринарных препаратов – Общий список продаж (AVM-GSL): законодательных ограничений на розничную поставку ветеринарных препаратов этой категории нет, но ожидается ответственный подход к поставкам.
Некоторые наркотики также контролируются в соответствии с Положением Великобритании о злоупотреблении наркотиками 200114. Эти правила устанавливают дополнительный контроль над поставкой и использованием наркотиков, которые потенциально вызывают привыкание или опасны. Лекарства классифицируются в соответствии с пятью списками, каждый из которых имеет различные требования к поставке, хранению и ведению учета. Ветеринарные препараты, являющиеся контролируемыми препаратами, включены в списки 2, 3 или 4. Примеры контролируемых препаратов списка 2 включают морфин и фентанил. Эти препараты должны храниться в запираемом шкафу, а их приобретение и индивидуальное использование должны регистрироваться. Препараты Списка 3 включают бупренорфин. Они должны храниться в запираемом шкафу, но отдельные приемы не должны записываться. Препараты Списка 4 включают кетамин и многие бензодиазепины, и они должны храниться в надежном месте, а их приобретение должно регистрироваться. Существуют строгие требования к форме реестров контролируемых наркотиков. Подробности см. в ссылке 14.
Они должны храниться в запираемом шкафу, но отдельные приемы не должны записываться. Препараты Списка 4 включают кетамин и многие бензодиазепины, и они должны храниться в надежном месте, а их приобретение должно регистрироваться. Существуют строгие требования к форме реестров контролируемых наркотиков. Подробности см. в ссылке 14.
Хранение и ведение учета
Все лекарства должны храниться надлежащим образом, чтобы обеспечить сохранение их полной активности. Некоторые нужно хранить в холодильнике при температуре 2–5°C, некоторые нужно хранить вдали от света, некоторые нельзя хранить в пластиковых бутылках. В паспорте, поставляемом с препаратом, будут указаны требования. Хорошей практикой является ведение учета всех хранящихся и используемых наркотиков, а также закон требует вести учет покупки и использования всех контролируемых наркотиков, перечисленных в Списках 1–3 Положений о злоупотреблении наркотиками 2001 г. 14. Рекомендуется проводить ежегодную проверку шкафа для хранения лекарств и утилизировать просроченные лекарства в соответствии с требованиями законодательства.
Удаление крови
Удаление крови у животного может причинить боль, страдание, дистресс или долговременный вред. Возможные побочные эффекты перечислены ниже.
- Стресс от обращения и удержания: необходимо использовать гуманные методы обращения и ограничения (см. разделы о видах), а также могут потребоваться седативные или анестезирующие средства. Также может быть полезным обучение животных приемам обращения с образцами крови.
- Боль и дискомфорт: венепункция требует значительных навыков и при некомпетентном выполнении может привести к кровотечению, синяку, тромбозу, эмболии или флебиту. Кроме того, неправильная техника отбора проб может привести к образованию тромбов или гемолизу пробы, что сделает результаты недействительными.
- Гиповолемия: эффекты удаления крови зависят от объема удаляемой крови и скорости ее отведения. Быстрое удаление большого количества крови может вызвать у животного гиповолемический шок и даже смерть.
 Процент кровопотери, необходимый для возникновения гиповолемического шока, зависит от скорости абстиненции, от того, восполняется ли жидкость одновременно, и от физиологического состояния животного в это время. Хроническое медленное кровотечение переносится лучше, чем острая кровопотеря, а спокойные животные переносят большие потери, чем нервные, что еще раз подтверждает необходимость грамотного обращения и дрессировки животных.
Процент кровопотери, необходимый для возникновения гиповолемического шока, зависит от скорости абстиненции, от того, восполняется ли жидкость одновременно, и от физиологического состояния животного в это время. Хроническое медленное кровотечение переносится лучше, чем острая кровопотеря, а спокойные животные переносят большие потери, чем нервные, что еще раз подтверждает необходимость грамотного обращения и дрессировки животных.
Стрессовые реакции у животных приводят к высвобождению гормонов и других веществ для противодействия стрессу, что может привести к аномальным результатам экспериментов. Опыт необходимо приобретать, сначала наблюдая за другими, затем практикуя на трупах или моделях, а затем выполняя технику под непосредственным наблюдением. Методика эксперимента должна быть усовершенствована таким образом, чтобы количество удаляемой крови было минимальным. Это особенно важно для мелких млекопитающих, таких как мыши, у которых объем крови невелик, а объем образца имеет решающее значение. Крайне важно следовать руководящим принципам передовой практики, таким как BVA/FRAME/RSPCA/UFAW (1993) отчет рабочей группы по изъятию крови у лабораторных млекопитающих и птиц15.
Крайне важно следовать руководящим принципам передовой практики, таким как BVA/FRAME/RSPCA/UFAW (1993) отчет рабочей группы по изъятию крови у лабораторных млекопитающих и птиц15.
Качество образцов
Для получения значимых результатов образцы должны быть хорошего качества и храниться наилучшим образом. Образцы должны быть взяты умело, а затем должным образом обработаны. Кровь можно собирать с помощью шприцев и игл для подкожных инъекций или игл-бабочки, через постоянные канюли, с помощью двусторонних игл и вакуумных трубок (например, Vacutainers, Becton Dickinson) или у очень мелких видов путем осторожного разреза вены с помощью стерильного ланцета или лезвия скальпеля. и сбор образца капиллярной трубкой. Если используются иглы, игла должна быть настолько большой, насколько это практически возможно для данного вида. Это позволяет крови течь быстрее, снижая вероятность свертывания крови, а также вызывает меньшее повреждение эритроцитов, снижая вероятность гемолиза.
Если антикоагулянт не используется, кровь свернется, и сыворотку можно будет удалить после центрифугирования. В качестве альтернативы кровь может быть собрана в антикоагулянт. Доступны различные антикоагулянты, в том числе следующие.
В качестве альтернативы кровь может быть собрана в антикоагулянт. Доступны различные антикоагулянты, в том числе следующие.
- Литий-гепарин: это антикоагулянт выбора для большинства биохимических анализов. Выход плазмы из гепаринизированной крови выше, чем выход сыворотки из свернувшейся крови, что может сделать гепарин хорошим выбором для сбора крови для сбора антител. Гепарин натрия иногда используется, если требуется сохранение лейкоцитов.
- Калийэтилендиаминтетрауксусная кислота (ЭДТА): используется для гематологических анализов, так как сохраняет клетки.
- Оксалат/фторид: используется для определения уровня глюкозы в крови.
Доступны несколько других антикоагулянтов, например, для сбора крови для переливания или анализа факторов свертывания крови. После сбора в антикоагулянт кровь следует тщательно перемешать перекатыванием, а не встряхиванием, так как это может повредить клетки и привести к гемолизу.
Предпочтительно, чтобы образцы представлялись свежими для анализа. Если это невозможно, может потребоваться охлаждение образцов или глубокая заморозка после отделения клеток и плазмы или сыворотки. Целесообразно определить точные требования лабораторного протокола до взятия образца.
Если это невозможно, может потребоваться охлаждение образцов или глубокая заморозка после отделения клеток и плазмы или сыворотки. Целесообразно определить точные требования лабораторного протокола до взятия образца.
Техника венепункции
Место и расположение вены
Важно точно определить местонахождение вены, визуализируя ее или прощупывая ее ход, и обеспечить ее иммобилизацию перед прокалыванием кожи. Если вы не уверены в положении вены, не следует пытаться делать венепункцию. Иногда необходимо приподнять вену, перекрывая венозный отток проксимальнее места венепункции. Это должно быть выполнено правильно, иначе изъятие крови будет затруднено. Использование быстросъемного жгута (рис. 7.5а) облегчает забор крови у некоторых видов, а у других можно использовать сосудорасширяющие средства. Согревание животного в термостатируемом горячем боксе в течение 30 минут при температуре 37°C или погружение хвоста в теплую воду может способствовать расширению хвостовых вен у мелких грызунов, облегчая венепункцию.
Подготовка места
Кровь следует собирать в асептических условиях. Участок следует подстричь, чтобы удалить волосы, если это необходимо, а затем очистить с помощью подходящего антибактериального моющего средства, такого как хлоргексидин. Также можно использовать препараты на основе йода, но они менее стойкие. Использование теплой воды с дезинфицирующим средством или без него поможет расширить поверхностные вены, а также очистить кожу. После очистки кожу можно протереть 70% этанолом или дезинфицирующим средством, что поможет выделить вену, а также продезинфицирует кожу. Может оказаться целесообразным нанести местный анестезирующий крем (например, EMLA, AstraZeneca) на пораженный участок за 30–60 мин до венепункции, чтобы предотвратить любой дискомфорт.
Взятие пробы
При венепункции иглой иглу следует держать срезом вверх и направлять через кожу по ходу вены. Попав в просвет вены, что определяется наличием крови во втулке иглы, иглу следует провести параллельно коже до втулки так, чтобы тело иглы оказалось в просвете вены. При необходимости игла может быть изогнута под углом для облегчения ее введения в вену; например, в яремной вене хорька (см. рис. 7.6).
При необходимости игла может быть изогнута под углом для облегчения ее введения в вену; например, в яремной вене хорька (см. рис. 7.6).
Аналогичный метод можно использовать для игл-бабочек. Канюли над иглой можно использовать почти для всех видов, за исключением, возможно, мышей. Выберите самую большую и длинную канюлю, которая будет проходить в вену. Состригите шерсть с широкой области над веной и очистите кожу, как указано выше. Поднимите и зафиксируйте вену (для этого может потребоваться помощник), снимите пробку со стилета, проходящего через канюлю, и введите его через кожу до тех пор, пока кончик не окажется в просвете сосуда, а кровь не будет видна в головке канюли. стилет. Для толстокожих животных, возможно, стоит сначала сделать крошечный разрез кожи, используя скошенный край иглы или нет. 11 лезвие скальпеля для облегчения прохождения канюли через кожу. Затем канюлю можно ввести в вену, удерживая стилет: это предотвращает разрыв стилетом вены по мере продвижения вверх по сосуду, а также стилет блокирует просвет канюли, поэтому кровь может быть взята только после удаления стилета. . Гибкие канюли менее травматичны для тканей, чем иглы, и поэтому менее болезненны при введении и более подходят для длительной канюляции.
. Гибкие канюли менее травматичны для тканей, чем иглы, и поэтому менее болезненны при введении и более подходят для длительной канюляции.
Вены вокруг иглы спадутся, если попытаться слишком быстро взять кровь, поэтому требуется терпение, особенно при работе с мелкими млекопитающими. Для этих видов крови можно позволить капать из иглы или гибкой канюли, помещенной в вену. К более крупным животным можно присоединить шприц и применить осторожное отсасывание. Можно использовать вакуумные трубки, если это позволяет диаметр вены. Их легко и быстро использовать, но они могут увеличить вероятность гемолиза, поскольку клетки крови могут быть повреждены при быстром попадании в контейнер с низким давлением. После забора крови следует приложить к месту взятия тампон и удалить иглу, при этом на вену оказывается давление на 30–60 с для предотвращения кровотечения. Затем следует проверить это место, чтобы убедиться, что кровотечение остановилось, и при необходимости применить дополнительное давление.
Потенциальные последствия
Может произойти кровотечение из проколотой вены. В этом случае следует оказывать давление до тех пор, пока кровотечение не прекратится. Доступны повязки, ускоряющие гемостаз (например, Kaltostat, Convatec). Синяки могут возникнуть, если вена кровоточит под кожей. Давление должно быть применено, как указано выше, и место перепроверено через 30 мин. Если ушибленная область продолжает распространяться, следует обратиться за советом к ветеринарному хирургу. Возникновение тромбоза или флебита после венепункции указывает на неправильную технику, и метод следует пересмотреть и обратиться за советом к ветеринарному хирургу.
Объем пробы
Объем взятой пробы определяется требованиями эксперимента и безопасным пределом, который можно взять, не причиняя беспокойства животному. В общем, следует брать как можно меньший объем. Как правило, при легкой степени тяжести следует удалять не более 10% объема крови за один раз и менее 15% объема крови за любой 30-дневный период. У животных примерно 70 мл крови на килограмм массы тела, но это зависит от вида (см. Таблицу 7.3), и изъятие меньшего объема крови может иметь пагубные последствия, если животное находится под угрозой. Большие объемы могут быть отозваны с небольшим эффектом, если одновременно проводится замещение объема. Максимальные пределы объема и частоты отбора проб обычно указываются в экспериментальном протоколе.
У животных примерно 70 мл крови на килограмм массы тела, но это зависит от вида (см. Таблицу 7.3), и изъятие меньшего объема крови может иметь пагубные последствия, если животное находится под угрозой. Большие объемы могут быть отозваны с небольшим эффектом, если одновременно проводится замещение объема. Максимальные пределы объема и частоты отбора проб обычно указываются в экспериментальном протоколе.
Таблица 7.3 (a) Практические объемы проб крови для лабораторных видов. (b) Практические объемы взятия проб крови для более крупных домашних видов.
Методы венепункции у разных видов
Грызуны
У хвостатых грызунов обычным местом венепункции является хвостовая вена. Обычно используются боковые хвостовые вены, так как они больше, чем спинная и брюшная вены. Согревание хвоста сначала увеличивает приток крови к участку и облегчает сбор образцов. Образцы крови можно получить, надрезав кожу над веной с помощью стерильного ланцета и собрав кровь в обычную капиллярную трубку или капиллярную трубку с антикоагулянтным покрытием, или позволив ей капать в контейнер. Лезвия скальпеля использовать не рекомендуется, так как они могут легко соскользнуть и повредить хвост. Образцы большего размера можно получить у крыс, поместив гибкую канюлю 23–26 G или иглу-бабочку в хвостовую вену и позволив крови стечь в емкость для сбора или осторожно отсосав ее шприцем. Если используется игла-бабочка, пластиковую трубку следует укоротить во избежание образования в ней тромбов.
Лезвия скальпеля использовать не рекомендуется, так как они могут легко соскользнуть и повредить хвост. Образцы большего размера можно получить у крыс, поместив гибкую канюлю 23–26 G или иглу-бабочку в хвостовую вену и позволив крови стечь в емкость для сбора или осторожно отсосав ее шприцем. Если используется игла-бабочка, пластиковую трубку следует укоротить во избежание образования в ней тромбов.
Для мышей и бесхвостых животных можно использовать подкожную вену16 (см. также film.oslovet.veths.no/). Вена пунктируется иглой 23 или 25 G, в месте прокола образуется капля крови, которую можно собрать в микрокапиллярную пробирку. Струп, который образуется на месте прокола, можно осторожно стереть, чтобы можно было собрать серийные образцы с одного и того же места прокола. У крупных животных эту вену можно канюлировать17.
Ампутация кончика хвоста для получения образца смешанной артериальной и венозной крови может проводиться у крыс, мышей и песчанок, но должна проводиться под общей анестезией21. У мышей это, по-видимому, не связано с удалением каких-либо позвонков, как у крыс. Это должно быть выполнено только в одном случае.
У мышей это, по-видимому, не связано с удалением каких-либо позвонков, как у крыс. Это должно быть выполнено только в одном случае.
Большие образцы могут быть получены от крыс и песчанок путем пункции яремной вены, обычно под общей анестезией. Вену поднимают на одной стороне шеи, оказывая давление на вход в грудную клетку, и иглу вводят через кожу в вену, направленную к голове.
Кровь также можно получить путем пункции поверхностной височной вены на лице стерильным ланцетом18. Лицевые вены идут вверх от шеи и делятся в углу челюсти на поверхностную височную вену, идущую к глазу, и лицевую вену, идущую вдоль линии челюсти. Держите мышь большим щипком за шкирку с левой стороны: глаза должны быть слегка выпучены. Вену можно пунктировать, так как она проходит вдоль нижней челюсти, непосредственно под латеральным уголком глазного яблока. У белых мышей имеется серая точка, обозначающая сальную железу на челюсти, и место прокола находят, отодвигая от этой железы один глаз на длину назад и на один глаз на ширину вверх. У черных мышей есть черная точка, обозначающая железу. Вена должна быть смело проколота ланцетом, и кровь должна попасть в собирательный сосуд, чтобы избежать гемолиза. Кровь свободно течет из этого места, если оно выполнено правильно, и необходимо соблюдать осторожность, чтобы не взять избыток крови. Этот метод требует обучения и практики перед использованием, и рекомендуется анестезия (см. ссылку 19).).
У черных мышей есть черная точка, обозначающая железу. Вена должна быть смело проколота ланцетом, и кровь должна попасть в собирательный сосуд, чтобы избежать гемолиза. Кровь свободно течет из этого места, если оно выполнено правильно, и необходимо соблюдать осторожность, чтобы не взять избыток крови. Этот метод требует обучения и практики перед использованием, и рекомендуется анестезия (см. ссылку 19).).
У некоторых бесхвостых животных, таких как морские свинки, можно брать крошечные образцы из ушных вен.
Для окончательного отбора проб допускается выполнение пункции сердца, которая должна проводиться под терминальной общей анестезией. Есть много потенциально опасных последствий этой процедуры, например, тампонада сердца. До сердца можно добраться, положив животное на правый бок и проткнув левый желудочек через грудную стенку в шестом межреберье на одну треть вверх, чтобы получить артериальную кровь, или проткнув правый желудочек животным на его левая сторона для венозной крови. В качестве альтернативы животное можно положить на спину и достать до сердца, проведя иглу под грудиной и через диафрагму.
В качестве альтернативы животное можно положить на спину и достать до сердца, проведя иглу под грудиной и через диафрагму.
Кролики
Кровь можно относительно легко собрать из краевой вены уха с помощью канюли с надрезом или иглы-бабочки. Кожу над веной обрезают и очищают подходящим дезинфицирующим средством, затем за 30–60 мин до венепункции наносят крем с местным анестетиком. Также можно применять периферические сосудорасширяющие средства за 5–10 мин до забора крови. После того, как вена наполнится кровью, вставляется канюля, и можно собирать кровь, позволяя ей капать в горшок. После сбора сосудорасширяющее средство вытирают и надавливают до тех пор, пока кровотечение не прекратится. Кровотечение из центральной ушной артерии возможно, но может привести к образованию больших гематом, которые могут вызвать повреждение уха или даже некроз.
Хорьки
Для небольшого количества крови можно обрезать ноготь на пальце ноги и собрать каплю крови в капиллярную трубку. Для образцов среднего размера можно использовать подкожную или вентральную хвостовую вену, в то время как большие количества можно собирать из яремной вены. Шерсть на шее должна быть хорошо подстрижена, а вена приподнята, поместив большой палец над яремной канавкой в грудном входе. Иглу можно вводить, направляя ее вверх по вене к голове или вниз к входу в грудную клетку. Кожа очень толстая, и может потребоваться некоторое давление, чтобы проникнуть через кожу. Сбор можно облегчить, согнув иглу под углом 30° до проникновения в кожу или введя иглу через кожу параллельно вене, а затем в вену. Давление на вену грудного отдела сохраняется до тех пор, пока не будет собрана кровь (см. рис. 7.6).
Для образцов среднего размера можно использовать подкожную или вентральную хвостовую вену, в то время как большие количества можно собирать из яремной вены. Шерсть на шее должна быть хорошо подстрижена, а вена приподнята, поместив большой палец над яремной канавкой в грудном входе. Иглу можно вводить, направляя ее вверх по вене к голове или вниз к входу в грудную клетку. Кожа очень толстая, и может потребоваться некоторое давление, чтобы проникнуть через кожу. Сбор можно облегчить, согнув иглу под углом 30° до проникновения в кожу или введя иглу через кожу параллельно вене, а затем в вену. Давление на вену грудного отдела сохраняется до тех пор, пока не будет собрана кровь (см. рис. 7.6).
Приматы
Наилучший метод забора крови у приматов — использование бедренной вены в паху. Эта вена плохо видна, и ее положение необходимо определять пальпацией. Иглу вводят в бедренный треугольник несколько медиальнее бедренного пульса и направляют в краниомедиальном направлении. Иглу следует продвигать медленно до тех пор, пока не будет достигнут сосуд, что определяется наличием крови в ступице иглы. Для более крупных обезьян Старого Света можно использовать головную вену на верхней части передней ноги ниже локтя, как для кошек и собак. В качестве альтернативного пути можно использовать яремную вену. Микрокапиллярную трубку можно использовать для сбора небольших образцов из пятки приматов без анестезии после того, как они были обучены принимать минимальные ограничения. У мартышек также может быть кровотечение из копчиковой вены.
Для более крупных обезьян Старого Света можно использовать головную вену на верхней части передней ноги ниже локтя, как для кошек и собак. В качестве альтернативного пути можно использовать яремную вену. Микрокапиллярную трубку можно использовать для сбора небольших образцов из пятки приматов без анестезии после того, как они были обучены принимать минимальные ограничения. У мартышек также может быть кровотечение из копчиковой вены.
Собаки и кошки
Малые и средние образцы могут быть взяты из головной вены на передней лапе. Кожа над передней частью передней ноги подготавливается путем стрижки и очистки, затем дрессировщик удерживает животное, кладя одну руку на тело животного, удерживая ногу вперед, помещая два пальца за локоть животного, приподнимая вену большим пальцем. над верхней частью ноги и удерживая заднюю часть животного локтем. Вторую руку кладут под подбородок, чтобы приподнять голову животного. У них также может быть кровотечение из яремной вены. Дрессировщик кладет правую руку на тело животного, чтобы удерживать передние лапы. Локоть используется для удержания тела животного на теле дрессировщика (рис. 7.9).). Левая рука помещается под подбородок, чтобы поднять голову. Человек, собирающий кровь, поднимает вену, помещая большой палец в яремную борозду у входа в грудную клетку.
Локоть используется для удержания тела животного на теле дрессировщика (рис. 7.9).). Левая рука помещается под подбородок, чтобы поднять голову. Человек, собирающий кровь, поднимает вену, помещая большой палец в яремную борозду у входа в грудную клетку.
РИСУНОК 7.9. Держите кошку для пункции яремной вены.
Читать дальше могут только участники с золотым статусом. Войдите или зарегистрируйтесь, чтобы продолжить
30 июля 2017 г. | Опубликовано администратором в ОБЩИЕ | Комментарии к записи «Обработка и методы»
Методы инъекций — Ветеринарная клиника Королевства 9 отключены0001
Инъекционное введение лекарства часто называют парентеральным путем (это означает, что лекарство не попадает в организм через кишечник). Эффективное лекарственное введение является ключевой частью большинства ветеринарных процедур, и многие лекарства наиболее эффективны при введении в виде инъекций. Введение лекарств путем инъекций необходимо для некоторых лекарств, которые разрушаются кислотами в желудке, например инсулина.
Общая информация
Инъекции можно делать в:
- мышцу (внутримышечно)
- ткань подкожная (подкожная)
- кровообращение (внутривенное)
- кожный (внутрикожный)
- полости тела (брюшная, т.е. внутрибрюшинная, или грудная, т.е. внутриплевральная)
В этом Информационном бюллетене рассматриваются только внутримышечный и подкожный пути введения, так как именно с ними чаще всего сталкиваются владельцы кошек.
При проведении инъекций всегда следует применять асептические методы. Если шерсть очень грязная, ее следует подстричь и почистить. Кожу следует протереть спиртом. Никогда не вводите инъекцию через грязную или инфицированную кожу.
Различные лекарственные формы для инъекций используются для разных путей, и особенно важно не вводить инъекцию непосредственно в кровь, если это специально не рекомендовано для этого пути.
Подкожная инъекция
Этот путь используется для введения большинства инъекций и прививок. У домашних животных много дряблой кожи, поэтому очень просто приподнять кожный лоскут и ввести иглу в подкожную клетчатку. Под кожей находится несколько важных (или легко повреждаемых) структур, поэтому это очень безопасный способ введения лекарств, и владельцев можно легко научить делать инъекции таким образом. Владельцев животных с диабетом учат, как вводить инсулин подкожно, чтобы они могли делать регулярные инъекции своему питомцу дома. Этот путь не подходит для введения раздражающих препаратов, так как они могут вызвать некроз кожи и шелушение.
У домашних животных много дряблой кожи, поэтому очень просто приподнять кожный лоскут и ввести иглу в подкожную клетчатку. Под кожей находится несколько важных (или легко повреждаемых) структур, поэтому это очень безопасный способ введения лекарств, и владельцев можно легко научить делать инъекции таким образом. Владельцев животных с диабетом учат, как вводить инсулин подкожно, чтобы они могли делать регулярные инъекции своему питомцу дома. Этот путь не подходит для введения раздражающих препаратов, так как они могут вызвать некроз кожи и шелушение.
Внутримышечная инъекция
Препараты, вводимые в мышцы, всасываются очень быстро, поскольку эта область хорошо кровоснабжается. Инъекция в мышечную ткань сопряжена с риском, поскольку через мышечную ткань проходит много важных структур, например артерий, вен и нервов. Перед инъекцией важно убедиться, что игла случайно не попала в кровеносный сосуд (особенно в артерию) в мышце. После введения иглы в мышцу необходимо осторожно отсосать шприц, чтобы кровь не попала обратно в иглу.
Одним из недостатков введения препарата глубоко в мышечную ткань является то, что трудно понять, что происходит в месте инъекции после того, как инъекция была сделана. Травматическая техника может привести к образованию синяков, а у животных с нарушением свертываемости крови (например, при отравлении антикоагулянтами-родентицидами) кровотечение после внутримышечной инъекции может быть сильным. Однако, поскольку место инъекции скрыто, эти осложнения могут оставаться незамеченными в течение нескольких часов или дней.
Подходящими местами для внутримышечных инъекций являются четырехглавая мышца (на передней поверхности бедра), пояснично-дорсальные мышцы (по обе стороны от остистых отростков поясничных позвонков) или трехглавая мышца (позади плечевой кости передней ноги). Подколенные сухожилия (в задней части бедра) следует избегать из-за возможности повреждения седалищного нерва. Объемы инъекций у кошек не должны превышать 2 мл. Положительное действие при введении игл в мышцы уменьшает повреждение мышц и боль, а массирование места инъекции после инъекции рассеивает инъекцию и может помочь уменьшить боль.
Некоторые лекарства специально разработаны таким образом, что они медленнее всасываются и могут задерживаться в мышцах, постепенно всасываясь в течение многих месяцев (так называемые «депо-инъекции»).
Альтернативные пути введения лекарств
Дыхательные пути
Оболочка дыхательных путей тонкая и сосудистая, поэтому всасывание некоторых лекарств из этого места может быть очень быстрым. Интраназальные вакцины, например, от питомникового кашля, вводятся в нос, и живой вирус способен проникать через слизистую оболочку носа. Распыляемые лекарственные средства могут использоваться для лечения респираторных заболеваний, и введение таким путем позволяет быстро проникнуть в местный участок, где они должны оказывать свое действие. Однако использование небулайзеров означает, что пациент должен дышать воздухом, содержащим лекарство. Распыляемые лекарства можно вводить через лицевую маску, хотя многие пациенты в сознании не переносят лицевую маску, поэтому часто требуется специальная камера для распыления. При остановке сердца адреналин иногда вводят через эндотрахеальную трубку, и всасывание этим путем происходит быстро, и этот метод намного безопаснее, чем альтернативная внутрисердечная инъекция адреналина.
При остановке сердца адреналин иногда вводят через эндотрахеальную трубку, и всасывание этим путем происходит быстро, и этот метод намного безопаснее, чем альтернативная внутрисердечная инъекция адреналина.
Тотальная инъекционная анестезия собак и кошек для удаленной ветеринарной стерилизационой клиники | BMC Veterinary Research
- Исследовательская статья
- Открытый доступ
- Опубликовано:
- Лиза Пэм Познер ORCID: orcid.org/0000-0003-4579-9648 1 ,
- Джеффри Эпплгейт 1 ,
- Allen Cannedy 1 ,
- Diane Deresienski 1 ,
- Kristie Mozzachio 1 ,
- Maria Serrano 1 &
- …
- Gregory Lewbart 1
Ветеринарные исследования BMC том 16 , Номер статьи: 304 (2020) Процитировать эту статью
5651 Доступ
2 Цитаты
3 Альтметрика
Сведения о показателях
Abstract
История вопроса
Клиники стерилизации часто расположены в отдаленных местах, где наркозные аппараты и сжатый кислород недоступны. В этом исследовании описывается использование тотальной инъекционной анестезии у собак и кошек, поступающих на стерилизацию в удаленном месте.
В этом исследовании описывается использование тотальной инъекционной анестезии у собак и кошек, поступающих на стерилизацию в удаленном месте.
Результаты
Всего было стерилизовано 100 животных; 26 кошек-самок (CF), 22 кота-самца (CM), 28 собак-самок (DF) и 24 собаки-самца (DM). МВ анестезировали дексмедетомидином (20 мкг/кг), кетамином (8 мг/кг) и гидроморфоном (0,1 мг/кг) внутримышечно. КМ анестезировали дексмедетомидином (15 мкг/кг), кетамином (5 мг/кг) и гидроморфоном (0,1 мг/кг) внутримышечно. Недостаточную анестезию у кошек лечили внутримышечным введением альфаксалона (1 мг/кг). Всем кошкам вводили мелоксикам в дозе 0,3 мг/кг п/к. ДФ анестезировали дексмедетомидином (15 мкг/кг), кетамином (7–10 мг/кг) и гидроморфоном (0,1 мг/кг) внутримышечно. СД анестезировали дексмедетомидином (15 мкг/кг), кетамином (5 мг/кг) и гидроморфоном (0,1 мг/кг) внутримышечно. Всем собакам был установлен внутривенный катетер и эндотрахеальная трубка. Если SpO 2 < 91%, искусственная вентиляция легких с помощью мешка Амбу. Недостаточную анестезию у собак лечили альфаксалоном (1 мг/кг) внутривенно. Всем собакам вводили мелоксикам в дозе 0,2 мг/кг п/к. После операции атипамезол (0,05–0,1 мг/кг) в/м вводили всем пациентам, у которых не было произвольных движений. Все пациенты выжили и были выписаны. Менее 25% кошек и кобелей собак нуждались в дополнительной анестезии. Пятьдесят семь процентов самок собак нуждались в дополнительной анестезии. Более 89% пациентов (в любой группе), которым потребовалось введение атипамезола. Одна кошка выздоровела с возбуждением и гипертермией (41,1C/106F). Некоторым собакам требовалась вспомогательная вентиляция легких, чтобы оставаться в нормоксемическом состоянии во время анестезии.
Недостаточную анестезию у собак лечили альфаксалоном (1 мг/кг) внутривенно. Всем собакам вводили мелоксикам в дозе 0,2 мг/кг п/к. После операции атипамезол (0,05–0,1 мг/кг) в/м вводили всем пациентам, у которых не было произвольных движений. Все пациенты выжили и были выписаны. Менее 25% кошек и кобелей собак нуждались в дополнительной анестезии. Пятьдесят семь процентов самок собак нуждались в дополнительной анестезии. Более 89% пациентов (в любой группе), которым потребовалось введение атипамезола. Одна кошка выздоровела с возбуждением и гипертермией (41,1C/106F). Некоторым собакам требовалась вспомогательная вентиляция легких, чтобы оставаться в нормоксемическом состоянии во время анестезии.
Заключение
Тотальная инъекционная анестезия может применяться в удаленных стерилизационных клиниках с минимальными осложнениями.
История вопроса
Нежелательное размножение у собак и кошек негативно влияет на сообщества, способствуя: распространению болезней, агрессии по отношению к людям, неприятному поведению (например, попаданию в мусор) и хищничеству других видов (например, диких птиц). Стерилизация как домашних, так и диких собак и кошек часто требуется в отдаленных или слаборазвитых районах, где доступ к ветеринарной медицине ограничен или отсутствует. Программы стерилизации предлагаются в различных стилях в этих местах через мобильные клиники, но доступ к помещениям и оборудованию варьируется. Ассоциация ветеринаров приютов предложила рекомендации по обеспечению постоянного ухода за собаками и кошками, поступающими в эти клиники [1, 2]. Однако эти рекомендации предполагают доступ к оборудованию, которое может отсутствовать в некоторых удаленных местах, например, к сжатым газам (например, кислороду) или аппаратам для анестезии [1, 2].
Стерилизация как домашних, так и диких собак и кошек часто требуется в отдаленных или слаборазвитых районах, где доступ к ветеринарной медицине ограничен или отсутствует. Программы стерилизации предлагаются в различных стилях в этих местах через мобильные клиники, но доступ к помещениям и оборудованию варьируется. Ассоциация ветеринаров приютов предложила рекомендации по обеспечению постоянного ухода за собаками и кошками, поступающими в эти клиники [1, 2]. Однако эти рекомендации предполагают доступ к оборудованию, которое может отсутствовать в некоторых удаленных местах, например, к сжатым газам (например, кислороду) или аппаратам для анестезии [1, 2].
Галапагосские острова — архипелаг у берегов Эквадора. Несмотря на то, что многие острова известны своей интересной и разнообразной дикой природой, на многих островах есть большие популяции нетронутых собак и кошек, которые предшествовали местным и исчезающим видам дикой природы (например, птицам, черепахам, морским игуанам) [3,4,5,6]. Остров Исабела — самый большой из Галапагосских островов, но его население составляет всего около 1800 человек [7], и до него можно добраться в основном на лодке. Поэтому на островах, подобных этому, получение всего оборудования, необходимого для стерилизации, представляет собой серьезную логистическую проблему. На этапе планирования считалось нецелесообразным перевозить наркозный аппарат и/или кислородные баллоны (без возможности их пополнения) на остров Изабела. Поэтому по необходимости от команды требовалось планировать клинику с использованием только инъекционных анестетиков. В то время как анестезия для больших объемов была изучена в недорогих клиниках кастрации/кастрации [8, 9].], большинство этих исследований было проведено в местах, где ресурсы доступны в случае необходимости, даже если они не используются рутинно (например, наркозные аппараты/кислород). И наоборот, существует недостаток информации об анестезии и осложнениях в отдаленных клиниках стерилизации/кастрации, где недоступно использование кислорода и/или ингаляционных анестетиков.
Остров Исабела — самый большой из Галапагосских островов, но его население составляет всего около 1800 человек [7], и до него можно добраться в основном на лодке. Поэтому на островах, подобных этому, получение всего оборудования, необходимого для стерилизации, представляет собой серьезную логистическую проблему. На этапе планирования считалось нецелесообразным перевозить наркозный аппарат и/или кислородные баллоны (без возможности их пополнения) на остров Изабела. Поэтому по необходимости от команды требовалось планировать клинику с использованием только инъекционных анестетиков. В то время как анестезия для больших объемов была изучена в недорогих клиниках кастрации/кастрации [8, 9].], большинство этих исследований было проведено в местах, где ресурсы доступны в случае необходимости, даже если они не используются рутинно (например, наркозные аппараты/кислород). И наоборот, существует недостаток информации об анестезии и осложнениях в отдаленных клиниках стерилизации/кастрации, где недоступно использование кислорода и/или ингаляционных анестетиков. Цель состояла в том, чтобы описать использование тотальной инъекционной анестезии у собак и кошек, поступающих на хирургическую стерилизацию в удаленном месте.
Цель состояла в том, чтобы описать использование тотальной инъекционной анестезии у собак и кошек, поступающих на хирургическую стерилизацию в удаленном месте.
Результаты
Всего было стерилизовано 100 пациентов. Температура в операционных и послеоперационных палатах колебалась в пределах 79,2–83,4 °F (26,2–28,8 °C). Сигнал и наличие беременности представлены в таблице 1.
Таблица 1 Сигнал и статус беременности у всех пациентокПолноразмерная таблица
Все пациентки пережили анестезию и операцию и были выписаны. Ни одной из кошек не потребовалась вентиляционная поддержка через мешок Амбу и установка эндотрахеальной трубки на основе RR и Sp0 2 %. При вспомогательной вентиляции все собаки оставались нормоксемическими (SpO 2 > 91%) во время анестезии. Время от инъекции анестетика до начала операции, время операции, общее время пациента и необходимые препараты неотложной помощи представлены в таблице 2.
Полная таблица
Количество пациентов, которым вводили атипамезол, общее количество введенного атипамезола, время от атипамезола до выздоровления, время до выздоровления после введения атипамезола , и температура при восстановлении представлены в табл. 3.
Таблица 3 Потребность в препаратах для реверсии, продолжительность восстановления после реверсии и температура восстановленияПолноразмерная таблица
После OVH у одной из кошек было возбужденное выздоровление и гипертермия (106F/41,1C). За кошкой наблюдали во время выздоровления, и как гипертермия, так и возбуждение разрешились без лечения. Первым трем кастрированным собакам вводили кетамин в дозе 7 мг/кг, и после выхода из наркоза у них наблюдалась дисфория. По указанию анестезиолога последующим собакам доза кетамина была снижена до 5 мг/кг, и ни у одной другой собаки не наблюдалось выздоровления от дисфории. У трех собак с OVH было выздоровление от дисфории, и их лечили ацепромазином в дозе 0,01 мг/кг внутривенно (Acepromazine, Vedco Inc., Сент-Джозеф, штат Миссури), который разрешил дисфорию. Две собаки, представленные для кастрации, продемонстрировали судорожную активность во время индукции; мышечная ригидность и мышечный спазм. Судорожную активность у обеих собак лечили альфаксалоном в дозе 1–2 мг/кг внутривенно; прекращение мышечных фасцикуляций и наступила мышечная релаксация. Обе собаки были кастрированы и выздоровели без происшествий. Остальные собаки и кошки выздоровели хорошо, без явных признаков боли/дискомфорта. Собаки, перенесшие OVH, были выписаны с карпрофеном в дозе приблизительно 4 мг/кг перорально SID в течение 3 дней.
У трех собак с OVH было выздоровление от дисфории, и их лечили ацепромазином в дозе 0,01 мг/кг внутривенно (Acepromazine, Vedco Inc., Сент-Джозеф, штат Миссури), который разрешил дисфорию. Две собаки, представленные для кастрации, продемонстрировали судорожную активность во время индукции; мышечная ригидность и мышечный спазм. Судорожную активность у обеих собак лечили альфаксалоном в дозе 1–2 мг/кг внутривенно; прекращение мышечных фасцикуляций и наступила мышечная релаксация. Обе собаки были кастрированы и выздоровели без происшествий. Остальные собаки и кошки выздоровели хорошо, без явных признаков боли/дискомфорта. Собаки, перенесшие OVH, были выписаны с карпрофеном в дозе приблизительно 4 мг/кг перорально SID в течение 3 дней.
Многим пациентам при выписке были назначены антибиотики и антигельминтные препараты, но эти данные не входят в предмет данной статьи.
Статистика
Описательная статистика представлена медианой и диапазонами (мин-макс).
Обсуждение
Представленные данные подтверждают гипотезу о том, что анестезия в клиниках стерилизации/кастрации может проводиться в отдаленных местах, где наркозные аппараты и/или кислород недоступны. Кроме того, в этом исследовании оценивались анестезиологические протоколы, которые обеспечивали быструю анестезию, но позволяли отменить и быстро восстановить пациентов. Это важно во многих отдаленных местах, так как часто бывает мало или вообще нет клеток для выздоравливающих / зон содержания, некоторые пациенты дикие, и чем дольше пациент остается на попечении клиники, тем меньше пациентов можно увидеть в день. Общее время пребывания пациента в клинике составило примерно 1 час, при этом кастрация кошек требовала наименьшего пребывания, а OVH собак требовала наибольшего времени.
Кроме того, в этом исследовании оценивались анестезиологические протоколы, которые обеспечивали быструю анестезию, но позволяли отменить и быстро восстановить пациентов. Это важно во многих отдаленных местах, так как часто бывает мало или вообще нет клеток для выздоравливающих / зон содержания, некоторые пациенты дикие, и чем дольше пациент остается на попечении клиники, тем меньше пациентов можно увидеть в день. Общее время пребывания пациента в клинике составило примерно 1 час, при этом кастрация кошек требовала наименьшего пребывания, а OVH собак требовала наибольшего времени.
Продолжительность операции колебалась от 1 мин до 1 ч. Это затруднило оценку дозировок препаратов для внутримышечного введения. Неудивительно, что 1% кастрированных кошек нуждались в экстренной анестезии, в то время как 57% собак, перенесших OVH, нуждались в дополнительных анестетиках. У кошек, недостаточно анестезированных во время операции, внутримышечное введение альфаксалона обеспечивало быстрое углубление анестезии. Внутримышечное введение альфаксалона оценивалось у кошек на предмет физиологической стабильности и фармакокинетических/фармакодинамических профилей [10, 11]. При введении кошкам в дозе 5 мг/кг внутримышечно кошки демонстрировали хорошую физиологическую стабильность, но качество восстановления считалось плохим [10]. В другом исследовании было показано, что внутримышечный альфаксалон в той же дозировке достигает пиковой концентрации (Tmax) через ~ 22 мин [11]. Кошки в этом исследовании не продемонстрировали каких-либо неприятных характеристик восстановления, вероятно, из-за меньшей дозы, использованной в этом исследовании (1,0 мг/кг в/м). Кроме того, внутримышечное введение альфаксалона действовало достаточно быстро, чтобы его можно было считать хорошим выбором для экстренной анестезии во время хирургической процедуры у кошки. Основываясь на Tmax ~ 22 мин, было неожиданно, но повторяемо, что дозировка и путь были достаточными. Успех дозировки и пути введения альфаксалона у кошек, вероятно, был обусловлен надежными дозировками используемых индуцирующих агентов.
Внутримышечное введение альфаксалона оценивалось у кошек на предмет физиологической стабильности и фармакокинетических/фармакодинамических профилей [10, 11]. При введении кошкам в дозе 5 мг/кг внутримышечно кошки демонстрировали хорошую физиологическую стабильность, но качество восстановления считалось плохим [10]. В другом исследовании было показано, что внутримышечный альфаксалон в той же дозировке достигает пиковой концентрации (Tmax) через ~ 22 мин [11]. Кошки в этом исследовании не продемонстрировали каких-либо неприятных характеристик восстановления, вероятно, из-за меньшей дозы, использованной в этом исследовании (1,0 мг/кг в/м). Кроме того, внутримышечное введение альфаксалона действовало достаточно быстро, чтобы его можно было считать хорошим выбором для экстренной анестезии во время хирургической процедуры у кошки. Основываясь на Tmax ~ 22 мин, было неожиданно, но повторяемо, что дозировка и путь были достаточными. Успех дозировки и пути введения альфаксалона у кошек, вероятно, был обусловлен надежными дозировками используемых индуцирующих агентов. Для собак, которые были недостаточно анестезированы перед операцией, внутривенное введение альфаксалона обеспечило подходящие условия для собачьего OVH и кастрации для поддержания анестезии. Это согласуется с данными, показывающими, что после премедикации инфузия альфаксалона с постоянной скоростью создавала подходящие условия анестезии для собак, перенесших OVH [12]. Однако как в исследовании Suarez, так и в этом исследовании многим собакам требовалась вспомогательная вентиляция легких, чтобы оставаться в нормоксемическом состоянии [12].
Для собак, которые были недостаточно анестезированы перед операцией, внутривенное введение альфаксалона обеспечило подходящие условия для собачьего OVH и кастрации для поддержания анестезии. Это согласуется с данными, показывающими, что после премедикации инфузия альфаксалона с постоянной скоростью создавала подходящие условия анестезии для собак, перенесших OVH [12]. Однако как в исследовании Suarez, так и в этом исследовании многим собакам требовалась вспомогательная вентиляция легких, чтобы оставаться в нормоксемическом состоянии [12].
Из-за нехватки мест для посадки и возможности пребывания пациентов без присмотра на улице всем животным, которые не могли ходить, вводили атипамезол. Несмотря на то, что рассматривалась потеря анальгезии, у кошек есть доказательства того, что введение атипамезола не оказывало негативного влияния на послеоперационную анальгезию у кошек, которые также получали опиоид и кетамин, как это использовалось в этом исследовании [13]. Кроме того, все животные получали НПВП для дополнительного обезболивания. Подавляющему большинству пациентов требовался антагонизм дексмедетомидина с атипамезолом (89–100% больных). У первых трех кастрированных собак после введения атипамезола возникло возбуждение/дисфория. Кетамин в анестетических дозах связан с высокой частотой возбуждения в периоде выздоровления у людей и ветеринарных пациентов [14, 15]. Анестезиологи часто комбинируют введение кетамина с другими депрессантами ЦНС, такими как бензодиазепины и агонисты альфа-2-адренорецепторов, чтобы сбалансировать риск возбужденного восстановления после анестезии [15]. Таким образом, наиболее вероятной причиной возбуждения после введения атипамезола у этих собак была потеря депрессии ЦНС из-за дексмедетомидина, который уравновешивал поведенческие эффекты кетамина в относительно короткой операции по кастрации. Сразу же после выздоровления трех дисфорических кастрированных собак анестезиолог уменьшил дозу кетамина с 7 мг/кг до 5 мг/кг, и ни у одной из последующих кастраций не было дисфорического выздоровления.
Подавляющему большинству пациентов требовался антагонизм дексмедетомидина с атипамезолом (89–100% больных). У первых трех кастрированных собак после введения атипамезола возникло возбуждение/дисфория. Кетамин в анестетических дозах связан с высокой частотой возбуждения в периоде выздоровления у людей и ветеринарных пациентов [14, 15]. Анестезиологи часто комбинируют введение кетамина с другими депрессантами ЦНС, такими как бензодиазепины и агонисты альфа-2-адренорецепторов, чтобы сбалансировать риск возбужденного восстановления после анестезии [15]. Таким образом, наиболее вероятной причиной возбуждения после введения атипамезола у этих собак была потеря депрессии ЦНС из-за дексмедетомидина, который уравновешивал поведенческие эффекты кетамина в относительно короткой операции по кастрации. Сразу же после выздоровления трех дисфорических кастрированных собак анестезиолог уменьшил дозу кетамина с 7 мг/кг до 5 мг/кг, и ни у одной из последующих кастраций не было дисфорического выздоровления. Большинству пациентов потребовалась только одна доза атипамезола, а четырем пациентам потребовались вторые дозы (кастрированные кошки ( n = 1), собачий OVH (n = 1), собачий кастрированный ( n = 2). После OVH три собаки продемонстрировали дисфорическое выздоровление. Всех трех собак лечили ацепромазином, который успешно их успокоил. Оглядываясь назад, можно было бы уменьшить дозу кетамина у собак с OVH и увеличить дозу альфаксалона для интраоперационной поддерживающей терапии. Однако из 28 проведенных собак OVH только у трех было дисфорическое выздоровление (11%). Ни одна из собак или кошек не нуждалась в дополнительном обезболивании перед выпиской. Как и ожидалось, комбинация агониста альфа-2, опиоида и НПВП обеспечивала соответствующее обезболивание.
Большинству пациентов потребовалась только одна доза атипамезола, а четырем пациентам потребовались вторые дозы (кастрированные кошки ( n = 1), собачий OVH (n = 1), собачий кастрированный ( n = 2). После OVH три собаки продемонстрировали дисфорическое выздоровление. Всех трех собак лечили ацепромазином, который успешно их успокоил. Оглядываясь назад, можно было бы уменьшить дозу кетамина у собак с OVH и увеличить дозу альфаксалона для интраоперационной поддерживающей терапии. Однако из 28 проведенных собак OVH только у трех было дисфорическое выздоровление (11%). Ни одна из собак или кошек не нуждалась в дополнительном обезболивании перед выпиской. Как и ожидалось, комбинация агониста альфа-2, опиоида и НПВП обеспечивала соответствующее обезболивание.
Температура тела во время выздоровления колебалась в пределах 95,7–106 °F (35,4–41,1 °C). Анализ Таблицы 3 показывает, что у большинства пациентов сохранялась нормотермия. Вероятно, это было связано с сочетанием теплой хирургической/восстановительной среды, отсутствием холодных, сухих анестезирующих газов и коротким временем операции/анестезии. Одна кошка действительно стала значительно гипертермичной (106F, 41,1C). Гидроморфон был вовлечен в гипертермию после анестезии у кошек [16], но у этой кошки неясно, было ли возбуждение причиной или результатом гипертермии.
Одна кошка действительно стала значительно гипертермичной (106F, 41,1C). Гидроморфон был вовлечен в гипертермию после анестезии у кошек [16], но у этой кошки неясно, было ли возбуждение причиной или результатом гипертермии.
У двух кастрированных собак наблюдалась судорожная активность во время внутримышечной индукции анестезии. Обе собаки демонстрировали поведение судорожного типа с потерей реакции, но ни у одной из собак не было недержания мочи во время эпизода. Введение кетамина действительно усиливает судороги, подобные формам волны электроэнцефалограммы [17], и это было связано с возникновением судорог у различных видов животных [15]. Следовательно, возможно, что у обеих собак были судороги после введения высоких доз кетамина. Однако также возможно, что несбалансированное всасывание кетамина и дексмедетомидина после внутримышечного введения могло привести к преувеличенной стадии 2 анестезии (непроизвольное возбуждение), которая выглядела похожей на судорогу, а отсутствие ответа было связано с индукцией анестезии. У обеих этих собак фасцикуляция/сокращение мышц прекратились после внутривенного введения альфаксалона, и обе собаки выздоровели без осложнений.
У обеих этих собак фасцикуляция/сокращение мышц прекратились после внутривенного введения альфаксалона, и обе собаки выздоровели без осложнений.
Хотя дополнительный кислород не был доступен для пациентов в этом исследовании, многие рутинные процедуры, требующие анестезии, выполняются за пределами ветеринарной больницы без происшествий (например, кастрация лошадей, иммобилизация диких животных, стерилизация/кастрация). Аналогичным образом, несмотря на то, что эндотрахеальная интубация кошек под анестезией проводится регулярно, в «Руководстве по ветеринарной медицинской помощи для программ стерилизации-кастрации» Ассоциации ветеринаров приютов от 2016 г. указано, что приемлемо не интубировать кошек при кратковременных операциях (например, OVH и кастрациях), пока есть оборудование. для интубации доступен в экстренных ситуациях [1]. На основании пульсоксиметрии кошки оставались нормоксемическими, поэтому ни одной из кошек не потребовалась интубация во время анестезии. И наоборот, многим собакам для поддержания нормоксемии требовалась вспомогательная вентиляция легких через мешок Амбу и эндотрахеальную трубку. Установка и фиксация эндотрахеальной трубки существенно не увеличивали общее время процедуры и оказались важными для пациентов, нуждавшихся в искусственной вентиляции легких, особенно при отсутствии дополнительного кислорода. В то время как дополнительная безопасность дополнительного кислорода всегда предпочтительнее, это исследование показало, что большинство, если не все здоровые собаки и кошки могут быть надлежащим образом анестезированы для кастрации и OVH без дополнительного кислорода, хотя им может потребоваться интубация и вспомогательная вентиляция.
Установка и фиксация эндотрахеальной трубки существенно не увеличивали общее время процедуры и оказались важными для пациентов, нуждавшихся в искусственной вентиляции легких, особенно при отсутствии дополнительного кислорода. В то время как дополнительная безопасность дополнительного кислорода всегда предпочтительнее, это исследование показало, что большинство, если не все здоровые собаки и кошки могут быть надлежащим образом анестезированы для кастрации и OVH без дополнительного кислорода, хотя им может потребоваться интубация и вспомогательная вентиляция.
Основным ограничением данного исследования является то, что оно не было задумано как исследовательский проект, и поэтому некоторые данные не собирались последовательно. Тем не менее, он предоставляет ценную информацию об использовании тотальной инъекционной анестезии у собак и кошек без использования ингаляторов или кислорода. Необходимо провести физиологическую оценку собак и кошек, подвергнутых наркозу и стерилизованных в соответствии с этими протоколами. Дополнительные ограничения включают: вариабельность внутри каждой группы по возрасту и размеру пациента, вариабельность у четырех разных хирургов и различное состояние здоровья пациентов. Однако, поскольку такой тип изменчивости ожидается в условиях удаленной клиники, общий успех планов анестезии является многообещающим.
Дополнительные ограничения включают: вариабельность внутри каждой группы по возрасту и размеру пациента, вариабельность у четырех разных хирургов и различное состояние здоровья пациентов. Однако, поскольку такой тип изменчивости ожидается в условиях удаленной клиники, общий успех планов анестезии является многообещающим.
Заключение
Тотальная инъекционная анестезия может применяться в отдаленных стерилизационных клиниках с минимальными осложнениями.
Методы
В июне 2016 года группа из 14 добровольцев из США, работающих в ветеринарном сообществе, отправилась на остров Исабела, Галапагос, чтобы провести стерилизацию любой собаки или кошки (домашней или дикой). Команда состояла из девяти ветеринаров, одного лицензированного ветеринарного техника, двух ветеринарных помощников и двух общих помощников.
Местная организация «Инициатива межкультурного общения» предоставила рекламу клинике, а также здание, оборудованное электричеством и холодной водой. Все оборудование и припасы были доставлены добровольцами на лодке на остров.
Все оборудование и припасы были доставлены добровольцами на лодке на остров.
Владельцы или опекуны предоставили письменное информированное согласие на всех стерилизованных животных. Во время процесса получения согласия с каждым владельцем/опекуном присутствовал по крайней мере один переводчик. После госпитализации каждый пациент проходил медицинский осмотр у лечащего ветеринара, который решал, является ли пациент подходящим кандидатом на анестезию и стерилизацию. Каждое животное взвешивали на подвесных багажных весах. Критерии исключения включали: наличие лихорадки, рвоты/диареи, истощения или тяжелого сердечно-сосудистого заболевания. Протоколы анестезии были разработаны ветеринарным анестезиологом (LPP) для каждого вида и пола (таблица 4). Собак и кошек стерилизовали в порядке поступления. Дополнительные соображения для протоколов включали поведение диких пациентов, потенциальное паразитарное бремя/скрытое заболевание и отсутствие анестезиологических аппаратов или медицинского кислорода.
Полноразмерная таблица
После госпитализации каждой собаке и кошке был назначен специальный анестезиолог с момента премедикации до выздоровления. Каждое животное взвешивалось на подвесных весах, анестезиолог рассчитывал и выдавал анестетики. После в/м введения препарата каждого пациента каждые 5 мин оценивали на предмет физиологической стабильности путем мониторинга ЧСС, ЧДД, цвета слизистых оболочек. Пульсоксиметрия (Sp0 2 ) (Nonin 8500, Nonin Medical, Inc., Плимут, Миннесота) оценивали для каждого пациента, но не всегда регистрировали. Был доступен один осциллометрический монитор артериального давления (АД) (Cardell 9402, Sharn Veterinary In, Tampa, FL 33618), который периодически использовался по усмотрению анестезиолога, но значения регистрировались непоследовательно. Каждый анестезиолог был проинструктирован уведомлять анестезиолога, если Sp0 2 < 91% или САД < 65 мм рт.ст. Первоначальный протокол не включал внутривенные катетеры или эндотрахеальные трубки ни для собак, ни для кошек, с планом, согласно которому, если какой-либо собаке или кошке потребуется вентиляционная поддержка, им будет установлена эндотрахеальная трубка. Однако после первого дня анестезиолог изменил протокол, чтобы всем собакам в асептических условиях устанавливали внутривенный головной катетер для облегчения внутривенного введения лекарственного средства и эндотрахеальную трубку, помещаемую для облегчения вентиляции с помощью мешка Амбу по мере необходимости. Вентиляция проводилась через мешок Амбу, если SpO 9.1018 2 < 91%. Всем пациентам, которые были недостаточно анестезированы до или во время операции, вводили альфаксалон (1,0 мг/кг). Кошкам вводили альфаксалон внутримышечно, тогда как собакам вводили альфаксалон внутривенно. Частота дыхания и SpO 2 оценивались у всех кошек перед началом операции, чтобы определить, требуется ли эндотрахеальная трубка (если SpO 2 < 91%).
Первоначальный протокол не включал внутривенные катетеры или эндотрахеальные трубки ни для собак, ни для кошек, с планом, согласно которому, если какой-либо собаке или кошке потребуется вентиляционная поддержка, им будет установлена эндотрахеальная трубка. Однако после первого дня анестезиолог изменил протокол, чтобы всем собакам в асептических условиях устанавливали внутривенный головной катетер для облегчения внутривенного введения лекарственного средства и эндотрахеальную трубку, помещаемую для облегчения вентиляции с помощью мешка Амбу по мере необходимости. Вентиляция проводилась через мешок Амбу, если SpO 9.1018 2 < 91%. Всем пациентам, которые были недостаточно анестезированы до или во время операции, вводили альфаксалон (1,0 мг/кг). Кошкам вводили альфаксалон внутримышечно, тогда как собакам вводили альфаксалон внутривенно. Частота дыхания и SpO 2 оценивались у всех кошек перед началом операции, чтобы определить, требуется ли эндотрахеальная трубка (если SpO 2 < 91%). Все пациенты были регулярно выбриты и асептически подготовлены к операции. Все операции были выполнены DVM. Одновременно стерилизовали до 4 животных на отдельных столах на расстоянии не менее 2,5 м друг от друга. Каждый хирург определял, беременна ли пациентка, и эти данные записывались. Всем пациентам, у которых не было спонтанных движений после экстубации, вводили атипамезол. Любой собаке или кошке с признаками дисфории при выздоровлении вводили 0,01 мг/кг ацепромазина в/м или в/в по усмотрению анестезиолога. Все больные наблюдались до полного выздоровления (лежа на груди с поднятой головой). Для каждого пациента регистрировали время от инъекции анестетика до начала операции, продолжительность операции, общее время пациента (от инъекции анестетика до полного выздоровления) и восстановление ректальной температуры.
Все пациенты были регулярно выбриты и асептически подготовлены к операции. Все операции были выполнены DVM. Одновременно стерилизовали до 4 животных на отдельных столах на расстоянии не менее 2,5 м друг от друга. Каждый хирург определял, беременна ли пациентка, и эти данные записывались. Всем пациентам, у которых не было спонтанных движений после экстубации, вводили атипамезол. Любой собаке или кошке с признаками дисфории при выздоровлении вводили 0,01 мг/кг ацепромазина в/м или в/в по усмотрению анестезиолога. Все больные наблюдались до полного выздоровления (лежа на груди с поднятой головой). Для каждого пациента регистрировали время от инъекции анестетика до начала операции, продолжительность операции, общее время пациента (от инъекции анестетика до полного выздоровления) и восстановление ректальной температуры.
Доступность данных и материалов
Наборы данных, использованные и/или проанализированные в ходе текущего исследования, можно получить у соответствующего автора по обоснованному запросу.
Сокращения
- CF:
Кошка
- СМ:
Кот
- ДФ:
Самка собаки
- Прямая почта:
Кобель
- КВ:
Подкожный
- ОВХ:
Овариогистерэктомия
- МЧ:
Внутримышечно
- IV:
Внутривенно
- Отдел кадров:
Частота сердечных сокращений
- Запасной:
Частота дыхания
- SpO 2 %:
Насыщение гемоглобина кислородом
- Кол-во/комплект:
Фармакокинетика/фармакодинамика
- ДВМ:
Доктор ветеринарной медицины
- ЦНС:
Центральная нервная система
Ссылки
- «>
Looney AL, Bohling MW, Bushby PA, Howe LM, Griffin B, Levy JK, et al. Руководство по ветеринарной медицинской помощи Ассоциации ветеринаров приютов для программ стерилизации. J Am Vet Med Assoc. 2008;233(1):74–86.
Артикул Google ученый
Барнетт Б.Д. Искоренение и борьба с дикими и бродячими собаками на Галапагосских островах. Сборник материалов конференции по позвоночным вредителям. 1986;1:358–70.
Барнетт Б.Д., Радд Р.Л. Дикие собаки Галапагосских островов: воздействие и контроль. Int J Study Anim Probl. 1983;4(1):44–58.

Google ученый
Carrión PL, Valle CA. Рацион интродуцированных кошек на острове Сан-Кристобаль, Галапагосские острова: кошачьи фекалии как показатель хищничества кошек. Мамм биол. 2018;90:74–7.
Артикул Google ученый
Конечный МЮ. Ареал и характер активности диких домашних кошек на Галапагосских островах. Ойкос. 1987; 1:17–23.
Conservancy G. Isabela Island 2018. Доступно по адресу: https://www.galapagos.org/about_galapagos/about-galapagos/the-islands/isabela/.
Google ученый
Леви Дж., Бард К., Такер С., Дискант П., Дингман П. Периоперационная смертность кошек и собак, подвергшихся стерилизации или кастрации в крупной клинике. Вет Дж. 2017; 224:11–5.
КАС Статья Google ученый
«>Грабб Т.Л., Грин С.А., Перес Т.Е. Сердечно-сосудистые и респираторные эффекты, а также качество анестезии при внутримышечном введении альфаксалона кошкам, усыпленным дексмедетомидином и гидроморфоном. J Feline Med Surg. 2013;15(10):858–65.
Артикул Google ученый
Rodrigo-Mocholí D, Escudero E, Belda E, Laredo FG, Hernandis V, Marín P. Фармакокинетика и эффекты альфаксалона после внутривенного и внутримышечного введения кошкам. NZ Vet J. 2018;66(4):172–7.
Артикул Google ученый
Суарес М.А., Дзикити Б.Т., Стегманн Ф.Г., Хартман М. Сравнение альфаксалона и пропофола, вводимых в качестве тотальной внутривенной анестезии при овариогистерэктомии у собак.
 Ветеринар Анаест Аналг. 2012;39(3): 236–44.
Ветеринар Анаест Аналг. 2012;39(3): 236–44.КАС Статья Google ученый
Хасюк М.М., Браун Д., Куни С., Ганн М., Панг Д.С. Применение принципов ускоренной хирургии для оценки влияния атипамезола на выздоровление и обезболивание после овариогистерэктомии у кошек под анестезией дексмедетомидин-кетамином-гидроморфоном. J Am Vet Med Assoc. 2015;246(6):645–53.
КАС Статья Google ученый
Коппел Д., Бовилл Дж., Данди Дж. Приручение кетамина. Анестезия. 1973; 28 (3): 293–6.
КАС Статья Google ученый
Лин Х-К. В: Tranquilli WJ, Thurmon JC, Grimm KA, редакторы. Ветеринарная анестезия и обезболивание Ламба и Джонса. Эймс: Уайли Блэквелл; 2015.
Познер Л.П., Глид Р.Д., Эрб Х.Н., Луддерс Дж.В.
 Постанестетическая гипертермия у кошек. Ветеринар Анаест Аналг. 2007;34(1):40–7.
Постанестетическая гипертермия у кошек. Ветеринар Анаест Аналг. 2007;34(1):40–7.Артикул Google ученый
Феррер-Алладо Т., Брехнер В.Л., Даймонд А., Козен Х., Крэндалл П. Вызванные кетамином электросудорожные явления в лимбической и таламической областях человека. Анестезиология. 1973;38(4):333–44.
КАС Статья Google ученый
Griffin B, Bushby PA, McCobb E, White SC, Rigdon-Brestle YK, Appel LD, et al. Руководство Ассоциации ветеринаров приютов 2016 года по ветеринарной медицинской помощи для программ стерилизации. J Am Vet Med Assoc. 2016;249(2): 165–88.
Артикул Google ученый
Ко JC, Берман АГ. Анестезия в приюте. Вопросы медицины животных-компаньонов. 2010;25(2):92–7.
Артикул Google ученый
Ссылки на скачивание
Благодарности
Спасибо компаниям Jurox и Pfizer за предоставление альфаксалона и дексмедетомидина для этого проекта. Ни одна из компаний не участвовала в разработке, анализе или подготовке рукописи.
Выражаем благодарность сотрудникам Инициативы по межкультурному взаимодействию и Агентству по регулированию и контролю биобезопасности на Галапагосских островах (ABG) за их помощь в организации этого проекта, а также за обеспечение языкового перевода.
Авторы признательны Susan Baker, Veronica Brasiliero, Amy Butler DVM, David Edmiston DVM, Kristina Edmiston, Kent Passingham и Bernard Quiros за их помощь в уходе за животными и сборе данных.
Финансирование
Декларировать финансирование не требуется. Некоторые препараты, использованные в исследовании, были переданы в дар, но компании не участвовали в их использовании или подготовке рукописей.
Информация об авторе
Авторы и организации
Университет штата Северная Каролина, Колледж ветеринарной медицины, 1060 William Moore Drive, Raleigh, NC, 27606, USA
Lysa Pam Posner, Jeffrey Applegate, Diane Cannedy, Allen Cannedy Кристи Моззачио, Мария Серрано и Грегори Льюбарт
Авторы
- Lysa Pam Posner
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Jeffrey Applegate
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Allen Cannedy
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Diane Deresienski
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Kristie Mozzachio
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Maria Serrano
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Gregory Lewbart
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Contributions
Все авторы прочитали и одобрили рукопись. LPP: Старший автор; разработанное исследование; собранные данные, проанализированные данные, подготовленная рукопись, автор-корреспондент. JA: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. AC: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. ДД: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. КМ: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. MS: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. Г.Л.: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи.
LPP: Старший автор; разработанное исследование; собранные данные, проанализированные данные, подготовленная рукопись, автор-корреспондент. JA: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. AC: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. ДД: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. КМ: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. MS: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи. Г.Л.: Участвовал в разработке исследования, собирал данные, участвовал в подготовке рукописи.
Автор, ответственный за переписку
Переписка с Лиза Пэм Познер.
Декларация этики
Одобрение этики и согласие на участие
Эта рукопись не была одобрена комиссией по этике, поскольку она представляет собой ретроспективную оценку ветеринарной клинической практики (обычно используемые лекарства и часто выполняемые операции). Люди не являются субъектами, и разрешение на хирургическое вмешательство (не являющееся частью этого исследования) было дано с письменного согласия.
Люди не являются субъектами, и разрешение на хирургическое вмешательство (не являющееся частью этого исследования) было дано с письменного согласия.
Согласие на публикацию
Не применимо.
Конкурирующие интересы
Лиза Познер является редактором отдела BMC Veterinary Research.
Дополнительная информация
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате, при условии, что вы укажете соответствующую ссылку на оригинальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала.