Трихофития у кошек: лечение на разных стадиях
Когда в доме появляется домашний питомец, вместе с ним появляются дополнительные хлопоты, связанные с питанием, уходом и здоровьем животного. Маленький ласковый шерстяной комочек такое же живое существо со своими потребностями, характером и нравом. В основном, при своевременном проведении профилактических мероприятий, правильном питании и уходе не должно возникать проблем. Но если кот или кошка часто гуляют на улице и общаются с дворовыми животными, то могут возникнуть такие заболевания как трихофития или стригущий лишай.
Общие сведения
Трихофития – это грибковое заболевание, которое появляется в основном у животных, но также может перейти и на человека. Грибок быстро распространяется за счет огромного количества спор, при этом инфекция остается практически на всех поверхностях, где была зараженная кошка или кот. Несмотря на это, не каждое домашнее животное может подхватить такое заболевание.
Взрослые здоровые домашние питомцы, которые получают полный рацион, имеют профилактические вакцинации, защищены от трихофитии.
Носителями заболевания могут быть не только бродячие коты, но и собаки и большая часть мышевидных грызунов. Также споры трихофитии имеют высокую устойчивость к различным дезинфицирующим веществам, а также не поддаются воздействию на них различных температур. Поэтому они могут длительное время находиться в почве, на деревянных и тканевых предметах.
Первые признаки
Первые признаки заражения заметить сложно, особенно у длинношерстных и пушистых кошек. Они проявляются как сыпь или легкое покраснение на коже, которое в первое время питомец начинает почесывать. В основном заболевание проявляется уже на стадии выпадения волос.
Инкубационный период длятся от 1 недели до 1 месяца. На животных его практически зразу можно заметить. Он появляется в виде лысых пятен с покраснениями на коже, от этого и второе название заболевания стригущий лишай. В основном такие залысины появляются на голове животного и на шее, в редких случаях повреждаются конечности и хвост.
Если заболевание запущено, то пятна распространяются на все тело и через некоторое время объединяются. Животное лишается большой части шерстяного покрова. Также покраснения покрываются коркой, под которой начинается нагноение волосяных луковиц и накапливается гной. В основном при этом заболевании зуд отсутствует.
Лечение трихофитии у кошек при легком заражении
При обнаружении непонятной сыпи или открытых пятен на коже без шерсти необходимо немедленно обратиться к ветеринару. Специалист при помощи анализов и соскобов определит заболевание и его стадию. Это поможет назначить правильное лечение и определить инкубационный период и стадию заражения.
При появлении у питомца трихофитии лечение длится около 2 месяцев. Причиной этому является высокая выживаемость споров грибков, которые вызывают это заболевание. При раннем обнаружении заболевания используются противогрибковые средства, такие как спрей, шампунь, мазь. Ветеринары рекомендуют миконазол, этот препарат при регулярном использовании имеет хороший эффект. Также похожими свойствами обладает мазь тиабендазол.
Лечение трихофитии у кошек в запущенном виде
Если животное имеет запущенное грибковое заболевание, то к средствам внешнего использования прописывают препараты для внутреннего лечения. При анализах и диагностики ветеринар самостоятельно определяет и прописывает курс лечения с необходимыми дозировками лекарствами.
Параллельно с лечение в доме, где проживает зараженное животное, должна регулярно проводиться дезинфицирующая обработка и влажная уборка. Все предметы, с которыми соприкасается питомец необходимо протирать раствором хлора. Если в доме есть другие животные, их необходимо проверить на заболевание и вакцинировать или провести профилактические работы.
Лечение должно проходить с регулярными консультациями у ветеринара. Особенно это важно при использовании антибиотиков и других лекарств, которые применяются внутрь. Также необходимо соблюдать режим питания и питомец должен получать все необходимые витамины, минералы и микроэлементы для скорейшего восстановления организма.
Лечение в домашних условиях
Бывают случаи, когда нет возможности обратиться к ветеринару и лечение приходится проводить самостоятельно, испытывая дедовские методы. В давние времена люди самостоятельно решали подобные проблемы. Для этого использовался йод и смесь растительного масла с золой. Дезинфицирующим средством, в этом случае йодом, обрабатывались все пораженные места. А кашица с золой и йодом налаживалась как компресс. Такие процедуры проводились 5-7 раз за день.
Для приготовления золы использовались газеты, ветки смородины или малины. Полученный пепел перемешивался с любым растительным маслом, которое есть в доме. Должна получиться кашеобразная смесь.
При любом способе лечения рекомендуется убрать шерсть у пораженных участков. Особенно это важно для пушистых и длинношерстных котов и кошек. В некоторых случаях рекомендуется животное полностью остричь, чтобы не пропустить зараженные участки кожи с красной сыпью.
Профилактические действия
Одним из главных способов уберечь домашнее животное от заболевания трихофитии, это оградить его от общения с уличными животными. Своевременная вакцинация и регулярное посещение ветеринара, также поможет сохранить здоровье питомца и при заражении выявить проблемы на ранних стадиях.
В основном такой болезни подвержены коты и кошки со слабым иммунитетом. Необходимо следить, чтобы домашний питомец получал вместе с питанием все необходимые вещества для здоровой жизнедеятельности. Питание можно подбирать специальное или готовить натуральную пищу с добавлением витаминов по рекомендации ветеринара.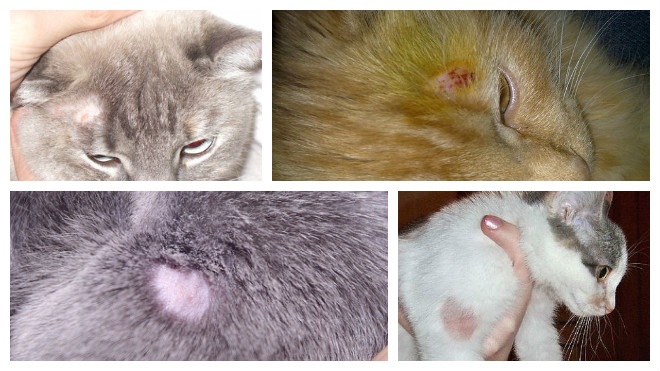
Место постоянной игры и сна животного должно находиться в порядке. В доме рекомендуется регулярно проводить влажную уборку и периодически обрабатывать поверхности дезинфицирующими средствами.
Рубрики: Болезни кошек |
автор admin
Как вылечить лишай у котенка в домашних условиях народными средствами
Если хозяин обнаружил у домашнего животного залысины на теле, возможно, это стригущий лишай. Если в ветеринарной клинике подтверждают, что это грибковое заболевание, то можно попробовать самостоятельно лечить лишай у кошек, лечение в домашних условиях и забота быстро избавит питомца от болезни.
Признаки заражения
Первые признаки данного инфекционного заболевания могут проявляться в виде красных пятнышек, которые кошка интенсивно и часто чешет. Через некоторое время красные пятна покрываются пузырьками, содержащими экссудативную жидкость.
Если лечение вовремя не начато, то пузырьки при расчесывании лопаются, в них попадает инфекция и образуются гнойники.
Шерстинки в этих местах начинает выпадать частично или полностью. Если шерсть у питомца длинная, то залысины трудно заметить. Но внимательные хозяева заметят беспокойное поведение кошки, она отказывается от еды, злится и постоянно чешется.
У животных с сильным иммунитетом залысины почти не видны, волоски только частично обламываются.
Что должны сделать хозяева больных животных
Обнаружив симптомы стригущего лишая, хозяевам необходимо как можно быстрее обратиться к ветеринару, чтобы он поставил точный диагноз и назначил необходимое лечение. Грибок заразен для человека, и самолечение может привести не только к ухудшению здоровья питомцев, но и к заражению хозяев.
Больное животное рекомендуется изолировать от контактов с членами семьи, чтобы споры не распространялись по всей квартире. Необходимо провести влажную уборку всего помещения, где находилось больное животное, применяя при этом дезинфицирующие средства.
Необходимо провести влажную уборку всего помещения, где находилось больное животное, применяя при этом дезинфицирующие средства.
Зараженные участки тела надо обрить или обстричь шерсть ножницами и сжечь, инструменты после этой процедуры обязательно надо продезинфицировать.
Трихофития (стригущий лишай) может развиваться в течение нескольких дней. При запущенном заболевании у животного поражаются кожные и лимфатические ткани с последующим воздействием на головной мозг.
Своевременное обращение в ветеринарную клинику и тщательное выполнение всех рекомендаций специалиста позволит быстро вылечить питомца.
Домашние способы лечения лишая
Если дорогостоящие лекарственные препараты хозяевам не доступны, то для лечения лишая на начальной стадии можно попробовать эффективные народные средства. 1 раз в день можно обрабатывать розовое пятнышко на теле котенка смесью древесной золы и растительного масла. Ранку предварительно смазывают раствором йода.
Для лечения стригущего лишая у животного и у человека можно использовать еще одно средство.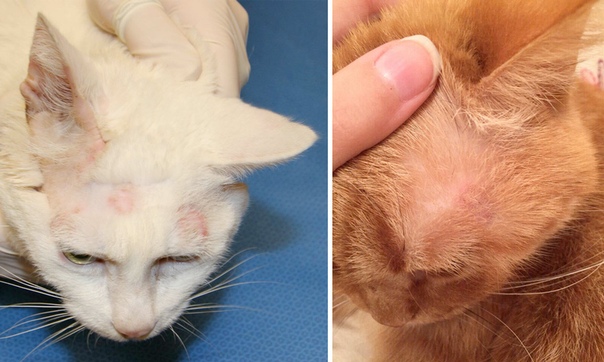 В емкости смешивают по 1 ч. л. 5%-ого раствора йода, валерианы и растительного масла. Полученной смесью смазывают пораженные участки тела 3 раза в день.
В емкости смешивают по 1 ч. л. 5%-ого раствора йода, валерианы и растительного масла. Полученной смесью смазывают пораженные участки тела 3 раза в день.
Можно приготовить раствор из спирта и ацетилсалициловой кислоты. В пузырек с 30 мл спирта добавляют 1 измельченную в порошок таблетку и тщательно его взбалтывают. Полученный раствор с помощью ватной палочки аккуратно наносят на пораженные участки кожи до 7 раз в день. Корочки на ранке нельзя снимать, они должны сами отпадать.
Хорошо помогает в борьбе с лишаем свежевыжатый сок чистотела, который втирается в пораженные участки до 5 раз в день. Можно смешать в равных частях оливковое масло и лимонный сок. Полученной смесью смачивают ватный тампон и прикладывают его к пораженному месту до 4 раз в день.
Процесс выздоровления будет зависеть от иммунитета животного. Если у животного появляется аллергическая реакция, то данное лечение следует прекратить. Если ни один способ народной медицины не помогает и болезнь прогрессирует, необходимо срочно обратиться к ветеринару.
Что назначают ветеринары
Для лечения лишая у кошек ветеринары назначают такие лекарственные средства, как мази, спреи, эмульсии и шампуни. Если заболевание запущено и наружные средства не помогают, врач может назначить таблетки и уколы. Эти препараты токсичны и могут нанести вред печени животного, поэтому их применяют только по назначению и под наблюдением специалиста.
Среди мазей, которые продаются в специализированных магазинах, можно выделить:
- серная мазь;
- салициловая мазь;
- Микозон;
- Клотримазол;
- Микосептин;
- Санодерм.
Среди растворов популярностью пользуются Фукорицин и Имаверол, их используют до полного выздоровления. Для купания животных в период лечения можно применять шампуни Себозол и Низорал.
Как правильно обрабатывать животное и давать различные лекарства
Чтобы лечение домашнего животного прошло эффективно и выздоровление наступило быстро, хозяева должны научиться правильно использовать препараты. Перед применением необходимо изучить инструкцию, которая прилагается к медикаментам, и строго ей следовать.
Таблетки, капсулы
Чтобы дать кошке таблетку или капсулу, потребуется обмотать животное пеленкой или полотенцем (голова при этом должна быть снаружи), чтобы оно не поцарапало хозяина.
Ограничив движение кошки, одной рукой аккуратно надавливают на пасть, чтобы она открылась.
Наглядный пример как дать таблетку кошке.
Другой рукой забрасывают таблетку в рот, стараясь попасть на заднюю часть языка. Затем надо убедиться, что кошка проглотила таблетку. После этого надо дать животному попить и поесть, чтобы лекарство легче прошло по пищеводу к желудку.
Способ кормления кота таблеткой с помощью шприца.
Можно спрятать небольшую таблетку во влажный кошачий корм, который животное любит больше всего. Для этого надо, чтобы кошка сильно проголодалась. Таблетку прячут в ¼ части порции и дают корм животному. Когда тарелка будет пустой, туда добавляют остатки еды.
Вакцины и любые инъекции
Противогрибковые вакцины можно применять только через 10 дней после дегельминтизации животного. Вакцинацию запрещено проводить беременным и кормящим кошкам, а также котятам младше 2 месяцев. Вакцина вводится по специальной схеме, повторная вакцинация разрешена после двухнедельного перерыва.
Если хозяин будет делать инъекции самостоятельно, то надо соблюдать некоторые правила. Перед процедурой обязательно тщательно моют руки с мылом. К игле шприца после того, как с нее снят колпачок, притрагиваться нельзя. Укол ставится только в то место, которое укажет ветеринар. Лекарство набирают в шприц и выпускают из него воздух до появления на игле первых капель.
Кожу животного оттягивают в складку, шприц располагают под углом 45˚, прокалывают кожу и выпускают лекарство. После извлечения иглы место укола надо легко погладить, а затем кошку отпускают. Если на месте укола появится шишка или питомец будет себя беспокойно вести, то следует срочно обратиться к врачу.
Шампуни
Шампуни используют в комплексном лечении стригущего лишая. Кошку рекомендуется купать 2 раза в неделю, курс лечения может длиться до 1,5 месяцев. При незначительном заражении купание может дать обратный эффект, споры будут распространяться на здоровые участки тела. Шампуни с противогрибковым эффектом назначают при генерализованной форме заболевания.
Купать кошку следует осторожно, чтобы не допустить побочных эффектов. Шампунь наносят на животное и выдерживают до 15 минут (время указано в инструкции к средству). Полученную пену тщательно смывают большим количеством теплой воды. После процедуры ванну следует помыть с дезинфицирующим средством.
Полученную пену тщательно смывают большим количеством теплой воды. После процедуры ванну следует помыть с дезинфицирующим средством.
Мази, гели, спреи
Лечебные мази, спреи и гели обладают противогрибковыми свойствами и способствуют быстрому восстановлению эпидермиса. Мазь или гель следует наносить на пораженную область тонким слоем, захватывая при этом здоровую кожу примерно на 3 см.
Если лишай находится на голове, то надо следить, чтобы крем не попал в глаза. Применяют мази до 2 раз в день, курс лечения может длиться до 10 дней.
Еще одним эффективным средством, особенно на ранней стадии заболевания, являются спреи, например Фунгин или Биопирокс. Аэрозолем обрабатывают пораженные места на коже до 4 раз в день с перерывом 3 дня.
Флакон предварительно встряхивают, распыление средства производят на расстоянии не менее 20 см от места воспаления в течение 3 секунд. Курс лечения ветеринар назначает индивидуально.
Курс лечения ветеринар назначает индивидуально.
Чтобы кошка не слизывала лекарственный препарат, на нее надевают намордник или специальный воротник.
Как можно оценить эффективность лечения
Через какое время наступит выздоровление, врач не может сказать, сложность в том, что из-за шерсти споры могут долго находиться на теле. Процесс выздоровления зависит от состояния питомца, от площади заражения, от качества содержания и соблюдения гигиены и от своевременного лечения.
Первым признаком выздоровления можно считать исчезновение воспаления, красноты и припухлости. Корочки подсыхают и постепенно отпадают. Обновленная шерсть может появиться через 1,5 месяца. Животное ведет себя спокойно и выглядит здоровым.
Чтобы заражение грибком не повторилось, следует оберегать своего питомца от общения с больными животными. Места обитания животного в квартире следует содержать в чистоте.
Места обитания животного в квартире следует содержать в чистоте.
Повышать иммунитет кошки необходимо с помощью рационального питания и витаминов. Для профилактики раз в год необходимо проводить вакцинацию, ветеринары для этого используют препараты Вакдерм или Микродерм.
Трихофития Котов Народное Лечение — О Животных на чистоту
Трихофития у кота лечение
Только зарегистрированные пользователи имеют возможность начинать новые темы. Зарегистрируйтесь и войдите на сайт, введя свои логин и пароль справа в окне, и Вы сможете начать новую тему.
Прежде чем задать вопрос на форуме, ознакомьтесь с темой: «Как правильно задать вопрос вет.врачу», а также со списком ответов на часто задаваемые вопросы, это поможет Вам сэкономить Ваше время и быстрее получить ответ на Ваш вопрос.
Обратите особое внимание на документ: Симптомы заболеваний животных. Возможно, в Вашей ситуации нельзя ожидать ответа на форуме, а нужно срочно вызывать врача или везти животное в ветеринарную клинику!
Прежде чем задать вопрос на форуме, ознакомьтесь со следующими разделами, это поможет сэкономить Ваше время и быстрее получить отсвет на ваш вопрос:
Внимание! Обратите особое внимание на документ «Симптомы заболеваний животных». Возможно, в Вашей ситуации нельзя ожидать ответа на форуме, а нужно срочно вызывать врача или везти животное в ветеринарную клинику!
Возможно, в Вашей ситуации нельзя ожидать ответа на форуме, а нужно срочно вызывать врача или везти животное в ветеринарную клинику!
Только зарегистрированные пользователи имеют возможность начинать новые темы. Зарегистрируйтесь и войдите на сайт, введя свои логин и пароль справа в окне, и Вы сможете начать новую тему.
Советы от ветеринара: чем лечить лишай у кошки и не допустить заражения домочадцев
С вопросом, чем лечить лишай у кошки, владелец сталкивается, как правило, после того, как у питомца обнаружат это неприятное заболевание. Опасность заключается в том, что он может передаваться от животного человеку. Поэтому комплексный подход в терапии кожной инфекции позволит существенно сократить срок лечения питомца и снизит риск заражения домочадцев.
Читайте в этой статье
Виды кожной инфекции
Лишай домашних животных – распространенное заболевание кожных покровов, некоторые формы которого представляют опасность и для человека.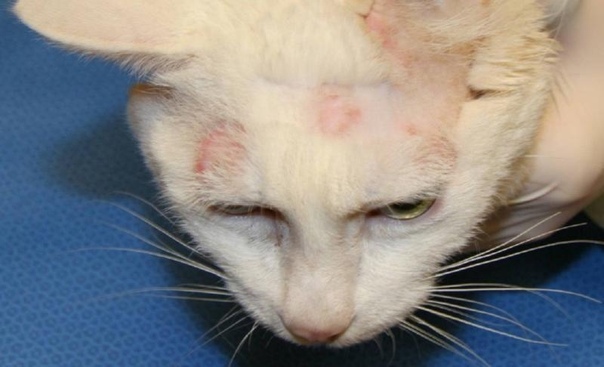 Заражение грибками-дерматофитами происходит чаще всего при контакте с больным животным, предметами обихода. Домашние питомцы заражаются, как правило, при общении с бродячими уличными животными, от грызунов.
Заражение грибками-дерматофитами происходит чаще всего при контакте с больным животным, предметами обихода. Домашние питомцы заражаются, как правило, при общении с бродячими уличными животными, от грызунов.
Существует множество разновидностей кожной инфекции. Они отличаются по виду возбудителя, заразности, клиническим симптомам. Кошки подвергнуты разным формам заболевания.
| Виды лишая | Особенности | Проявления на животном |
| Стригущий лишай (трихофития, микроспория, кошачий лишай) | Самая распространенная форма заболевания, вызываемая грибками Trichophyton и Microsporum, долго сохраняющими свою патогенность в окружающей среде. Данный вид заразен для человека и наибольшую опасность представляет для детей | |
| Отрубевидный лишай | Вирусная инфекция, заразная как для других животных, так и для человека | |
| Розовый лишай | Вирусная форма патологии, не опасна для человека, но заразна для других животных | |
| Красный плоский лишай | Является причиной сбоя иммунной системы и относится к незаразным формам | |
| Мокнущий лишай (экзема) | Эта форма аллергического заболевания, не представляющая опасности для человека |
Вылечить лишай можно только при условии правильно поставленного диагноза и эффективной комплексной терапии. Поэтому при обнаружении первых признаков заболевания у питомца владелец должен посетить ветеринарного специалиста с целью установления его формы. Регулярный профилактический осмотр кожного покрова животного позволит заметить первые симптомы заболевания.
Поэтому при обнаружении первых признаков заболевания у питомца владелец должен посетить ветеринарного специалиста с целью установления его формы. Регулярный профилактический осмотр кожного покрова животного позволит заметить первые симптомы заболевания.
Клинические проявления
Перед тем, как лечить лишай у кошек, необходимо понять, какой именно его вид у питомца. Каждая форма кожной инфекции имеет свои особенности клинической картины.
Заметить первые симптомы заболевания владелец может при регулярном осмотре кожного покрова домашней кошки. При лишае происходит поражение волосяных луковиц и клинически это выражается в появлении участков кожи без волос. Насторожить владельца должно внезапное выпадение шерсти. При лишае чаще всего такое явление наблюдается в области головы, шеи и конечностей.
Потеря шерсти приводит к облысению участка кожи, появлению алопеций. Очаги облысения со временем приобретают малопривлекательный вид. Все формы заболевания развиваются довольно быстро, общим признаком является появление на коже маленького сероватого или бледно-розового пятна. Кошку беспокоит зуд, она часто чешется.
Кошку беспокоит зуд, она часто чешется.
Стригущий лишай
Наиболее распространенный стригущий лишай характеризуется округлыми и овальными очагами облысения, кожа при этом шелушится и покрывается чешуйками. Животное расчесывает пораженные участки, что сопровождается кровоточивостью. Нарушение целостности кожного покрова приводит к проникновению бактерий и инфицированию участков кожи. Она становится сальной, сильно шелушится, появляются чешуйчатые и ороговевшие образования. С течением времени повреждения становятся бугристыми с ярко выраженными контурами. Владельцу животного следует знать, что лечить стригущий лишай труднее всего.
Отрубевидная форма отличается наличием желто-коричневого пятнышка без четких границ с явлениями воспаления. Пигментация облысевшего участка кожи становится бледно-розовой, желтоватой или коричневой.
При розовом лишае участки алопеций на голове животного имеют округлую форму размером 1,5 — 2 см. При локализации очагов облысения на шее и спине их форма может быть вытянутой. Самый первый очаг (материнская бляшка) с течением времени становится желтоватого цвета. Животное сильно беспокоит зуд.
Самый первый очаг (материнская бляшка) с течением времени становится желтоватого цвета. Животное сильно беспокоит зуд.
Красный плоский лишай характеризуется наличием красных пузырьков на безволосых участках кожи, а также в ротовой полости. Пузырьки лопаются при расчесывании и вызывают еще большее раздражение.
Сильный зуд и жжение вызывает мокнущий лишай, первым признаком которого является покраснение и появление пузырьков.
Диагностика заболевания
Эффективность лечения зависит в первую очередь от правильной диагностики формы заболевания. Если владелец заподозрил у кошки лишай, что делать в таком случае: следует ее как можно раньше показать ветеринарному специалисту.
После клинического осмотра кожный покров питомца просвечивают специальной лампой Вуда. Под действием ее света грибковые колонии флуоресцируют (светятся ярко-зеленым цветом). Данный метод не всегда информативен, так как некоторые непатогенные споры грибков также реагируют свечением на ультрафиолетовый свет.
Правильная диагностика в амбулаторных условиях позволит подобрать наиболее эффективные лекарственные средства, так как вывести лишай у кошки – задача непростая. Поэтому современная ветеринария подходит к вопросу диагностики комплексно.
Более достоверные способы определения заболевания – микроскопическое исследование и посев возбудителя на питательную среду с последующей его идентификацией. Лишай дифференцируют от дерматитов, аллергии, пиодермии.
Лечение заболевания
Когда встает вопрос после обследования, чем лечить лишай у кота, то ответ будет зависеть от ряда факторов: стадии, интенсивности заражения, состояния иммунитета животного. В терапии применяются разнообразные по форме и действию ветеринарные препараты и средства. В комплексном лечении используют:
- Вакцины. “Микродерм”, “Поливак ТМ”, “Вакдерм F” обладают не только профилактическим эффектом, но и лечебным при применении их в начальной стадии заболевания. Вакцина вводится по определенной схеме (2 — 3 раза с интервалом 10 — 14 дней) в лечебной дозе.

- Местное лечение. Обработать лишай можно наружными средствами. Перед их применением шерстный покров нужно коротко срезать или побрить, собранную шерсть при этом необходимо сжечь. Больным животным применяют специальные шампуни против грибков, мази, растворы. Очаги поражения обрабатывают 10%-ным раствором салицилового спирта, 4%-ным раствором хлоргексидина, 5%-ным раствором однохлористого йода.
Среди разнообразия противогрибковых мазей легко растеряться. Чем мазать лишай у кошки? Наиболее эффективными противогрибковыми мазями являются: “Фунгин”, “ЯМ БК”, “Санодерм”, “Тиабендазол”, “Миконазол”, “Низорал” и т.д.
- Оральные препараты. Применяются при неэффективности наружных противогрибковых средств, в случае заражения обширных участков кожи и когтей. Гризеовульфин, тербафин, итраконазол – специальные противогрибковые антибиотики, направленные на подавление инфекции и регенерацию поврежденных тканей.
 Препараты имеют ряд побочных действий, с осторожностью применяются у беременных самок.
Препараты имеют ряд побочных действий, с осторожностью применяются у беременных самок.
Ветеринарные специалисты не рекомендуют лечить лишай у кошки народными средствами, так как они неэффективны.
Если наблюдается гнойный дерматит из-за инфицирования очагов поражения, то животному назначаются антимикробные препараты. Кроме того, комплексная терапия такого сложного заболевания включает применение иммуномодуляторов, витаминов. Необходимо на весь курс лечения обеспечить животное полноценным питанием.
О том, чем и как лечить лишай у кошек, смотрите в этом видео:
Дезинфекция и профилактика
Особое место в терапии заболевания занимают мероприятия по дезинфекции помещения и предметов обихода. Избавиться от лишая, применяя только препараты для лечения животного, практически невозможно. Высокую активность спор грибка и его сохранность в окружающей среде следует учитывать при выборе антисептических средств.
Прежде всего на весь период лечения необходимо свести к минимуму контакт с животным. Все манипуляции следует проводить в перчатках. После чего тщательно вымыть руки с мылом, обработать хлоргексидином.
На протяжении всего времени, сколько лечится лишай у кошки, следует проводить регулярную уборку помещения с применением пылесоса для удаления волос и частичек кожи животного. Содержимое мешка после каждой уборки необходимо сжечь.
Для обработки предметов обихода, средств по уходу за животным следует применять противогрибковые вещества, например, “Энилконазол”, “Бланидас”, “Виркон-С”. Для мытья полов и других поверхностей подойдут обычные дезинфицирующие вещества, в том числе хлорка. Подстилку периодически меняют, сжигая старую или замачивая ее в дезинфицирующих растворах.
При обнаружении заболевания у питомца владелец должен знать, что эффективно лечить лишай у кошки в домашних условиях можно.
Терапия потребует комплексного подхода и соблюдения мер предосторожности.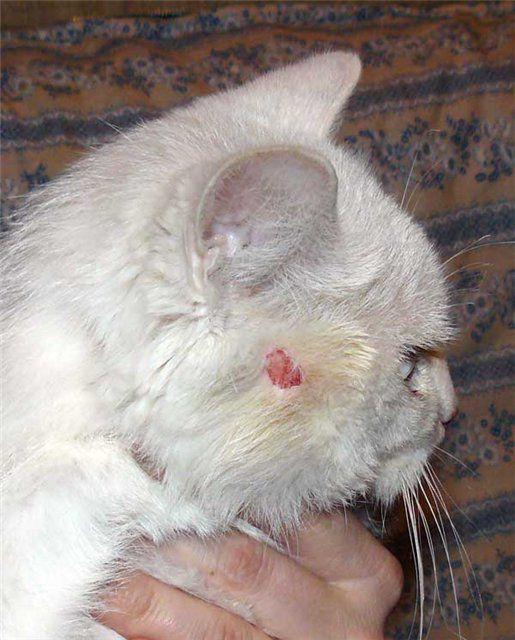
Сильный зуд и жжение вызывает мокнущий лишай, первым признаком которого является покраснение и появление пузырьков.
Трихофития (стригущий лишай) у собак: причины развития болезни, основные симптомы, способы лечения.
Трихофития (более распространенное название – стригущий лишай) – это кожная болезнь, развитие которой вызывают споры патогенных грибков. Заболевание опасно не только для питомцев, но и для их владельцев. Каковы симптомы трихофитии? Возможно ли ее вылечить?
Причины развития заболевания
Возбудителями трихофитии (или стригущего лишая) являются грибки, которые относятся к роду Trichophyton (у собак развитие болезни вызывают Tr. Gypseum). Их споры могут быть где угодно: на подстилке, в почве, на коже зараженного животного, в навозе и т. д. Они попадают на кожу питомца и начинают размножаться, приводя к развитию трихофитии.
Грибки способны сохраняться до 10 лет в волосах; в жиже и фекалиях – до 8 месяцев. В почве они живут до 140 дней, но погибают под воздействием ультрафиолета и сухого жара. В кипящей жидкости грибки гибнут уже через пару минут. Уничтожить возбудителей можно растворами щелочи (1-3%), карболовой кислоты (2-5%) и салициловой к-ты (1-2%).
В почве они живут до 140 дней, но погибают под воздействием ультрафиолета и сухого жара. В кипящей жидкости грибки гибнут уже через пару минут. Уничтожить возбудителей можно растворами щелочи (1-3%), карболовой кислоты (2-5%) и салициловой к-ты (1-2%).
Грибок особенно опасен для ослабленных и пожилых собак. К благоприятным факторам относят:
- наличие на коже царапин и ранок;
- ослабленный иммунитет;
- наличие кожных болезне
Трихофития у кошек
Трихофития у кошек или стригущий лишай — это грибковое заболевание, которое является разновидностью лишая. Болезнь характеризуется образованием на коже животного облысевших участков с гнойным фолликулитом и экссудативным дерматитом.
Трихофитией может заболеть и человек.
Грибки рода Trichophiton поражают кошек, вызывая у них эту страшную болезнь. Паразиты имеют неразветвленное тело нитчатого типа с огромным количеством спор. Это и объясняет широкое распространение этого заболевания.
Возбудитель обладает значительной жизнестойкостью. Он нормально переносит различные температуры окружающей среды и дезинфицирующие вещества. В почве, на подстилках и на деревянных предметах споры грибка способны сохраняться долгое время.
Носителями грибка являются крысы, мыши и другие грызуны. Трихофития или стригущий лишай у бродячих кошек возникает чаще, чем у домашних. Это обусловлено образом жизни. Если не уделять должного внимания уходу за домашним питомцем, он легко может заразиться.
Этиология трихофитии
В зоне риска обычно находятся котята, животные с ослабленным иммунитетом и плохо питающиеся кошки. Болезнь передается кошкам от других животных, путем попадания спор в поврежденные участки кожи. У некоторых кошек болезнь протекает без проявления симптомов, это делает заболевание еще более опасным.
От недели до месяца длится инкубационный период. Поражение чаще всего начинается с головы, конечностей и шеи. В запущенных случаях пятна захватывают практически все тело. Зуд отсутствует, но может возникнуть нагноение под засохшей коркой. Стригущий лишай поражает не только кожу, а еще и ногти. Заболевание легко спутать с микроспорией у кошек.
В запущенных случаях пятна захватывают практически все тело. Зуд отсутствует, но может возникнуть нагноение под засохшей коркой. Стригущий лишай поражает не только кожу, а еще и ногти. Заболевание легко спутать с микроспорией у кошек.
Лечение трихофитии у кошек
Определить какой именно грибок вызвал эту болезнь самостоятельно практически невозможно, поэтому диагноз должен поставить ветеринар, основываясь на лабораторные исследования. Пораженных мест врач должен облучить ультрафиолетовом и взять соскоб кожи. Чтобы избавить животное от стригущего лишая при локальном поражении нужно состричь пораженную шерсть и очистить кожу от корки, смочим ее раствором бетадина.
Пораженные участки следует ежедневно обрабатывать фунгистатической мазью, кремом или раствором. Если на коже присутствуют нагноения, животному необходимо пропить курс антибиотиков. Внутрь назначают фульвицин.
Для лечебных и профилактических целей в современной ветеринарной медицине используют специальные вакцины.
Профилактика трихофитии у кошек
Для профилактики стригущего лишая проводятся санитарнo-гигиенические мероприятия и вакцинация животных.
Предметы, с которыми контактирует кошка, обрабатываются слабым раствором хлора или гипохлорита натрия. Ковры в доме нужно еженедельно пылесосить, чтобы удалить зараженные волоски.
Стригущий Лишай У Кошек Симптомы Лечение Фото Первый День
Автор Дарья Ветеринар На чтение 40 мин. Просмотров 1 Опубликовано
Лишай у кошек — лечение и профилактика
С давних времен кошки своим появлением в доме несут пользу человеку. Они могут ловить мелких грызунов или своей лаской утешить и поднять настроение хозяину. Но бывает так, что усатым питомцам необходима помощь человека в лечении болезней. Одним из таких недугов является лишай у кошек. Что же он из себя представляет и как с ним бороться рассмотрим далее.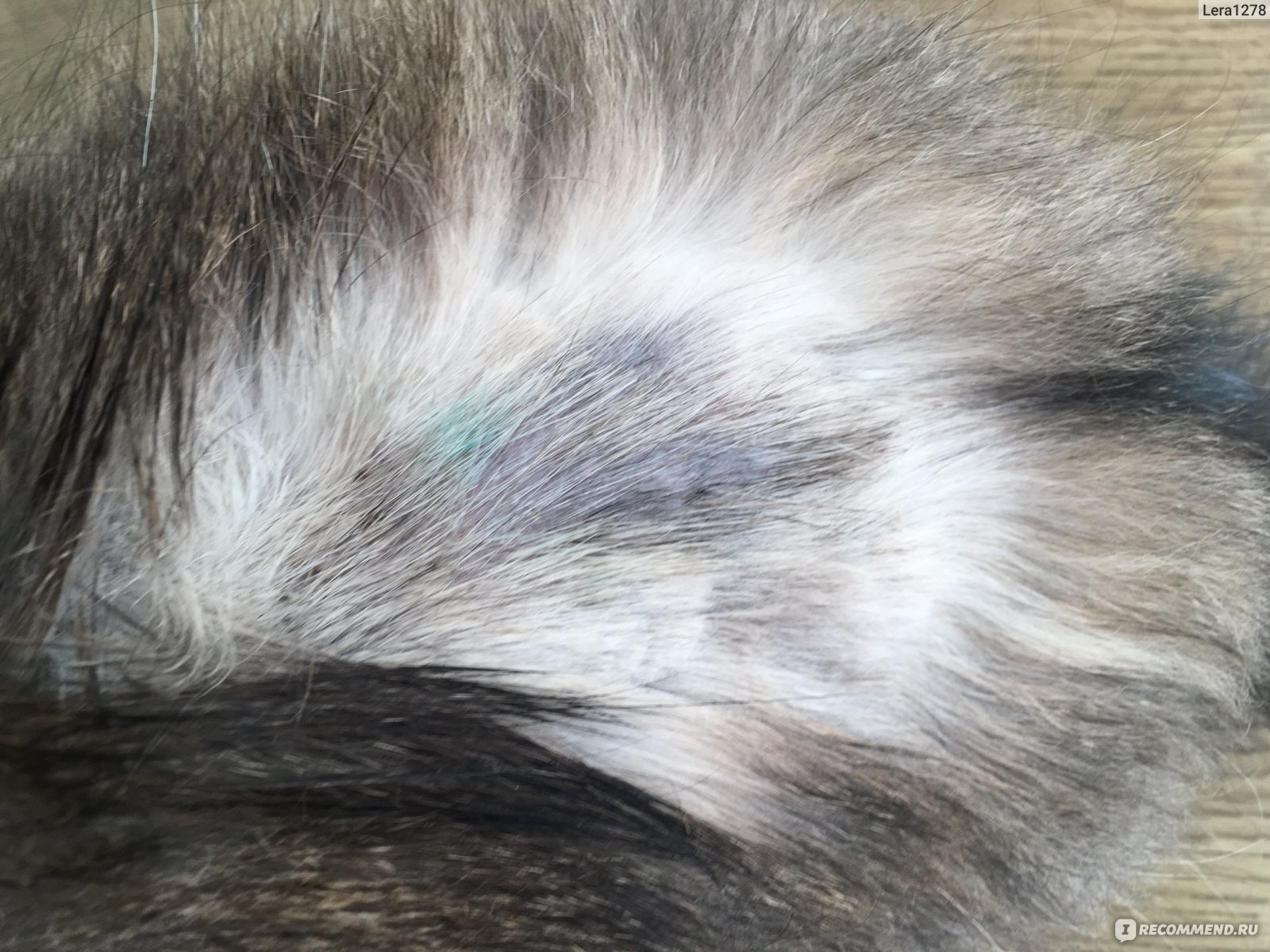
Разновидности кошачьего лишая с фото
Лишай – дерматологическое заболевание, вызванное различными грибками или вирусами. У кошек он выступает на коже, шерсти или когтях, а его виды имеют разные варианты появления.
Когда споры грибка попадают в организм домашних животных, скрытый период (инкубационный) продолжается от нескольких дней до месяца, затем начинается наружное проявления кошачьего лишая, выделяющегося в первую очередь выпадением шерсти на кожных покровах. Среди кошачьих видов встречаются следующие:
Плоский красный лишай
Появляется при сбое иммунной системы животного. Причины его возникновения не известны, другим особям не передается. Характерен зудящими красными пузырьками с жидкостью на коже или слизистых оболочках. При расчесывании прыщики лопаются, вызывая больший зуд.
Розовый лишай
Передается вирусным путем от одного животного к другому. Встречается данный вид лишая у котят и взрослых особей, но проходит самостоятельно при укреплении иммунитета. Выглядит как розовое пятно размером от 1,5 до 2 см, поверхность которого шелушится и чешется.
Мокнущий лишай (экзема)
Иногда сопровождается вместе с грибковыми инфекциями. Имеет вид воспаленных красноватых пятен с пузырьками, а также сильный зуд. При расчесывании прыщей зуд становится еще сильнее. Не является заразным для других животных.
Отрубевидный лишай (разноцветный)
Возникает от грибковой инфекции. Популярен в странах с жарким климатом, распространяется быстро и незаметно. Имеет вид небольших желто-коричневых пятен, без особого воспаления.
Стригущий лишай
Самый встречаемый и опасный лишай у котов и кошек. Далее о нем и пойдет речь.
Как распознать стригущий лишай
Стригущий лишай у кошек происходит от таких видов грибков как Trichophyton, Microsporum gypseum и Microsporum canis. Первый вид провоцирует болезнь, именуемую трихофитией, а второй и третий вид – микроспорией. В двух данных заболеваниях симптомы очень похожи. Распознать их можно только в лабораторных условиях.
Грибки способны существовать как на зараженном животном, так и на участках его пребывания. Размножение грибков происходит благодаря спорам, жизнеспособность которых достигает двух лет. Отлично размножаются в условиях тепла и влаги.
Кроме того, споры могут находиться долгий период на мебели, ковре или выпавших волосках больной кошки, а потом стать причиной заражения следующего животного.
Стригущий лишай у кошки вокруг глаза
При стригущем лишае у кошки повреждаются участки на коже, шерсти или когтях. Чаще всего лишай начинает свое распространение с морды кошки, ее лап, затем переходит на уши, живот, спину, хвост. Главные его симптомы:
- Полысевшие пятна круглой или овальной формы.
- Воспаленная кожа в местах поражения.
- Частое чесание кошки в местах появления лишая.
- Появление жирных на ощупь корочек, похожих на перхоть.
- Изредка бывают прыщики.
При первых симптомах стригущего лишая на кошке появляются пятна размером от 1 см. Если не заметить распространение болезни, они быстро расползутся по всему телу домашнего питомца. Сам грибок имеет способность существовать годами на животном, а вылечить одним махом не получится. Так что стоит внимательно отнестись к проблеме при первых проявлениях лишая у кошки.
Кто подвержен заболеванию
По статистике к заболеванию лишаем склоны кошки с нарушенным иммунитетом, в том числе особи, которые переживают период другой болезни или ослаблены.
Также быстрое инфицирование грибком лишая происходит у старых кошек и котят, животные с длинной шерстью тоже попадают в категорию быстрого подхвата заболевания.
Часто обнаруживается лишай у породистых кошек, например, персидских, так как они выведены искусственно и не имеют природного иммунитета от данного заболевания.
Некоторые кошки могут быть только переносчиками лишая. То есть происходит инфицирование лишаем, но болезнь не начинается. А когда такой питомец начнет контактировать с другими животными, они могут подхватить заболевание.
Диагностика стригущего лишая
Обычно видимые признаки лишая у кошек сложно определить с первого взгляда. Популярным способом определения болезни станет использование флуоресцентной лампы, ее еще называют лампа Вуда. В темном помещение включается лампа и светиться на любимого питомца.
Если на кошке есть лишай, свечение будет кислотно-зеленого цвета. Но эффективность данного метода работает с точностью до 60%. Это связано с тем, что не все грибки отсвечивают, а само животное может не болеть, а лишь переносить на своей шерсти лишай.
Лучшим способом узнать, что происходит с кошкой, будет поход к ветеринару. Именно специалист сможет с помощью исследований определить вид заболевания усатого питомца.
Врач соберет с кошки образцы грибка, это могут быть корочки или чешуйки с лишайного пятна. В некоторых случаях делается анализ крови животного. Кроме того, специалист вовремя обнаружит прочие болезни.
Если одновременно с лишаем кошка инфицирована другими вирусами или паразитами, то увеличивается риск ухудшения кошачьего здоровья.
Поэтому пушистых любимцев нужно лечить, тем более что кошачий лишай проявляется у человека тоже. Больше всего от него страдают дети и взрослые со слабым иммунитетом.
[attention type=green]В случае обнаружения лишайных пятен на теле или голове человека следует немедленно обратить за помощью к дерматологу.[/attention]
Откуда идет заражение
Заразится лишаем кошка может где угодно. В первую очередь, гуляя по улице и общаясь с другими питомцами, болеющими лишаем. Также очагом грибков являются предметы после зараженных животных, это могут быть подстилки, миски, игрушки или шерсть на полу со спорами грибков. Споры способны до года существовать без своей жертвы.
Еще одним источником инфекции бывают грызуны, на которых охотится мяукающий любимец. Но тогда у кошки лишай будет не единственной проблемой. Ловя мышей или крыс, усатые питомцы могут нахвататься других не менее неприятных болезней.
Но пушистым любимцам, не выходящим за пределы квартиры, тоже грозит опасность получить инфицирование лишаем. Поскольку занесение грибка в дом случается чаще, чем люди об этом подозревают. Придя домой с улицы, человек заносит различные микробы и грязь на подошве обуви, при этом люди переобуваются в домашние тапочки, а вот питомцы своими лапками контактируют напрямую с лишаем.
Человек получает инфекцию лишая от животного через банальное поглаживание шерсти. Имея сильный иммунитет, есть шанс избежать заболевание. Но из-за долгого контакта с больной кошкой все же может случится заражение.
Лечение народными средствами
В домашних условиях лечение лишая у кошек возможно. На ранних этапах, когда только стало заметно полысевшее пятно на теле животного, выручают средства народной медицины. Перед их использованием нужно с помощью ножниц остричь шерсть вокруг пораженного места кошки. Популярны следующие средства:
- Йод — пятно лишая смазывается йодом два раза в сутки при помощи ушной палочки. Также необходимо обработать края лишайного пятна. Стоит осторожно использовать йод, так как от него при обильном смазывании бывают ожоги кожи.
- Раствор бриллиантовый зеленый — используется как вспомогательное средство к обработке йодом. Зеленка чередуется с ним через раз.
- Пепел — чтобы его получить следует сжечь лист газеты, а затем собранный пепел смешать с любым растительным маслом. Полученную смесь втирать питомцу в пораженное пятно два-три раза в сутки.
- Солидол — это техническое средство для машин, но лечит стригущий лишай у кошек гораздо быстрее других средств народной медицины. Он безопасен для животного, если вдруг кот попытается слизать смазанное место. Применяют дважды в сутки.
- Дегтярное мыло — такое мыло используют во время купания кошки. Также можно применить сам деготь, обработав им лишай у питомца.
Применяя данные средства стоит ответственно отнестись к здоровью кошки, обезопасив ее специальным воротником для животных (его еще называют послеоперационный). Если кошка беременна, кормит молоком котят, или же это сами котята до двух месяцев, нельзя самостоятельно убирать лишай у кошек, лечение в домашних условиях может усугубить ситуацию или навредить животному, вплоть до гибели. Надо обязательно отнести питомца на осмотр ветеринару и проводить лечение под его присмотром.
Лечение стригущего лишая медикаментами
Чтобы домашнее животное максимально быстро избавилось от лишая, его необходимо показать ветеринару. Лечение лишая у кошек следует выполнять после результатов осмотра врачом и прописанного им рецепта. Но бывают случаи, когда добраться до ветеринарной клиники невозможно, либо кошка напрочь не переносит транспортировку. Тогда варианты следующего лечения помогут избавиться от заболевания.
Каждый кот нуждается в индивидуальном лечении. В ветеринарных клиниках первым делом врач определяет критерии, указанные ниже.
- Степень болезни.
- Участки, пораженные лишаем.
- Степень иммунитета животного.
Зная состояние данных критериев, ветеринар составляет рецепт, как лечить у кошки лишай. Если степень заражения невелика, болезнь только началась, достаточно проколоть вакцины лечебно-профилактического назначения.
Но при запущенных случаях питомцам необходимы противогрибковые препараты, желательно внутреннего и наружного использования. Лучшим методом терапии станет комплексное лечение – это сочетание вакцинации, препаратов местной терапии, применение таблеток и средств, повышающих иммунитет.
Важно одновременно с лечением пушистого друга провести дезинфекцию помещения, так как споры лишая могли разнестись животным по всему дому. Следует пропылесосить все углы и ковры, промыть мыльным раствором поверхности. Также необходимо использовать кварцевую лампу. По возможности больное животное держать в карантине от других питомцев дома и исключить их контакт с детьми.
Вакцинация
Проверенными вакцинами, лечащими стригущий лишай у кошек, являются следующие медицинские препараты:
[attention type=yellow]Данные вакцины используются согласно инструкции. Для профилактики заболевания их действие малоэффективно. Хорошо сочетаются в комплексном лечении. Их можно применять даже от лишая у котят с двухмесячного возраста. Запрещено использовать кошкам, вынашивающим или кормящим котят.[/attention]
ТРИХОФИТИЯ | kotodom.ru
Трихофития, или стригущий лишай, — контагиозное грибковое заболевание, характеризующееся образованием на коже округлых, резко ограниченных облысевших участков с экссудативным дерматитом и гнойным фолликулитом. Этим заболеванием может болеть и человек.
Заболевание вызывают грибки рода Trichophiton. Они имеют нитчатое, неразветвленное тело и образуют большое количество спор, что способствует их широкому распространению. Трихофитии обладают значительной устойчивостью к действию тепла и дезинфицирующих веществ, долго сохраняются во внешней среде: на подстилке, в почве, на деревянных предметах.
Носителями патогенных дерматомицентов являются мыши, крысы и другие грызуны. У бродячих кошек стригущий лишай возникает и легко распространяется на других домашних животных при нарушении зоогигиенических правил содержания. Такие бездомные особи представляют пасность и для человека (прежде всего для детей). Неблагоприятные пoгодные условия и поверхностные повреждения кожи способствуют проявлению стригущего лишая.
Болеют обычно котята, плохо питающиеся кошки, а также животные с ослабленным иммунитетом из-за другого заболевания. Источником инфекции являются больные и переболевшие животные. Это заболевание передается кошкам от других животных через поврежденные участки кожи, путем контакта со спорами, находящимися в земле, на игрушках и мебели. Кошки могут быть бессимптомными носителями, представляя угрозу для всех живущих рядом с ней. Резервуаром возбудителя являются мышевидные грызуны, бродячие кошки.
Инкубационный период длится от 7 до 30 дней. Заболевание протекает хронически и выражается в появлении на коже небольшин безволосых пятен округлой формы, покрытых чешуйками и корочками асбестово-серого цвета. Чаще всего поражается кожа головы, шеи, конечностей. В запущенных случаях множественные пятна могут сливаться и захватывать значительные участки тела. Зуд отсутствует или слабо выражен.
При глубокой форме трихофитии у кошек происходит нагноение волосяных мешочков, под корками скапливается мнoго гноя. Стригущий лишай может поражать и когги (онихoмикоз). В этом случае когги становятся толстыми и деформируются.
В легких случаях заболевание протекает без зуда. На пораженных местах могут появиться корочки и струпья, которые позже начинают мокнуть. Кошка лижет их и пытается чесать. Иногда отмечается обширное поражение кожи. В легких случаях заболевание приводит к выпадению волос и локальнoму шелушению кожи.
Диагноз ставят на основании клинических признаков и при ультрафиолетовом облучении пораженныx мест, при микроскoпическом исследовании соскобов кожи, которое проводится в ветеринарной лаборатории.
В cлучae локального поражения состригите пораженную шерсть у краев бляшки и вымойте кожу раствором бетадина для удаления омертвевших чешуек. Ежедневно обрабатывайте пораженные участки фунгистатическим кремом, мазью или раствoром. В случае инфицирования пораженных участков обработайте их мазями с антибиотиками. При обширных поражениях состригается вся шерсть и кошку обрабатывают фунгистатической жидкостью 2 раза в неделю. Внутрь назначают гризеофульвин (фульвицин). Для лечебных и профилактических целей используют высокоэффективные, надежные и малотоксичные живые и инактивированные вакцины.
Для профилактики заболевания и повторного заражения проводится вакцинация, санитарнo-гигиенические мероприятия в помещении и на улице.
Предметы ухода обрабатывают слабым раствором гипохлорита натрия (1: 10) или любым хлор содержащим чистящим средством. Проводится тщательная уборка в доме, ковры еженедельно пылесосят для удаления зараженных волос.
Тропические микозы: причины, симптомы, диагностика, лечение
Тропический желтый лишай
Ярким представителем разноцветных лишайников в жарком климате является тропический желтый лишай, вызываемый в основном Malassezia furfur, который относится к кератомикозам и характеризуется появлением преимущественно на коже лица, шеи, реже на других участках небольшие желтовато-оранжевые пятнистые высыпания. Независимость этого кератомикоза признают далеко не все, а потому его удобнее отнести к одной из разновидностей красочного лишая.
Чаще всего желтый лишай встречается в тропических и субтропических странах Юго-Восточной Азии, Южной Америки и Кубы, реже — на Африканском континенте. Заболевание имеет ярко выраженный сезонный характер и возникает обычно в сезон максимальной влажности. Болеют не только взрослые, но и дети, среди которых наблюдаются групповые заболевания.
Симптомы тропического желтого лишая характеризуются появлением на коже лица и шеи изначально небольших размеров и неправильных очертаний желтоватых пятен с легким оранжевым оттенком.Что касается периферического разрастания, то они сливаются, образуя крупные пятна с более или менее цикличными очертаниями пятна, на поверхности которого наблюдается небольшое шелушение. Субъективные ощущения отсутствуют.
Тропический черный лишайник
Как вариант тропического кератомикоза рассматривается тропический черный лишай (tinea nigra) с соответствующим цветом пятен, также имеющий излюбленную локализацию на коже лица. Кроме того, в тропических условиях очень широко распространены классические разновидности разноцветных лишайников с типичной локализацией и склонностью к обширным поражениям.
Пьедра
К группе грибковых поражений волос, или, к типичным представителям тропических грибковых инфекций, можно отнести пиедру. Этот трихомикоз характеризуется развитием на волосах небольших множественных или единичных плотных узловатых образований, которые представляют собой грибковые колонии, окружающие волосы в форме комков. Пьедра встречается в основном в Центральной и Южной Америке, чаще в Колумбии, Аргентине, Бразилии, Парагвае и Уругвае. Отдельные случаи зарегистрированы в Юго-Восточной Азии, Японии и некоторых других странах.Возбудителями пиедры являются представители рода Trichosporon, в частности, пиедра белая Тр. Giganteum, Tr. Cerebriforme, Тр. Овале и др.
Причины пьедры
Патогенетическими факторами, способствующими развитию болезни, являются высокая температура и влажность окружающей среды, определенные социальные и бытовые условия. Например, некоторые национальные обычаи, в частности, смазывание волос при укладке растительными маслами и кисломолочными продуктами имеют значение.Условия, которые постоянно создаются с помощью этого метода укладки волос (при высокой температуре и влажности окружающей среды), близки к термостатическим условиям для развития грибка. Закономерностью также является то, что пиедра встречается в основном у людей с прямыми длинными волосами и, реже, с короткими и вьющимися волосами. Видимо поэтому пиедра практически не встречается на африканском континенте. Болеть могут люди обоего пола, хотя чаще встречается у молодых женщин.
[1], [2], [3], [4], [5], [6], [7]
Симптомы пьедры
Симптомы пиедры характеризуются наличием на волосах в области головы от нескольких до 20-30 и более мелких и очень твердых узелков, которые особенно хорошо видны через хрусталик.Они имеют вид неправильных, овальных или веретенообразных образований, покрывающих волосы почти сплошным кольцом. В некоторых случаях в результате слияния близкорасположенных узелков волосы кажутся окруженными сплошной муфтой. Существует два основных типа пьедры: черная и белая.
Тропическая, или черная, пьедра характеризуется коричневатым или насыщенно-коричневым цветом узелков, которые легко обнаруживаются при пальпации при переноске волос между пальцами. Иногда в запущенных случаях туго натянутые волосы из-за склеивания узелков плотно прилегают друг к другу и образуют целые пучки пораженных волос, которых часто называют колумбийским жеребенком.Однако даже в таких тяжелых случаях практически не поражаются сами волосы, так как споры обнаруживаются только на волосах, не проникая внутрь и тем самым поражая кутикулу, поэтому волосы, пораженные ножкой, никогда не обламываются.
Несколько отличается белая пиедра, которая, помимо стран Южной Америки, встречается также в странах Азии и Европы. Белая пиедра может наблюдаться у мужчин в области роста бороды и усов, у женщин — на волосистой части головы, лобковой области и в подмышечных впадинах.Узелки с белой пиедрой имеют светлый цвет с серовато-желтым и молочно-матовым оттенками, они не такие каменистые, как у черной пиедры. Размер муфт с белой пьедрой иногда достигает 7-10 мм.
Диагностика пьедры
Диагностика педры в целом несложна и основана на типичных клинических проявлениях.
[8], [9], [10], [11], [12], [13], [14]
Лечение пьедры
Самый радикальный способ лечения пиедры — стрижка пораженных грибком волос.Также можно использовать специальные лечебные шампуни, содержащие в необходимой концентрации антимикотики, преимущественно из группы азолов.
Завозный трихомикоз
Особой проблемой в контексте тропического дерматомикоза может быть возможный риск заноса тропической инфекции в страны с умеренным климатом. Примером такой завозной грибковой инфекции из группы трихомикозов могут служить некоторые варианты поверхностного трихофитоза волосистой части головы, который в целом, как известно, относится к одной из самых заразных форм трихомикоза.Выделенные патогены в таких завозных случаях чаще всего классифицируются как Trichophyton soudanense и обычно «импортируются» из стран африканского континента. Клиническая картина такого трихомикоза практически не отличается от таковой у обычного «стригущего лишая». Тем более важна необходимая настороженность дерматолога для этого диагноза у пациента, приехавшего из тропических стран.
Хронический кандидоз кожи и слизистых оболочек
Грибы Candida — очень распространенная инфекция, которая может приобретать особое значение в тропическом климате, где создаются наиболее благоприятные условия для их роста и размножения.Поражения кожи и слизистых оболочек, вызываемые Candida spp., , в этих условиях нередко приобретают хронический, широко распространенный характер. Пример — хронический кандидоз кожи и слизистых оболочек, сочетающий одновременное поражение этих структур. Кожа становится эритематозно-инфильтрированной, покрывается корками и растениями. Соседние участки слизистой оболочки ярко гиперемированы, покрыты белым налетом, часто с явлениями гранулематоза.
Особой тенденции к эндемичности кандидоза кожи и слизистых оболочек, как известно, не существует и встречается повсеместно.Однако, помимо высокой температуры и влажности в тропиках, распространению этой грибковой инфекции во многом может способствовать гиповитаминоз, характерный для ряда стран этого пояса.
Для обычного дерматомикоза, при котором Tr представляет собой , признанный частым возбудителем . рубрум, В условиях тропиков характерно быстро развивающееся преобладание высыпаний на больших участках кожи с поражением кожи лица.
Кроме того, в последние годы в европейских странах зарегистрировано заметное увеличение количества завозных грибковых инфекций с обычной клинической картиной, но с атипичными патогенами для умеренного климата. Бытует мнение, что это связано не только с миграционными процессами, но и может происходить за счет простого физического переноса возбудителя по транспортным путям. В частности, поверхностный дерматомикоз, вызываемый Scytalidium dimidiatum, в последние годы диагностирован в Европе улицами из стран Юго-Восточной Азии и Океании.Клинические симптомы этой грибковой инфекции очень похожи на симптомы гиперкератотического микоза стоп, но многие его детали еще не известны, включая механизм передачи. Поскольку во многих случаях грибковая инфекция протекает бессимптомно на начальных этапах развития или может напоминать другие заболевания, требуется особое внимание для повышения возможности диагностики такой грибковой инфекции.
Особый интерес с точки зрения тропической дерматологии представляют глубокие микозы, которые, как известно, очень распространены в жарких странах.Самый яркий пример этой группы — мадуромикоз.
[15], [16], [17], [18], [19]
Мадуромикоз
Болезнь Мадура или мадурская стопа (мицетома) — один из классических представителей тяжелых и длительных глубоких микозов тропических стран с преимущественным поражением стоп и голеней.
Заболевание известно давно — первое его описание относят к началу XVII века. Мадуромикоз встречается во многих странах мира с условиями тропического или субтропического климата: это практически все страны Юго-Восточной Азии, многие страны Африки и Южной Америки.Спорадические случаи также могут возникать в некоторых европейских странах с умеренным климатом. Многие дерматологи склонны рассматривать мадуромикоз как болезнь полиэтилена, поскольку грибы, которые выявляются в разных случаях, принадлежат к самым разным семействам, родам и видам: Actinomyces, Nocardia, Aspergillus, и другие.
Причины болезни Мадуры
В целом возбудители мадуромикоза можно отнести к условно-патогенным организмам. Они широко распространены в природе, особенно в тропическом климате.Основной путь заражения — экзогенный, а травмы, например, колючки или острые окончания растений или просто хождение босиком по загрязненной почве, способствуют проникновению возбудителя.
[20], [21], [22], [23], [24], [25], [26], [27], [28]
Симптомы болезни Мадура
Чаще всего процесс начинается в области стоп, несколько реже — в области голени. На месте проникновения возбудителя единичный небольшой размер вплоть до узелка гороха, при пальпации плотный и несколько болезненный.По мере того, как узлы увеличиваются и расширяются через несколько месяцев, в их центральной части начинается размягчение и наблюдается колебание. В конце концов, абсцесс вскрывается с образованием свищей, от которых отделяется гнойный со зловонным запахом, содержащий видимый невооруженным глазом грибовидный гриб размером 2-3 мм, похожий на икру. Цвет этих друзов может быть разным — белым, желтым, черным, иногда красным, что зависит от пигмента, который собирают грибы на разных этапах своего развития.
В течение 3-4 лет процесс медленно распространяется как на здоровые участки, так и на более глубокие слои кожи, подкожную клетчатку, вплоть до поражения костей. Стопа становится увеличенной в размерах, бугристой, резко деформируется, иногда становится бесформенной массой. Свод стопы сглаживается, пальцы как бы повернуты кверху, голень наоборот выглядит заметно истонченной.
Диагностика болезни Мадуры
Диагностика мадурикоза в типичных случаях несложна и основывается на типичных клинических проявлениях.В некоторых случаях необходимо провести дифференциальный диагноз с актиномикозом.
[29], [30], [31], [32], [33]
Лечение болезни Мадуры
С прогностической точки зрения мадуромикоз не относится к заболеваниям с тяжелым прогнозом, известны даже случаи самолечения. Однако развивающиеся деформации стопы и поражения костей могут потребовать хирургического вмешательства, вплоть до ампутации стопы.
Споротрихоз
Другой тропический микоз — споротрихоз — хроническое заболевание из группы глубоких микозов с лимфогенным поражением преимущественно кожи, подкожной клетчатки и реже других органов и систем.Чаще всего споротрихоз встречается в Южной Америке, прежде всего в Мексике, несколько реже — в странах Африки и Юго-Восточной Азии.
Что вызывает споротрихоз?
Споротрихоз вызывается различными видами грибов рода Sporotrichon. Как сапрофиты, они широко распространены в природе, в почве, на растениях, овощах, цветах и т. Д. Их существование и распространение в природе способствуют высокой температуре и влажности. Поражение человека, по мнению большинства исследователей, происходит экзогенно, чаще всего после травмы кожи и реже — слизистых оболочек.Люди болеют в любом возрасте и любого пола. Локализация высыпаний связана с открытыми участками тела, которые часто травмируются: кистями, стопами, предплечьями, иногда лицом. Обычно различают две клинические формы споротрихоза: локализованный и диссеминированный. Локализованную форму иногда называют лимфатической, и она встречается чаще, чем диссеминированная.
Симптомы споротрихоза
Вначале на месте проникновения возбудителя образуются небольшие прыщи, которые затем становятся типичной язвой.Иногда все сразу может начаться с липкого узла. Узелок или узел, изначально размером с горошину, плотный и безболезненный, начинает постепенно увеличиваться в размерах и приобретает форму полусферической опухоли. Образование спаяно с подкожно-жировой клетчаткой, кожа над ним воспаляется, приобретает тускло-синюшный оттенок и, некротизируясь, превращается в язву. Весь этот процесс занимает довольно много времени. Иногда это первичное проявление споротрихоза называют споротрихозным шанкром. Обычно он единичный, но возможно наличие трех или пяти очагов одновременно.
Постепенно в процесс вовлекаются регионарные лимфатические сосуды, и на коже появляются линейно расположенные полосы. Пальпаторно прощупываются в виде тяжей с четкими утолщениями. Характерная особенность — полное отсутствие боли даже после пальпации. Позже, иногда по ходу пораженного лимфатического сосуда могут появляться линейно расположенные вторичные узлы, некоторые из них имеют тот же цикл развития, что и первичный аффект.
Локализованная форма споротрихоза отличается доброкачественным течением.Споротрихоз протекает в удовлетворительном состоянии без выраженных изменений со стороны крови. Некоторые авторы описывают акне-подобные проявления споротрихоза, которые изначально могут имитировать вульгарные акне, особенно их конглобатные разновидности.
Диагностика споротрихоза
В типичных случаях диагностика локализованного споротрихоза не составляет труда. Однако в сомнительных ситуациях диагноз может быть подтвержден посевом.
[34], [35], [36], [37], [38], [39], [40], [41], [42]
Глубокие микозы тропических регионов
К частым глубоким микозам тропических регионов относится также южноамериканский бластомикоз или бразильский бластомикоз.
Этот представитель глубоких микозов встречается в основном на южноамериканском континенте и характеризуется торпидным течением с развитием язвенно-гранулематозного поражения не только кожи, но и слизистых оболочек, иногда с поражением внутренних органов, желудочно-кишечного тракта и др. лимфатический узел. Возбудителем болезни в настоящее время признан Blastomyces braziliensis, близкий к бластомицетам североамериканского бластомикоза. Предполагается, что возбудитель попадает в организм человека экзогенным путем.Однако не исключается и роль эндогенного пути заражения.
[43], [44], [45], [46], [47], [48], [49], [50], [51]
Южноамериканский бластомикоз
Южноамериканский бластомикоз встречается исключительно в климатических условиях жарких стран. Главный эндемичный регион — Бразилия. Встречается также в других странах Центральной и Южной Америки. Болеют обычно люди молодого и среднего возраста, несколько чаще — мужчины. Обычно описывается локализованная и реже генерализованная форма.Среди локализованных форм выделяются кожные, кожно-слизистые и висцеральные.
На месте проникновения возбудителя сначала возникают групповые папулезные высыпания. Иногда заболевание начинается сразу с клинической картины ангины или язвенного стоматита. Постепенно, в течение нескольких месяцев, образуется довольно обширный плотный инфильтрат, который постепенно размягчается и подвергается центральному некрозу с поверхностным изъязвлением. Поверхность язв покрыта грануляциями, но рост продолжается как в глубину, так и по периферии, захватывая большие участки слизистой оболочки полости рта, глотки, носоглотки с переходом на более отдаленные участки слизистых оболочек и кожи.При этом развивается реакция со стороны регионарных лимфатических узлов: они разрастаются, становятся болезненными и срастаются вместе с подлежащими тканями. В дальнейшем без лечения в результате генерализации процесса заболевание принимает все более систематический характер.
Диагностика южноамериканского бластомикоза основана на типичных клинических проявлениях и лабораторных данных, включая исследования культур. Прогноз при отсутствии лечения не всегда благоприятен, и болезнь может закончиться летальным исходом.
Дерматофитоз, «стригущий лишай» у кошек |
Обновление, март 2020 г.
Рекомендации по дерматофитиям были впервые опубликованы в J Feline Med Surg 2013, 15: 598-604 Tadeusz Frymus et al. Настоящее руководство было обновлено Тадеушем Фримусом.
Сводка
- Дерматофития, обычно вызываемая Microsporum canis , является наиболее распространенной грибковой инфекцией у кошек и одним из наиболее серьезных инфекционных кожных заболеваний у этого вида.
- M. canis продуцирует артроспоры, которые могут оставаться заразными около года и легко передаются при прямом контакте или через фомиты кошкам, другим видам животных и людям.
- Многие кошки инфицированы субклинически или являются фомитными переносчиками артроспор.
- Дерматофитоз может быть эндемическим заболеванием у групп кошек, особенно в неблагоприятных условиях окружающей среды, и в таких случаях его искоренить трудно.
- Круговая алопеция, шелушение и иногда эритематозный край вокруг центрального заживления («стригущий лишай») — типичные поражения этого хронического кожного заболевания.
- У многих кошек болезнь проходит сама по себе, проявляется только выпадение волос и шелушение. У молодых животных и взрослых с ослабленным иммунитетом исход может быть многоочаговым или генерализованным кожным заболеванием.
- Золотым стандартом обнаружения дерматофитов является посев на агаре Сабуро.Исследование с помощью лампы Вуда и микроскопическое обнаружение артроспор очень хороши для первоначального скрининга.
- Местное лечение может быть эффективным только у одиночных кошек с легкими локализованными поражениями. Для искоренения в группах кошек системная и местная терапия должны сочетаться и продолжаться в течение нескольких недель, и в таких случаях решающее значение имеет интенсивная дезинфекция окружающей среды.
- Для системной терапии препаратами выбора являются итраконазол или тербинафин.
- Рекомендуемое местное лечение — два раза в неделю полоскание тела раствором энилконазола или миконазол с хлоргексидином.
- Безопасные и эффективные вакцины для кошек против этой грибковой инфекции отсутствуют; ABCD не рекомендует вакцинацию.
Свойства агента
В отличие от одноклеточных дрожжей, дерматофиты (буквально: «кожные растения») представляют собой сложные грибы, растущие в виде гиф и образующие мицелий.Почти 40 видов, принадлежащих к родам Microsporum , Trichophyton и Epidermophyton , считаются дерматофитами. Более 90% случаев дерматофитоза кошек во всем мире вызываются Microsporum canis (Moriello and DeBoer, 2012). Другие вызываются M. gypseum , T. mentagrophytes , T. quinckeanum , T. verrucosum или другими возбудителями. За исключением M. gypseum , все эти грибы продуцируют протеолитические и кератолитические ферменты, которые позволяют им использовать кератин в качестве единственного источника питания после колонизации мертвой, ороговевшей части эпидермальной ткани (в основном stratum corneum и волос. , иногда гвозди).
Дерматофиты продуцируют артроспоры, которые обладают высокой устойчивостью и выживают в сухой среде в течение 12 месяцев или более (Sparkes et al., 1994b [EBM grade III]). Однако во влажной среде артроспоры недолговечны. Высокая температура (100 ° C) быстро их разрушает. Артроспоры очень прочно прикрепляются к кератину.
В зависимости от источника инфекции и резервуаров виды дерматофитов подразделяются на зоофильные, сильватические, геофильные и антропофильные грибы.
Эпидемиология
Хотя данные о распространенности дерматофитии ограничены, это заболевание считается наиболее распространенной грибковой инфекцией кошек во всем мире и одним из самых серьезных инфекционных кожных заболеваний у этого вида (Moriello et al., 2017). Он может передаваться другим видам животных, а также является зоонозом (рис. 1, 2).
Рис. 1. Дерматофития ногтя человека. Предоставлено Энди Спарксом, AHT
.Рис.2. Дерматофития на голове человека. Предоставлено Энди Спарксом, AHT
.M. canis — типичный зоофильный дерматофит. Считалось, что субклинические инфекции очень распространены у кошек, особенно у длинношерстных животных старше 2 лет. Однако во многих группах распространенность относительно низкая. Следовательно, M. canis не следует рассматривать как часть нормальной грибковой флоры кошек, и его выделение от здорового животного указывает либо на субклиническую инфекцию, либо на носительство фомита (Moriello and DeBoer, 2012).
Артроспоры передаются в основном при прямом контакте с больными или субклинически инфицированными кошками, а также с собаками или другими видами животных (Moriello, 2014). Кроме того, неинфицированные кошки могут пассивно переносить артроспоры на своей шерсти, тем самым действуя как фомиты. У больных животных стержни инфицированных волос хрупкие, а фрагменты волос, содержащие артроспоры, очень эффективно распространяют инфекцию. Факторы риска включают: введение новых животных в питомник, выставки кошек, питомники, приюты, вязки и т. Д.Артроспоры легко распространяются на частицах пыли, в том числе в недоступные для кошек помещения. Поэтому следует учитывать и косвенный контакт (через загрязненные ошейники, щетки, игрушки, окружающую среду и т. Д.), Хотя это редко документируется (Moriello, 2014).
Кошки, живущие на открытом воздухе, особенно в сельской местности, могут подвергаться воздействию M. gypseum , геофильного гриба, обитающего в почве. Кошки могут быть инфицированы T. mentagrophytes или T. quinckeanum при контакте с мелкими грызунами и T.verrucosum при контакте с крупным рогатым скотом.
Патогенез
Здоровая кожа действует как эффективный барьер против грибкового заражения. Повышенная скорость регенерации клеток эпидермиса в ответ на дерматофит с последующим удалением грибка с поверхности кожи — еще один защитный механизм. Поскольку дерматофиты не могут проникнуть через здоровую кожу, многие кошки являются просто пассивными переносчиками артроспор или остаются инфицированными субклинически.Приведет ли такая инфекция к клиническому заболеванию, зависит от многих факторов. Факторы, предрасполагающие к заболеванию, включают: молодой возраст (первые 2 года жизни), иммуносупрессию (включая иммунодепрессивное лечение), другие заболевания, дефицит питательных веществ (особенно белков и витамина А), высокую температуру и высокую влажность (Moriello and DeBoer, 2012). Для облегчения инфекции очень важны любые травмы кожи в результате повышенной влажности, травмы эктопаразитами или царапины из-за зуда, игры или агрессивного поведения, стрижки и т. Д.В целом, плохая гигиена является предрасполагающим фактором. В переполненных группах кошек социальный стресс может играть важную роль. Это может очень затруднить искоренение стригущего лишая в питомниках или приютах, инфицированных M. canis .
Исследовано потенциальное иммунодепрессивное действие вируса иммунодефицита кошек (FIV) и вируса лейкемии кошек (FeLV) на распространенность грибковой инфекции. О более высокой распространенности M. canis у FIV-инфицированных животных по сравнению с нормальными кошками сообщалось в одном исследовании (Mancianti et al., 1992) не наблюдалась другой группой (Sierra et al., 2000). Было высказано предположение, что любая ассоциация может быть связана с различиями в окружающей среде, а не с ретровирусным статусом кошек (Mignon and Losson, 1997). В недавнем консенсусе был сделан вывод, что серопозитивный статус FIV и / или FeLV сам по себе не увеличивает риск дерматофитоза (Moriello et al., 2017).
Инкубационный период стригущего лишая, вызванного M. canis , составляет от 1 до 3 недель.В это время гифы растут вдоль стержней волос через роговой слой к фолликулам, где они производят споры, которые образуют толстый слой вокруг стержней волос. Поскольку дерматофиты восприимчивы к высоким температурам, они не могут колонизировать более глубокие части кожи или сам фолликул. Таким образом, волосы растут нормально, но легко ломаются у поверхности кожи, что приводит к их выпадению. Некоторые продукты метаболизма грибка могут вызывать воспалительную реакцию в коже и могут наблюдаться в основном вокруг инфицированной области, образуя иногда кольцевые поражения с центральными участками заживления и папулами на периферии («стригущий лишай»).
У многих иммунокомпетентных кошек, живущих в гигиенических условиях, эти поражения ограничены (например, на голове) и исчезают через несколько недель. У животных с подавленным иммунитетом результатом может быть мультифокальное или генерализованное кожное заболевание с вторичными бактериальными инфекциями. В редких случаях выраженная воспалительная реакция на гифы вызывает узловую гранулематозную реакцию с вовлечением дермы и дренированием на поверхности кожи. Эти так называемые псевдомицетомы чаще встречаются у персидских кошек, иногда одновременно с классическими поражениями.
Патогенез других дерматофитных инфекций аналогичен описанному выше.
Иммунитет
Естественный стригущий лишай редко повторяется, что свидетельствует об эффективном и длительном иммунитете. Экспериментальные исследования подтверждают, что животные проявляют повышенную устойчивость к последующему заражению гомологичным грибком. Повторное инфицирование может произойти, но для этого требуется гораздо большее количество спор, и обычно эти последующие инфекции исчезают быстрее (Moriello and DeBoer, 2012).Было высказано предположение, что для развития полного иммунитета инфекция должна протекать своим естественным течением, поскольку у кошек, у которых инфекция была прервана противогрибковым лечением, реакции гиперчувствительности замедленного типа часто были слабее (Moriello et al., 2003).
Хотя дерматофитная инфекция ограничивается поверхностными ороговевшими тканями, индуцируются гуморальные и клеточные иммунные ответы. Выраженная активация Т-хелперных клеток 2-го типа (Th3) и соответствующий цитокиновый профиль приводят к образованию антител с последующим хроническим заболеванием, тогда как активация Th2-клеток стимулирует клеточно-опосредованный ответ, характеризующийся интерфероном-γ, интерлейкинами 12 и 2, и приводит к выздоровлению. (Спаркес и др., 1995; Moriello и DeBoer, 2012). Такие кошки защищены от повторного заражения (Sparkes et al., 1993a). Роль гуморального ответа при дерматофитии неясна, хотя антитела могут оказывать фунгистатический эффект посредством опсонизации и активации комплемента (Sparkes et al., 1994a).
Клинические признаки
У многих кошек дерматофиты вызывают легкую, самоограничивающуюся инфекцию с выпадением и шелушением волос.
Типичным проявлением стригущего лишая у кошек является регулярная и циркулярная алопеция с ломкой шерсти, шелушением, а иногда и эритематозным краем и центральным заживлением (Chermette et al., 2008; Moriello и DeBoer, 2012). Поражения иногда очень маленькие, но иногда могут иметь диаметр 4-6 см. Пораженные участки могут быть одиночными или множественными и локализуются в основном на голове (рис. 3), но также и на любой части тела, включая дистальные части ног и хвост. В частности, у молодых кошек наблюдаются поражения, локализующиеся сначала на переносице, а затем на висках, внешней стороне ушных раковин и краях ушных раковин (рис. 4). Множественные поражения могут сливаться.Зуд варьирует, обычно от легкого до умеренного, и обычно не наблюдается лихорадки или потери аппетита (Chermette et al., 2008; Moriello and DeBoer, 2012).
Рис. 3. Дерматофития во многих случаях начинается на голове. Предоставлено International Cat Care (ранее Feline Advisory Bureau)
Рис. 4. Поражения на носу; любезно предоставлено Энди Спарксом, AHT
У некоторых кошек дерматофития может проявляться в виде папуло-коркового дерматита («милиарный дерматит»), поражающего в основном спинной хобот.
У кошек с ослабленным иммунитетом обширные поражения со вторичным бактериальным поражением иногда связаны с хроническим стригущим лишаем. У таких пациентов наблюдаются атипичные, большие участки облысения, эритема, зуд, экссудация и корки (рис. 5). На этом этапе дерматофития может имитировать другие дерматологические состояния. Типичные признаки все еще могут быть видны на краях поражений.
Рис. 5. В частности, у кошек с ослабленным иммунитетом дерматофитоз может быть многоочаговым и даже генерализованным.Предоставлено International Cat Care (ранее Feline Advisory Bureau)
Редкий исход — ониксис и перионикс, а также исключительно узловой гранулематозный дерматит (псевдомицетома) с единичными или множественными кожными узелками, твердыми и безболезненными при пальпации (Nuttall et al., 2008). Возможны свищи этих узелков. Псевдомицетома в виде образования в брюшной полости может быть редким осложнением лапаротомии у животных с кожным дерматофитозом (Black et al., 2001; Bianchi et al., 2017).
Диагностика
Поскольку дерматофиты могут вызывать поражения, подобные многим кожным заболеваниям кошек, их следует учитывать у всех кошек с любыми кожными заболеваниями. По возможности перед любым лечением следует провести диагностику дерматофитов.
Рис. 6. Предварительный диагноз: флуоресценция при освещении лампой Вуда. Предоставлено Энди Спарксом, AHT
.Недорогой и простой инструмент для просеивания M.canis — исследование с помощью лампы Вуда (рис. 6, 7). Во время процедуры инфицированные стержни волос проявляют флуоресценцию яблочно-зеленого цвета. Обычно считается, что этот метод не очень чувствителен, поскольку только около 50% из штаммов M. canis флуоресцируют, а другие дерматофиты — нет (Sparkes et al., 1994c). Кроме того, мусор, накипь, ворсинки и лекарства для местного применения (например, тетрациклин) могут давать ложноположительные результаты. Таким образом, выводы лампы Вуда должны быть подтверждены другими методами.Однако, согласно выводам Мориелло (Moriello, 2014), по крайней мере, часть так называемых «нефлуоресцирующих штаммов M. canis » могла быть выращена на кошках, которые на самом деле не были инфицированы, а были только пассивными носителями спор (и споры не флуоресцируют). Точно так же, по ее опыту, правильная техника обследования может значительно снизить количество ложноположительных и ложноотрицательных результатов. Она также предположила, что расхождения в отношении полезности лампы Вуда могли частично быть результатом другого качества доступной модели, и пришла к выводу, что лампа с центральной областью, которая позволяет увеличивать исследуемое место, используемое обученным наблюдателем, является очень полезной первой. линейный диагностический тест [EBM степень IV].Советы по правильному использованию лампы Вуда описаны в обзоре (Moriello, 2014).
Рис. 7. Флуоресценция при освещении лампой Вуда. Предоставлено Энди Спарксом, AHT
.Прямое микроскопическое исследование — еще один простой и быстрый метод обнаружения дерматофитов на волосках или чешуях. Для этой цели настоятельно рекомендуется выщипывать волосы при освещении лампой Вуда, что намного лучше, чем извлекать их с края поражения (Moriello, 2014).Перед исследованием образец должен быть очищен 10-20% КОН, хотя возможно прямое наблюдение в капле минерального масла (Moriello, 2014). Существует ряд методов, позволяющих улучшить визуализацию грибковых элементов на стержнях волос (Moriello and DeBoer, 2012). Волосы или фрагменты волос с гифами и артроспорами более толстые, с шероховатой и неровной поверхностью. Однако прямое микроскопическое исследование может дать ложноположительные результаты, особенно если присутствуют споры сапрофитных грибов или мусор интерпретируется как грибковые элементы.Кроме того, чувствительность этого метода относительно низкая и оценивается в 59% (Sparkes et al., 1993b). Более высокая чувствительность (76%) была достигнута с помощью флуоресцентной микроскопии с калькафлуоровым белым — специальным флуоресцентным красителем, который прочно связывается со структурами, содержащими целлюлозу и хитин (Sparkes et al., 1994c).
Культура на агаре с декстрозой Сабуро или других средах обычно считается золотым стандартом для обнаружения дерматофитов, однако неправильный отбор образцов и / или метод посева может привести к ложным результатам (Moriello et al., 2017). Этот метод очень чувствителен и может определять вид. Образцы (волосы, чешуйки) следует собирать с краев новых очагов поражения после осторожного протирания спиртом для уменьшения загрязнения. Если есть подозрение на субклиническую инфекцию или пассивное носительство, чистка стерильной щеткой в течение 5 минут является лучшим методом взятия материала пробы. Совершенно новая зубная щетка микологически стерильна (Moriello and DeBoer, 2012). После такой процедуры количество колоний на чашке отражает серьезность инфекции, и некоторые приюты приняли систему «оценки патогенов» для мониторинга лечения (Moriello, 2014; Moriello et al., 2017). Засеянные среды обычно инкубируют до 3 недель до определения отсутствия роста грибов. Недавно на 2876 культурах M. canis было показано, что только 2,6% из них требовалось> 14 дней для получения положительного результата (Stuntebeck et al., 2018). Несколько коммерческих сред для тестирования дерматофитов (DTM) на основе изменения цвета доступны в продаже. Однако было сделано несколько попыток оценить эффективность таких сред на ветеринарных образцах (Chermette et al., 2008). Следовательно, подозрительные колонии необходимо исследовать под микроскопом, чтобы подтвердить присутствие грибка (Moriello and DeBoer, 2012; Kaufmann et al., 2016).
ПЦРможет помочь подтвердить инфекцию M. canis у подозреваемой кошки (Nardoni et al., 2007; Moriello and Leutenegger, 2018; Jacobson et al., 2018). Было показано, что коммерчески доступная панель ПЦР дерматофитов в реальном времени является высокочувствительной и специфичной для диагностики инфекции M. canis по сравнению с грибковой культурой, но была ненадежной для определения микологического излечения, поскольку были распространены ложноположительные результаты (Jacobson et al. др., 2018).Они могут быть результатом обнаружения мертвых грибковых организмов или пассивного переноса спор (Moriello et al., 2017). Однако отрицательный результат ПЦР у пролеченной кошки означает микологическое излечение (Moriello et al., 2017).
Редко встречающиеся узелковые или атипичные поражения следует оценивать с помощью биопсии кожи и гистопатологии или цитологического исследования аспирата (Moriello et al., 2017).
Ведение болезней
У иммунокомпетентных кошек изолированные поражения исчезают самопроизвольно через 1-3 месяца и могут не требовать лечения.Однако лечение таких случаев снизит течение болезни, а также риск для других животных и людей и загрязнение окружающей среды.
Местная терапия является необходимой частью лечения, поскольку это единственный способ уничтожить споры на шерсти (Moriello, 2014). Однако в качестве лечения он обычно менее эффективен для кошек по сравнению с людьми из-за плохого проникновения лекарств через шерсть, непереносимости этой процедуры многими кошками и возможного существования незаметных небольших повреждений.Таким образом, терапевтические меры должны включать сочетание системного и местного лечения, продолжающееся не менее 10 недель. Как правило, кошек следует лечить не только до тех пор, пока поражения полностью не исчезнут, но и до тех пор, пока дерматофиты не перестанут культивироваться на волосах, по крайней мере, при двух последовательных чистках с интервалом в 1-3 недели. Недавно было высказано предположение, что у кошек, у которых было строгое соблюдение правил очистки окружающей среды, а также рекомендаций по местному и системному лечению, две последовательные отрицательные культуры грибов могут не потребоваться для определения микологического излечения.Если соблюдается хорошая методика отбора проб, первый отрицательный посев у здоровой кошки, вероятно, указывает на устранение возбудителя (Stuntebeck and Moriello, 2019). Кроме того, отрицательный результат ПЦР у пролеченной кошки означает микологическое излечение (Moriello et al., 2017).
В питомниках и приютах инфекцию дерматофитами очень трудно искоренить, она требует много времени и средств. Поэтому важно соблюдение требований владельца. Необходима программа лечения с полным разделением инфицированных и неинфицированных животных и интенсивной очисткой и обеззараживанием окружающей среды.Это потребует прерывания программ разведения и выставок. Целесообразно сгруппировать кошек на 3 категории:
больных животных (положительные как на очаги поражения, так и на культуру, обычно положительные по лампе Вуда)
субклинически инфицирован (без повреждений, положительный посев, обычно положительный результат на лампу Вуда)
кошек-носителей фомита (без повреждений, отрицательный результат по лампе Вуда и отрицательный результат при повторной культуре грибов)
Все животные в питомнике должны проходить лечение, однако переносчиков фомитов лечат только местно, что позволяет избежать длительной дорогостоящей и ненужной системной терапии.При обращении с инфицированными животными необходимо соблюдать особые меры гигиены, чтобы предотвратить заражение людей (перчатки, дезинфекция кошачьих царапин или любых других травм). Большое количество рекомендаций по ведению инфицированных групп кошек было недавно опубликовано в Рекомендациях по клиническому консенсусу Всемирной ассоциации ветеринарной дерматологии «Диагностика и лечение дерматофитоза у собак и кошек» (Moriello et al., 2017).
Местная терапия
У кошек с ограниченным количеством поражений волосы следует обрезать по периферии поражений, включая широкий край.Стрижка должна быть аккуратной, чтобы избежать распространения инфекции из-за микротравм. Точечное лечение поражений может иметь ограниченную эффективность; вместо этого рекомендуется вымыть шампунем, окунуть или ополоснуть все тело. У пациентов с генерализованным заболеванием, длинношерстных кошек и для дезинфекции питомника может быть полезно стричь кошку целиком, чтобы упростить местную терапию и обеспечить лучшее проникновение препарата. Такой подход также ограничивает распространение спор в окружающую среду, среди людей и других животных.После удаления всего волосяного покрова, включая усы, все волосы следует обернуть и продезинфицировать перед утилизацией. Необходима химическая или термическая стерилизация инструментов. Кошек нельзя стричь в ветеринарных клиниках, чтобы избежать загрязнения окружающей среды. Лучшее место для стрижки — в собственном доме кошки, где окружающая среда уже загрязнена. Однако есть сообщения, что стрижка всей кошки приводила к распространению дерматофитии на неинфицированные участки кожи и ухудшению тяжести заболевания (Moriello et al., 2017). Поэтому вместо использования машинок для стрижки, которые могут вызвать травму, следует рассмотреть возможность укорочения волос ножницами. Ножницы также можно более тщательно и легко дезинфицировать.
Противогрибковые препараты для местного применения сильно различаются по своей эффективности. Одна из наиболее эффективных процедур — это лечение всего тела 0,2% раствором энилконазола, проводимое два раза в неделю (Moriello and DeBoer, 2012). О местных или общих побочных эффектах очень редко сообщают, если не допускать ухода (елизаветинский ошейник) до тех пор, пока кошка не высохнет (Hnilica and Medleau, 2002).Очень эффективен также 2% миконазол с 2% хлоргексидином в качестве ополаскивателя или шампуня два раза в неделю (Moriello and DeBoer, 2012; Moriello et al., 2017). В США широко используется раствор извести и серы (смесь полисульфидов кальция) с очень хорошими результатами.
Системная терапия
Итраконазол
Несмотря на то, что итраконазол относительно дорог, в настоящее время он является предпочтительным препаратом при дерматофитиях кошек и лицензирован для этого показания (Moriello and DeBoer, 2012).По эффективности он сравним (или превосходит) кетоконазол или гризеофульвин и намного лучше переносится кошками. Единственная побочная реакция, о которой иногда сообщается, — это анорексия. Эмбриотоксичность и тератогенность итраконазола также ниже, чем у кетоконазола. Тем не менее его применение при беременности не рекомендуется. Возможно использование у котят в возрасте от 6 недель. Большинство ветеринарных дерматологов используют итраконазол в качестве так называемой пульс-терапии, которую также рекомендует производитель.Этот протокол эффективен, а также снижает стоимость лечения. Было предложено пульсирующее введение 5 мг / кг / день в течение одной недели, каждые две недели в течение 6 недель (Colombo et al., 2001). Другое исследование продемонстрировало достаточный уровень итраконазола в плазме и шерсти кошек со стригущим лишаем, которым было проведено три цикла лечения, состоящие из одной недели с лечением (5 мг / кг / день) и одной недели без лечения. Снижение уровней на 25-30% наблюдалось после недели без лечения, но концентрации все еще были достаточно высокими даже через две недели после последнего введения (Vlaminck and Engelen, 2004 [EBM степень IV]).Эти данные показывают, что такая схема лечения (прием дозировки 3 x 7 дней) обеспечивает фактическое покрытие продолжительностью не менее 7 недель.
Тербинафин
Тербинафин, вводимый перорально в дозе 30-40 мг / кг один раз в день, также очень эффективен (Nuttall et al., 2008; Moriello and DeBoer, 2012; Moriello et al., 2017). Кажется, также подходит для пульс-терапии. После приема в течение 14 дней тербинафин сохранялся в волосах кошек в подавляющих концентрациях в течение 5,3 недель (Foust et al., 2007 [EBM grade III]). В качестве побочных эффектов наблюдались эпизодическая рвота и интенсивный кожный зуд.
Кетоконазол
Кетоконазол применялся перорально 2,5–5 мг / кг два раза в день. Однако кошки относительно восприимчивы к побочным эффектам этого препарата, включая токсичность для печени, анорексию, рвоту, диарею и подавление синтеза стероидных гормонов. Кетоконазол также противопоказан беременным животным.
Гризеофульвин
В некоторых странах до сих пор используется гризеофульвин.Однако сейчас это вообще не рекомендуется, так как доступны более безопасные и эффективные препараты. Его вводят перорально в течение как минимум 4-6 недель в дозе 25-50 мг / кг от одного до двух раз в день. Гризеофульвин плохо растворяется в воде, и его микронизированный состав, а также прием с жирной пищей усиливают абсорбцию. Побочные реакции включают анорексию, рвоту, диарею и угнетение функции костного мозга, особенно у сиамских, гималайских и абиссинских кошек. Использование гризеофульвина противопоказано котятам в возрасте до 6 недель и беременным животным, поскольку это соединение обладает тератогенным действием, особенно в течение первых недель беременности.Есть несколько сообщений, предполагающих, что инфекция FIV предрасполагает кошек к подавлению костного мозга, вызванному гризеофульвином. Таким образом, кошки должны быть проверены на эту инфекцию до начала терапии. Если выбран гризеофульвин, необходимо ежемесячно проводить общий анализ крови для выявления возможного угнетения костного мозга.
Луфенурон
Луфенурон — ингибитор синтеза хитина, используемый для предотвращения заражения блохами собак и кошек. Поскольку хитин также является компонентом клеточной стенки грибов, ожидалось противогрибковое действие.Однако исследования на кошках не продемонстрировали противогрибкового эффекта, и луфенурон не рекомендуется для лечения дерматофитии (Moriello and DeBoer, 2012; Moriello et al., 2017).
Прочие опции
Считается, что иммунотерапия крупного рогатого скота и пушных зверей с применением антидерматофитных вакцин уменьшает поражение и ускоряет их исчезновение. Хотя вакцины M. canis продаются для лечения пораженных кошек, трудно найти контролируемые исследования, демонстрирующие эффективность этой процедуры у кошек.Опубликованы результаты плацебо-контролируемого двойного слепого исследования, проведенного на 55 кошках с тяжелым дерматофитозом, вызванным M. canis или T. mentagrophytes (Westhoff et al., 2010). Инактивированная вакцина, содержащая антигены M. canis , M. canis var. distortum , M. canis var. obesum , M. gypseum и T. mentagrophytes три раза внутримышечно вводили больным животным. Наблюдалась тенденция улучшения у всех кошек после терапевтической вакцинации, хотя это улучшение существенно не отличалось от такового у кошек, получавших плацебо.
Обеззараживание окружающей среды
Тщательная (ежедневная) чистка пылесосом и механическая чистка необходимы для удаления инфекционного материала (не должно быть видимых волосков), особенно в домах с одной или несколькими кошками, где дезинфекция нецелесообразна. Однако в питомниках и приютах дезинфекция очень важна, и ее следует проводить не реже двух раз в неделю (Moriello et al., 2017). Большинство дезинфицирующих средств, обозначенных как «противогрибковые», обладают фунгицидным действием против мицелиальных форм дерматофитов или макроконидий, но не против артроспор.Наиболее эффективными против артроспор являются известково-сера в соотношении 1:33, 0,2% -ный энилконазол и бытовой хлорный отбеливатель от 1:10 до 1: 100 (Moriello and DeBoer, 2012). Также было показано, что ускоренная перекись водорода очень эффективна (Moriello, 2019). Все поверхности следует очистить одним из этих растворов. Состав дымового фумиганта с энилконазолом доступен во многих европейских странах.
Подробные процедуры дезактивации, а также обращение с зараженными питомниками и убежищами во время лечения описаны в другом месте (Carlotti et al., 2009; Мориелло и ДеБоэр, 2012; Мориелло, 2014; Moriello et al., 2017).
Вакцинация
Было выполнено и опубликовано очень мало исследований эффективности вакцин против M. canis (профилактических или терапевтических) для кошек. Хотя достигнуты значительные успехи в профилактическом или терапевтическом применении противодерматофитных вакцин у крупного рогатого скота и пушных зверей, безопасная и эффективная вакцина для кошек все еще недоступна (Chermette et al., 2008; Лунд и ДеБоэр, 2008; Moriello et al., 2017).
А убитая вакцина M. canis -клеточной стенки индуцировала как гуморальный, так и клеточно-опосредованный иммунитет у экспериментальных кошек; однако эти ответы не защищали кошек от заражения (DeBoer and Moriello, 1994). Точно так же антигены M. canis в сочетании с живой вакциной Trichophyton не индуцировали защитный иммунитет против местного заражения M. canis (DeBoer et al., 2002). Коммерческая вакцина, состоящая из убитых компонентов M. canis в адъюванте, была лицензирована в США для лечения кошек, а не для профилактики. Однако у экспериментальных кошек эта вакцина не препятствовала возникновению контрольной инфекции, а также не обеспечивала более быстрого излечения установленной инфекции у вакцинированных кошек по сравнению с невакцинированными контрольными животными (DeBoer et al., 2002). Товар был снят с продажи. Были рассмотрены некоторые другие исследования по разработке вакцин против дерматофитоза (Lund and DeBoer, 2008).
ABCD не рекомендует вакцинацию от дерматофитоза.
Зоонозный риск
Инфекция M. canis у людей представляет собой излечимое кожное заболевание. У пациентов с ослабленным иммунитетом время лечения может быть увеличено, но серьезные осложнения крайне редки (Moriello et al., 2017).
Благодарность
ABCD Europe с благодарностью отмечает поддержку Boehringer Ingelheim (спонсор-основатель ABCD) и Virbac.
Список литературы
Bianchi MV, Laisse CJM, Vargas TP, Wouters F, Boabaid FM, Pavarini SP, Ferreiro L, Driemeier D (2017): Интраабдоминальная грибковая псевдомицетома у двух кошек. Преподобный Ибероам Микол 34 (2), 112-115. DOI: 10.1016 / j.riam.2016.10.001.
Black SS, Abernethy TE, Tyler JW, Thomas MW, Garma-Avia A, Jensen HE (2001): Внутриабдоминальная дерматофитная псевдомицетома у персидской кошки. J Vet Intern Med 15, 245–248.
Carlotti DN, Guinot P, Meissonnier E, Germain PA (2009): Искоренение дерматофитоза кошек в приюте: полевое исследование.Ветеринарный дерматол 21, 259-266.
Chermette R, Ferreiro L, Guillot J (2008): Дерматофитозы у животных. Mycopathologia 166, 385-405.
Colombo S, Cornegliani L, Vercelli A (2001): Эффективность итраконазола в качестве комбинированной непрерывной / импульсной терапии при дерматофитии кошек: предварительные результаты в девяти случаях. Vet Dermatol 12, 347–350.
DeBoer DJ, Moriello KA (1994): Иммунный ответ на Microsporum canis , индуцированный вакциной против грибковой клеточной стенки.Ветеринарный дерматол 5, 47-55.
DeBoer DJ, Moriello KA, Blum JL, Volk LM, Bredahl LK (2002): Безопасность и иммунологические эффекты после инокуляции инактивированных и комбинированных живых инактивированных дерматофитийных вакцин кошкам. Am J Vet Res 63, 1532–1537.
Foust AL, Marsella R, Akucewich LH, et al (2007): Оценка стойкости тербинафина в шерсти нормальных кошек после 14 дней ежедневной терапии. Vet Dermatol 18, 246-251.
Hnilica KA, Medleau L (2002): Оценка местного применения энилконазола для лечения дерматофитоза в персидском питомнике.Ветеринарный дерматол 13, 23-28.
Jacobson LS, McIntyre L, Mykusz J (2018): Сравнение ПЦР в реальном времени с грибковой культурой для диагностики дерматофитии Microsporum canis у кошек из приютов: полевое исследование. J Feline Med Surg. 20 (2), 103-107. DOI: 10.1177 / 1098612X17695899.
Kaufmann R, Blum SE, Elad D, Zur G (2016): Сравнение тестовой среды для дерматофитов в местах оказания помощи и микологической лабораторной культуры для диагностики дерматофитоза у собак и кошек.Ветеринарный дерматол 27 (4), 284-e68. doi10.1111 / vde.12322.
Lund A, DeBoer DJ (2008): Иммунопрофилактика дерматофитоза у животных. Mycopathologia 166, 407-424.
Mancianti F, Giannelli C, Bendinelli M, Poli A (1992): Микологические находки у кошек, инфицированных вирусом иммунодефицита кошек. J Med Vet Mycol 30, 257–259.
Mignon BR, Losson B (1997): Распространенность и характеристика носительства Microsporum canis у кошек.J Med Vet Mycol 35, 249-256.
Moriello K (2014): Дерматофитоз кошек: аспекты, относящиеся к ведению болезней в ситуациях с одной или несколькими кошками. J Feline Med Surg 16, 419-431. DOI: 10.1177 / 1098612X14530215.
Moriello KA, DeBoer DJ (2012): Дерматофитоз. В: Грин CE (ред.): Инфекционные болезни собак и кошек. 4 -е изд. Elsevier, стр. 588-602.
Moriello KA, DeBoer DJ, Greek J, Kukl K, Fintelman M (2003): Распространенность реакций гиперчувствительности немедленного и замедленного типа на антигены Microsporum canis у кошек.J Feline Med Surg 5, 161–166.
Мориелло К.А., Койнер К., Патерсон С., Миньон Б. (2017): Диагностика и лечение дерматофитоза у собак и кошек. Рекомендации по клиническому консенсусу Всемирной ассоциации ветеринарной дерматологии. Ветеринарный дерматол 28 (3), 266-e68. DOI: 10.1111 / vde.12440.
Moriello KA, Leutenegger CM (2018): Использование коммерческого анализа количественной ПЦР у 52 кошек из приютов высокого риска для выявления дерматофитии и микологического излечения.Ветеринарный дерматол 29 (1), 66-e26. DOI: 10.1111 / vde.12485.
Moriello KA (2019): Обеззараживание 70 домов приемных семей, подвергшихся воздействию кошек, инфицированных Microsporum canis: ретроспективное исследование. Ветеринарный дерматол 30 (2), 178-e55, DOI: 10.1111 / vde.12722.
Nardoni S, Franceschi A, Mancianti F (2007): Идентификация Microsporum canis из дерматофитной псевдомицетомы в залитых в парафин ветеринарных образцах с использованием общего протокола ПЦР. Микозы 50, 215-217.
Nuttall TJ, German AJ, Holden SL, Hopkinson C, McEwan NA (2008): Успешное разрешение дерматофитной мицетомы после лечения тербинафином у двух кошек. Ветеринарный дерматол 19, 405-410.
Sierra P, Guillot J, Jacob H, Bussiéras S, Chermette R (2000): Грибковая флора на кожных и слизистых поверхностях кошек, инфицированных вирусом иммунодефицита кошек или вирусом кошачьей лейкемии. Am J Vet Res 61, 158–161.
Sparkes AH, Gruffydd-Jones TJ, Shaw SE, Wright AI, Stokes CR (1993b): Эпидемиологические и диагностические особенности дерматофитоза собак и кошек в Соединенном Королевстве с 1956 по 1991 год.Vet Rec 133, 57-61.
Sparkes AH, Stokes R, Gruffydd-Jones TJ (1993a): Гуморальный иммунный ответ у кошек с дерматофитиями. Am J Vet Res 54, 1869–1873.
Sparkes AH, Stokes R, Gruffydd-Jones TJ (1994a): разделение дерматофитных антигенов с помощью SDS-PAGE и вестерн-иммуноблоттинг при дерматофитии кошек. Mycopathologia 128, 91–98.
Sparkes AH, Stokes R, Gruffydd-Jones TJ (1995): Экспериментальная инфекция Microsporum canis у кошек: корреляция между иммунологическими и клиническими наблюдениями.J Med Vet Mycol 33, 177–184.
Sparkes AH, Werrett G, Stokes CR, Gruffydd-Jones TJ (1994b): Microsporum canis : неявное носительство кошек и жизнеспособность артроспор. J Small Anim Pract 35, 397-401.
Sparkes AH, Werrett G, Stokes CR, Gruffydd-Jones TJ (1994c): Повышенная чувствительность в диагностике дерматофитоза с помощью флуоресцентной микроскопии с калькафлуор-белым. Vet Rec 134, 307-308.
Stuntebeck R, Moriello KA, Verbrugge M (2018): Оценка времени инкубации культур дерматофитов Microsporum canis.J Feline Med Surg 20 (10), 997-1000. DOI: 10,1177 / 1098612X17729286.
Stuntebeck RL, Moriello KA (2019): Одна против двух отрицательных грибковых культур для подтверждения микологического излечения у кошек из приюта, получавших лечение от Microsporum canis dermatophytosis: ретроспективное исследование. J Feline Med Surg 3. DOI: 10.1177 / 1098612X19858791.
Vlaminck KMJA, Engelen MACM (2004): Итраконазол: лечение с использованием фармакокинетических основ. Ветеринарный дерматол 15, 8.
Westhoff DK, Kloes M-C, Orveillon FX, Farnow D, Elbers K, Mueller RS (2010): Лечение дерматофитоза кошек инактивированной грибковой вакциной.Откройте Mycology J 4, 10-17.
Криптококкоз |
Криптококкоз у кошек
Отредактировано в ноябре 2016 г.
Руководство по криптококкозу у кошек было впервые опубликовано в J Feline Med Surg 2013, 15: 611-618 by Maria Grazia Pennisi et al. Настоящие правила были обновлены Марией Грацией Пенниси.
Сводка
Криптококкоз — наиболее распространенное системное грибковое заболевание кошек во всем мире; это вызвано C.neoformans-C.gattii видовой комплекс, который включает восемь генотипов и несколько подтипов (штаммов) с различным географическим распространением, патогенностью и чувствительностью к антимикробным препаратам. Криптококкоз — незаразное, редкое или спорадическое заболевание; кошки заражаются зараженной средой.
Прогноз в большинстве случаев благоприятный, при условии, что диагноз будет получен достаточно рано (до распространения или до развития необратимых поражений), а пациенты и владельцы будут сотрудничать, чтобы обеспечить длительный курс лечения (месяцы) и последующее наблюдение (годы).
Базидиоспоры являются инфекционными размножениями криптококка , , поскольку они проникают в дыхательную систему и вызывают первичную инфекцию. Бессимптомная колонизация дыхательных путей встречается чаще, чем клиническое заболевание. Птичьи гуано, особенно голубиный помет, создают благоприятные условия для размножения C. neoformans , но оба вида Cryptococcus связаны с гниющей растительностью, такой как листья эвкалипта.
Криптококкоз, вызванный C. neoformans или C. gattii , клинически неотличим. Заболевание может проявляться в нескольких различных клинических формах, включая назальную форму, форму ЦНС (которая может происходить из носовой формы или возникать независимо), кожную форму и системную форму. Постулируются географические различия в распространенности некоторых клинических проявлений как следствие распределения генотипов с разной вирулентностью.
Простым и надежным тестом для диагностики криптококкоза является обнаружение антигена в жидкостях организма. В качестве альтернативы образцы биопсии могут быть взяты из очагов поражения и отправлены на цитологию, посев, гистопатологию и ПЦР. Только изоляция и ПЦР дают возможность идентифицировать рассматриваемые виды и генотип.
Рекомендации по лечению не установлены, и выбор подходящего противогрибкового препарата зависит от многих факторов, в том числе от согласия владельца.Амфотерицин B, кетоконазол, флуконазол и итраконазол использовались для лечения кошек. Хирургическое удаление любых узелков, расположенных на коже, слизистой оболочке носа или полости рта, является ценным подспорьем у кошек, находящихся на лечении. Как правило, лечение рекомендуется до получения отрицательного результата теста на антиген.
Присутствие птичьих гуано, особенно голубиного помета, и некоторых гниющих растительных субстратов, таких как листья эвкалипта, можно рассматривать как фактор риска, но эффективных профилактических мер продемонстрировано не было.Вакцины недоступны.
Свойства агента
Криптококкоз кошек (КК), открытый более века назад, представляет собой незаразное системное грибковое заболевание, передающееся из загрязненной окружающей среды. По этой причине это не считается зоонозом; животные могут служить дозорным хозяином.
FC вызывается базидиомицетными дрожжами из рода Cryptococcus , принадлежащих к C. neoformans-C.gattii комплекс . Предыдущая классификация выделила пять серотипов (A, B, C, D, AD) в соответствии с антигенными характеристиками капсульного полисахарида (Sykes and Malik, 2012). Обновленная номенклатура, основанная также на генотипировании, различает два основных вида, поражающих кошек: C. neoformans — включая разновидности C. n. вар. grubii (бывший серотип A) и C. n. вар. neoformans (бывший серотип D) — и C. gattii (бывшие серотипы B и C). Согласно молекулярной характеристике, изоляты из C. neoformans-C. Комплекс gattii включает восемь генотипов и несколько подтипов (штаммов) с различным географическим распространением, патогенностью и чувствительностью к антимикробным препаратам (Lester et al., 2011).
Инфекционные пропагулы небольшого размера, такие как базидиоспоры (<2 мкм) и высушенные дрожжевые клетки (<3 мкм), легко распространяются воздушным потоком и могут проникать в дыхательную систему, где происходит первичная инфекция.Гриб может дифференцироваться на несколько морфологических форм, включая дрожжи, хламидоспоры, псевдогифы и гифы, при определенных условиях, но обычно он присутствует в дрожжевой форме у млекопитающих-хозяев, размножаясь путем митоза в тканях животных (Alspaugh et al., 2000; Lin and Heitman, 2006).
Редко сообщалось о других видах: C. albidus , который может поражать кошек с ослабленным иммунитетом, и C. magnus , выделенный у кошек, страдающих отитом (Kano et al., 2004, 2008).
Эпидемиология
Криптококкоз поражает людей, кошек, собак, хорьков, лошадей, коз, овец, крупный рогатый скот, дельфинов, птиц, коал и других сумчатых животных (Sykes and Malik, 2012). Он распространен во всем мире и чаще встречается у кошек, чем у собак (McGill et al., 2009).
К сожалению, Cryptococcus обычно не идентифицируется на видовом и молекулярном уровне при рутинном диагностическом отборе проб, а данные о болезни кошек в Европе берутся из отчетов об отдельных случаях или небольших серий случаев, поскольку болезнь обычно возникает спорадически (Castella et al., 2008). Более крупные ретроспективные исследования доступны только в Канаде, Австралии и Калифорнии (Craig et al., 2002; O’Brien et al., 2004; Duncan et al., 2005, 2006; McGill et al., 2009; Sykes et al., 2010).
Заболевание обычно редкое или спорадическое. Однако в 1999 г. крупномасштабная вспышка криптококкоза, вызванная C. gattii , впервые затронула людей, наземных (собаки, кошки, хорьки, ламы, лошади, птицы) и морских (морские свиньи Phocoenoides dalli ). ) животные; это произошло на юге острова Ванкувер, Британская Колумбия, Канада, в регионе, характеризующемся влажной мягкой зимой и сухим теплым летом.В настоящее время хорошо известно, что C. g attii широко распространен во всем мире на тихоокеанском побережье Северной Америки. В Европе о нем сообщили из Австрии, Дании, Франции, Германии, Греции, Италии, Нидерландов, Португалии, Испании, Швеции и Великобритании (Lester et al., 2011). Также C. n. вар. grubii распространен по всему миру и обычно выделяется от пораженных особей у различных видов животных. C. neoformans считается космополитическим условно-патогенным микроорганизмом в городских популяциях человека, тогда как C.gattii — настоящий патоген, более распространенный в сельской местности (Sykes and Malik, 2012).
Воздействие окружающей среды и бессимптомная колонизация дыхательных путей более распространены, чем клиническое заболевание (Malik et al., 1997b; Connolly et al., 1999). Бессимптомное носительство C. gattii было обнаружено у 4,3% кошек, 1,1% собак и 2% диких животных (белок), пойманных в ловушку в Британской Колумбии (Bartlett et al., 2003; Duncan et al., 2005). .
- neoformans экология обычно связана с присутствием птичьих гуано, особенно голубиного помета, который создает благоприятные условия для митотической амплификации и размножения гриба, но оба вида Cryptococcus связаны с гниющей растительностью, такой как листья эвкалипта (Fortes et al., 2001). Голуби служат носителями C. neoformans , которые, вероятно, способствуют распространению во всем мире, поскольку они несут Cryptococcus на своих клювах, перьях и ногах (Pal, 1989). Животные, растения, почвы и водные пути являются источниками, откуда может заразиться потенциальный патоген.
Кошки в пять-шесть раз чаще подвержены этой болезни, чем собаки, и в три раза больше, чем лошади (McGill et al., 2009). Ретроспективные исследования кошачьих имели тенденцию показывать преобладание у мужчин, хотя этот результат не был подтвержден в других исследованиях (Malik et al., 1992; Flatland et al., 1996; Jacobs et al., 1997; Гердс-Гроган и Дэйрелл-Харт, 1997; Лестер и др., 2004; McGill et al., 2009; Сайкс и др., 2010). Породные породы, такие как рэгдолл, бирман, сиамская и гималайская, считались более подверженными заболеванию, чем домашние кошки, но, опять же, это открытие не было подтверждено в более поздних исследованиях (Malik et al., 1992; O’Brien et al., 2004; McGill и др., 2009; Сайкс и др., 2010; Триведи и др., 2011). В отличие от других видов животных, у которых инфекцией заражаются обычно молодые люди, могут поражаться кошки любого возраста (Malik et al., 1992; McGill et al., 2009). Сезонной тенденции в диагностике инфекции не наблюдается (McGill et al., 2009). Кроме того, образ жизни не является фактором риска — заболевание регистрировалось и у домашних кошек.
Патогенез
Cryptococcus — это прежде всего патоген, передающийся воздушно-капельным путем, а носовая полость обычно является первичным очагом инфекции у кошек и собак. В большинстве случаев наблюдается только субклиническая колонизация без инвазии эпителия (Duncan et al., 2005). Когда происходит инвазия слизистых оболочек, заболевание развивается локально и / или системно. Как у людей, так и у кошек инфекция может возникать в результате проглатывания высушенных дрожжевых клеток или, реже, кожной инокуляции грибковых форм. Инкубационный период варьируется от месяцев до лет, и источник инфекции часто остается неизвестным. Вирулентность (генотип) и нагрузка вдыхаемых организмов влияют на исход инфекции.
Из верхних дыхательных путей инфекция может распространяться локально в ЦНС через решетчатую кость, а в редких случаях — в нижние дыхательные пути или системно (Martins et al., 2011).
Существуют чувствительные к температуре штаммы, которые не могут расти при температурах > 37,0 ° C и могут вызывать инфекции только на участках тела, где температура ниже (кожа, нос, мошонка) (Bemis et al., 2000; Lin, 2009 г.).
Иммунитет
Антитела, вырабатываемые против капсульных антигенов, не являются защитными. Стойкие инфекции могут возникать из-за того, что капсула дрожжевых форм Cryptococcus подавляет фагоцитоз, а другие факторы вирулентности, такие как выработка меланина, защищают дрожжевые клетки от окислительного повреждения.Следовательно, он способен выживать внутри фагоцитарных клеток, таких как макрофаги и нейтрофилы, и может распространяться вместе с этими клетками (Urban et al., 2006; Lester et al., 2011; Tvedi et al., 2011).
Некоторые исследования показали, что криптококкоз имеет более высокую распространенность или менее благоприятный исход у кошек, инфицированных FeLV или FIV (Gerds-Grogan and Dayrell-Hart, 1997; Jacobs et al., 1997), но этот вывод не разделяется другие (Малик и др., 1992; О’Брайен и др., 2004, 2006; Норрис и др., 2007; Сайкс и др., 2010). Заболевание было зарегистрировано у кошек, получающих химиотерапию или с сопутствующей оппортунистической инфекцией, так что нельзя исключить роль иммунокомпетентности в патогенезе ФК (Tvedi et al., 2011; Graham et al., 2011).
Клинические признаки
Криптококкоз, вызванный C. neoformans или C. gattii , клинически неотличим.
Это заболевание может проявляться в нескольких различных клинических формах, включая назальную форму, форму ЦНС (которая может происходить из носовой формы или возникать независимо), кожную форму и системную форму.Постулируются географические различия в распространенности некоторых клинических проявлений как следствие распределения генотипов с разной вирулентностью. Отклонения от нормы в анализах крови неспецифические, если они присутствуют, что свидетельствует о воспалительном процессе.
Рис.1 Носовой криптококкоз — хронические монолатеральные выделения из носа и легкая деформация носа. Предоставлено Марией Грации Пенниси
Носовая форма
Носовая форма является наиболее распространенной у кошек, проявляясь как хроническое сино-носовое заболевание, либо отдельно, либо вместе с местным распространением на кожу, подкожную клетчатку, кости и региональные (поднижнечелюстные) лимфатические узлы (Malik et al., 1992; О’Брайен и др., 2004 г .; McGill et al., 2009). Он вызывает отек носа и лица, за которым следует глубокая незаживающая язва с дренированием студенистого экссудата, хронические выделения из носа (монолатеральные или двусторонние) с серозным, слизисто-гнойным или кровянистым проявлением, стерильная и инспираторная одышка, чихание и сопение, а также подчелюстная лимфаденопатия (рис. 1-3). Анорексия и последующая потеря веса также могут быть результатом аносмии у кошек с хроническим заболеванием носа. Криптококк — важный дифференциал у кошек с хроническими выделениями из носа, независимо от наличия отека лица и / или изъязвления кожи.
.
Рис. 2. Криптококковая инфекция — тяжелый отек и деформация носо-лицевой области. Предоставлено Марией Грации Пенниси
В некоторых случаях может появиться выступающая мясистая масса из одной или обеих ноздрей. Также были описаны гранулемы носоглотки (напоминающие полипы или рак), проявляющиеся стертором, инспираторной одышкой и открытым ртом (Malik et al., 1997a). Также могут развиваться пролиферативные или язвенные поражения в полости рта или глотке.Может возникнуть средний / внутренний отит с вестибулярными признаками (Beatty et al., 2000, Paulin et al., 2013). За этим может последовать заболевание нижних дыхательных путей, и его проявление может быть очевидным радиологически только в виде узелков в легких или средостении.
Рис. 3. Криптококковая инфекция — изъязвленные узелки на коже лица. Предоставлено Марией Грации Пенниси
Форма CNS
Поражение ЦНС наиболее вероятно возникает в результате локального распространения через решетчатую пластину; в таких случаях внезапная слепота из-за оптического неврита появляется вместе с судорогами или изменениями поведения.В других случаях он следует за диссеминацией и вызывает гранулематозный энцефаломиелит с одиночными или множественными поражениями (Belluco et al., 2008; Sykes et al., 2010). У многих кошек наблюдается боль в голове или позвоночнике, но другие признаки поражения менингеальных органов (гиперестезия, ригидность затылочной кости) встречаются нечасто (Sykes et al., 2010).
Кожная форма
Кожные формы характеризуются одиночными или множественными дермальными или подкожными узелками на коже: первые указывают на прямую инокуляцию, вторые — на гематогенное распространение из первичного очага инфекции (Sykes and Malik, 2012).Узелки обычно не вызывают зуда и боли и обычно сопровождаются регионарной лимфаденопатией.
Рис. 4. Криптококковая инфекция — кератоувеит и криптококкома передней камеры. Предоставлено Марией Грации Пенниси
Системная форма
Системные формы могут возникать через гематогенное распространение и проявляться признаками менингоэнцефаломиелита (см. Форму ЦНС), увеита, хориоретинита, остеомиелита и полиартрита, системного лимфаденита или поражения многих органов, включая почки (рис.4 и 5). Синдром полости черепа с тяжелым отеком головы и шеи недавно был зарегистрирован у кошки, пораженной развитием криптококковой массы средостения, сдавливающей вену, а также пищевод и трахею (Letendre and Boysen, 2015).
Апатия и кахексия возникают у кошек с тяжелой диссеминацией при длительном хроническом течении болезни. Системная форма, возникающая в результате диссеминации, может быть или не следовать за классическим заболеванием носа (Tisdall et al., 2007; Martins et al., 2011).
Рис. 5. Рентгенография грудной клетки, вид с вентро-дорсальной стороны: диффузные, множественные, плохо очерченные узелки с размытыми краями в легких кошки с системным криптококкозом. Предоставлено Марией Грации Пенниси
Диагностика
Простым и надежным тестом для диагностики криптококкоза является обнаружение антигена в жидкостях организма. В качестве альтернативы образцы могут быть взяты из пораженных участков и отправлены на цитологию, посев, гистопатологию и ПЦР.К ним относятся (i) плевральный или перитонеальный выпот, (ii) спинномозговая жидкость (CSF), (iii) образцы, взятые из бронхоальвеолярного лаважа, (iv) тонкоигольные аспираты из узелков или увеличенных лимфатических узлов, (v) биопсии, взятые из любых пораженные ткани. Предполагается повышенный риск грыжи мозжечка после сбора CSF, и эту инвазивную процедуру следует рассматривать только в том случае, если заболевание ЦНС, совместимое с FC, не было подтверждено с помощью других подходящих биологических образцов (Sykes et al., 2010).
Выделение и ПЦР дают возможность идентифицировать участвующие виды и генотип (только ПЦР).
Обнаружение антигена
Обнаружение антигена в крови — это тест выбора, если он доступен, потому что он быстрый, надежный и минимально инвазивный. Криптококковый капсульный антиген может быть обнаружен с помощью латексного теста на агглютинацию криптококкового антигена (ЛХАТ) в сыворотке, спинномозговой жидкости или моче. Чувствительность и специфичность теста повышаются за счет предварительной обработки образцов теплом и протеиназой (проназа, часто включаемая в коммерческие диагностические наборы), и это считается хорошим для кошек (Sykes and Malik, 2012).В некоторых случаях могут быть ложноотрицательные результаты (Belluco et al., 2008). Если тест на антиген отрицательный, а криптококкоз все еще возможен, образцы ткани должны быть отправлены на цитологию, гистологию и культуру. С другой стороны, в случае титров <200 рекомендуется подтверждающая цитология, посев или ПЦР.
ТитрЛХАТ также является эффективным способом мониторинга эффективности терапии. Лечение обычно продолжают до получения отрицательного ЛХАТ, но сообщалось, что титр продолжает снижаться после прекращения терапии у кошек с клиническим разрешением и все еще положительным ЛХАТ (O’Brien et al., 2006).
Цитология
Цитология может быть простым инструментом для диагностики криптококкоза, потому что внешний вид микроорганизмов является характерным, а количество дрожжевых грибов в поражениях обычно велико, но отрицательный результат не исключает диагноза. Соответствующие цитологические образцы могут быть получены с помощью мазков-слепков с изъязвленных поражений кожи, аспиратов тонкой иглой узелков, мазков-слепков биоптатов, бронхоальвеолярного лаважа или спинномозговой жидкости.В случае поражения почек в осадке мочи можно увидеть дрожжи (Brandt and Blauvelt, 2010).
Рис. 6. Окрашенный Diff Quick мазок назального экссудата от кошки с инфекцией C. neoformans. Обратите внимание на заметную капсулу (четкий ореол) и узкую почку (стрелка). Микрофотография любезно предоставлена Ричардом Маликом.
Мазки, окрашенные красителем типа Романовского (Wright, Diff-Quick, Giemsa), могут показывать розовые или фиолетовые, круглые или распускающиеся внеклеточные дрожжи, которые различаются по размеру (4-15 мкм) и форме и обычно окружены более или менее прозрачным толстый ореол, соответствующий неокрашенной капсуле (рис.6, 7). Если используется окраска по Граму, микроорганизм выглядит как Gram + с капсулой Gram- (розовой). Обычно наблюдается пиогранулематозный воспалительный процесс. Хотя нитчатые формы обычно не наблюдаются в тканях, эти атипичные морфологические формы C. neoformans могут присутствовать у кошек (Bemis et al., 2000; Lin, 2009).
Рис. 7. Окрашенный Diff Quick мазок аспирата тонкой иглы из криптококкового поражения. Обратите внимание на огромную капсулу, окружающую дрожжевые клетки.Микрофотография любезно предоставлена Марком Крокенбергером
Гистология
Образцы биопсии слизистой оболочки носа, лимфатических узлов или узелков кожи могут быть получены для гистологии, но они также могут предоставить мазки-слепки для цитологии и материал для посева и ПЦР. Срезы, окрашенные гематоксилином-эозином, показывают эозинофильные тельца, окруженные четким ореолом, и пиогранулематозную реакцию (рис. 8). Муцикармин Майера специфически окрашивает капсулу Cryptococcus .Иммуногистохимия на тканевых срезах используется для дифференциации видов с использованием моноклональных антител (рис. 9) (Krockenberger et al., 2001).
Рис. 8. Ранняя инвазия Cryptococcus gattii в респираторный эпителий коалы. Обратите внимание на эозинофильное тело, окруженное четким ореолом. Микрофотография любезно предоставлена Марком Крокенбергером.
Рис. 9 Иммуногистология для демонстрации Cryptococcus gattii в ткани. Агент может быть окончательно идентифицирован в залитых парафином фиксированных формалином срезах с использованием моноклональных антител, направленных против различных эпитопов капсулы.Коричневые осадки выделяют как тело дрожжевой клетки, так и ее капсулу. Обратите внимание также на узкую бутонию шеи. Микрофотография любезно предоставлена Марком Крокенбергером.
Культура
Посев следует проводить, если тест на антиген отрицательный, титры низкие или отсутствуют.Для посева следует сдавать только образцы биопсии носа, поскольку наличие криптококка в культурах выделений из носа не считается признаком заболевания. Положительный посев образцов биопсии и гистологические изменения, соответствующие инфекции, считаются диагностическими и могут использоваться для проверки чувствительности к противогрибковым препаратам.
Посев образцов биопсии более чувствителен, чем цитология в подтверждении инфекции. Cryptococcus легко выделяется в декстрозном агаре Сабуро после инкубации при 25 ° C и 37 ° C в течение 10 дней, а также на стандартной бактериальной среде.Теперь возможно дифференцировать C. neoformans от C. gattii с помощью специфического теста на агар (Lester et al., 2011).
Когда образцы загрязнены бактериями, как это происходит в выделениях из носа, полезны среды, содержащие антибиотики (Sykes and Malik, 2012).
Полимеразная цепная реакция
Полимеразная цепная реакция (ПЦР) была разработана для генетической идентификации в спинномозговой жидкости, моче, сыворотке и образцах биопсии, но на практике не используется в повседневной практике (Kano et al., 2001; Мейер и др., 2003; Okabayashi et al., 2006).
Обнаружение антител
Обнаружение антител не является диагностическим инструментом, поскольку с его помощью нельзя отличить субклиническую инфекцию от заболевания.
Диагностическая визуализация
Передовые методы диагностической визуализации (КТ и МРТ) часто используются в процессе диагностики хронических симптомов носа и ЦНС. Патологические изменения при криптококкозе кошек включают наличие хронического ринита, фронтального синусита и / или интраназальных или внутричерепных очаговых единичных или мультифокальных образований или поражений, заполненных жидкостью (Sykes et al., 2010). Подтверждение диагноза невозможно только с помощью визуализации, но разрешение массового поражения можно проследить с помощью МРТ у кошек, находящихся на лечении (Karnik et al., 2009; Hammond et al., 2011). Результаты МРТ могут также включать усиление менингеальной оболочки, поражение зрительного нерва и решетчатой пластинки (Sykes et al., 2010).
Прогноз
Прогноз в большинстве случаев благоприятный, при условии, что диагноз будет получен достаточно рано (до распространения или до развития необратимых поражений), а пациенты и владельцы будут сотрудничать, чтобы обеспечить длительный курс лечения (месяцы) и последующее наблюдение (годы).
Хотя информация о результатах весьма ограничена, похоже, что у кошек прогноз более благоприятный, чем у собак или лошадей, у которых чаще развиваются заболевания нижних дыхательных путей, диссеминированные и неврологические заболевания, связанные с более высокой смертностью (Duncan et al., 2006; O’Brien et al. ., 2006; McGill et al., 2009; Sykes et al., 2010).
В одном ретроспективном исследовании тяжесть заболевания не повлияла на исход, хотя наличие поражения ЦНС оказало значительное неблагоприятное влияние на исход терапии (O’Brien et al., 2006). С другой стороны, изменение психического статуса было единственным негативным прогностическим фактором в ретроспективном исследовании кошек с формой ФК ЦНС, а полное выздоровление было зарегистрировано также у кошек с формой ФК (Sykes et al., 2010; Hammond et al. ., 2011).
Ведение болезней
Терапия
Нет проспективных контролируемых исследований по лечению криптококкоза кошек, и все данные основаны на ретроспективных исследованиях и отчетах о случаях.Рекомендации по лечению не установлены, и выбор подходящего противогрибкового препарата зависит от многих факторов. Соблюдение требований владельца имеет решающее значение из-за высоких затрат с точки зрения денег и длительного времени, необходимого для лечения.
Сообщалось о некоторых ретроспективных исследованиях результатов лечения криптококкоза кошек с неоднородными критериями оценки успеха терапии (Medleau et al., 1995; Davies and Troy, 1996; Jacobs et al., 1997). В крупнейшем ретроспективном исследовании, проведенном на 59 кошках, 68% имели успешный результат (O’Brien et al., 2006). Большинству из них потребовался один курс лечения продолжительностью несколько месяцев (от 1 до 24), и несколько кошек получили второй курс лечения из-за клинического рецидива или повышения титра ЛХАТ. Согласно более позднему ретроспективному исследованию, клинический результат может быть благоприятным примерно у 2/3 пролеченных кошек (McGill et al., 2009). У большинства выздоровевших кошек были выявлены сино-носовые или единичные поражения на коже, подкожной клетчатке или кишечнике, а у тех, у кого не выздоровели, были поражения ЦНС или диссеминированное заболевание.
Амфотерицин B, кетоконазол, флуконазол и итраконазол применялись для лечения кошек. Что касается эффекта различных терапевтических протоколов, не было существенной разницы в результатах между кошками, получавшими протоколы, содержащие амфотерицин B, и кошками, получавшими монотерапию азолом с использованием флуконазола или итраконазола (O’Brien et al., 2006).
Средняя кумулятивная доза AMB для кошек, вылеченных с первой попытки, составила 16 мг / кг (от 7 до 23 мг / кг).Это было выше, чем ранее рекомендованная кумулятивная доза от 4 до 8 мг / кг. Средняя продолжительность лечения кошек, получавших флуконазол, была значительно короче (4 месяца; диапазон от 1 до 8 месяцев), чем медиана для группы итраконазола (9 месяцев; диапазон от 3 до 24 месяцев). Липосомальные формы AMB могут лучше переноситься, но они очень дороги и труднодоступны. Рекомендации по лечению, основанные на тематических исследованиях, заключаются в том, что флуконазол или итраконазол являются хорошим выбором.
В ЦНС или системных случаях амфотерицин B, отдельно или в комбинации с флуцитозином, может быть первым выбором с последующим длительным лечением флуконазолом или итраконазолом (O’Brien et al., 2006). Кошек с уже существующим заболеванием почек следует лечить только итраконазолом или флуконазолом. Флуконазол, по-видимому, более эффективен, чем итраконазол, при инфекциях ЦНС, глаз и мочевыводящих путей, а также лучше переносится (Tvedi et al., 2011; Hammond et al., 2011; Sykes and Malik, 2012). Об устойчивости к флуконазолу сообщалось у некоторых изолятов, которые, однако, были чувствительны к другим азолам (Lester et al., 2011; Kano et al., 2015).
Клиническое состояние кошек с церебральным криптококкозом может ухудшиться вскоре после начала терапии амфотерицином B, предположительно из-за воспалительной реакции и повышения внутричерепного давления.Сообщается, что терапия кортикостероидами короткого действия (дексаметазон или преднизолона натрия сукцинат) дает немедленный эффект в таких случаях и связана с большими шансами на выживание в краткосрочной перспективе (O’Brien et al., 2006; Sykes et al., 2010).
Хирургическое удаление любых узелков, расположенных на коже, слизистой оболочке носа или полости рта, следует рассматривать как ценную помощь кошкам, получающим медикаментозное лечение (Hunt et al., 2002).
Как правило, лечение рекомендуется до получения отрицательного результата теста на антиген.Если на момент постановки диагноза тест на антиген отрицательный, и заболевание было подтверждено другими методами или если тест на антиген недоступен, лечение следует продолжать как минимум в течение 2–4 месяцев после исчезновения клинических признаков.
В таблице 1 перечислены варианты лечения этой инфекции.
Лечение криптококкоза
| Препарат / терапия | Доза и продолжительность | Комментарии |
|---|---|---|
| IV = внутривенно, PO = перорально, ЦНС = центральная нервная система | ||
| Итраконазол | 50-100 мг на кошку каждые 24 часа | Хорошая абсорбция без еды.Пероральный раствор лучше, чем капсулы. Возможна гепатотоксичность; контролировать ферменты печени периодически / ежемесячно |
| Амфотерицин B | 0,25 мг / кг каждые 48 часов внутривенно до общей дозы 4–16 мг / кг | Лечение выбора при инфекции ЦНС и / или системном заболевании. Значительная нефротоксичность; контролировать функцию почек часто / еженедельно |
| Флуцитозин | 25-50 мг / кг перорально каждые 6 часов | Синергетическое средство с амфотерицином B; не использовать в качестве однократного лечения |
| Флуконазол | 50 мг / кошку каждые 12 часов | Предлагаемое лечение выбора, особенно при инфекции ЦНС.Хорошая абсорбция без еды. Монитор ферментов печени |
| Тербинафин | 10 мг / кг каждые 24 часа | Используется при устойчивости к азолам |
| Хирургическое удаление | Гранулемы кожи, ротоглотки и ноздри |
Профилактика
Свободно бродячие кошки в сельской местности потенциально более подвержены заражению Cryptococcus, , хотя городские кошки могут быть заражены голубиным гуано . Согласно экологическим данным, присутствие птичьих гуано, особенно голубиного помета и некоторых гниющих растительных субстратов, таких как листья эвкалипта, может считаться фактором риска (Fortes et al., 2001). Знание местных местообитаний грибов, которые несут наибольший риск заражения, и сезонных колебаний в производстве заразных пропагул было бы полезно для разработки профилактических мер как для заражения людей, так и для животных.
Список литературы
Alspaugh JA, Davidson RC, Heitman J (2000): Морфогенез Cryptococcus neoformans .Contrib Microbiol 5, 217-238.
Bartlett KH, Fyfe MW, MacDougall LA (2003): Environment Cryptococcus neoformans var gattii в Британской Колумбии, Канада. Am J Respir Crit Care Med 167, A499.
Битти Дж. А., Баррс В. Р., Суинни Г. Р., Мартин П. А., Малик Р. (2000): Периферическое вестибулярное заболевание, связанное с криптококкозом у трех кошек. J Feline Med Surg 2, 29-34.
Belluco S, Thibaud JL, Guillot J, Krockenberger MB, Wyers M, Blot S, Colle MA (2008): Спинальная криптококкома у иммунокомпетентной кошки.J. Comp Pathol 139, 246-251.
Bemis DA, Krahwinkel DJ, Bowman LA, Mondon P, Kwon-Chung KJ (2000): термочувствительный штамм Cryptococcus neoformans , продуцирующий гифальные элементы в гранулеме носа у кошек. J Clin Microbiol 38, 926-928.
Brandt LE, Blauvelt MM (2010): Каков ваш диагноз? Осадок мочи от похудевшей кошки из южной Калифорнии. Ветеринарная клиника Патол 39, 517-518.
Castella G, Abarca L, Cabanes FJ (2008): Criptococosis y animales de Compañía.Ред. Iberoam Micol 25, S19-S24.
Connolly JH, Krockenberger MB, Malik R, Canfield PJ, Wigney DI, Muir DB (1999): бессимптомное носительство Cryptococcus neoformans в носовой полости коалы (Phascolarctos cinereus). Med Mycol 37, 331-338.
Крейг С., Лестер С., Блэк В., Файф М., Раверти С. (2002): Многовидовая вспышка криптококкоза на юге острова Ванкувер, Британская Колумбия. Может Ветеринар J 43, 792-794.
Дэвис С., Трой Г.К. (1996): Глубокие микотические инфекции у кошек.J Am Anim Hosp Assoc. 32, 380–391.
Duncan C, Stephen C, Campbell J (2006): Клинические характеристики и предикторы смертности от инфекции Cryptococcus gattii у собак и кошек на юго-западе Британской Колумбии. Can Vet J 47, 993–998.
Duncan C, Stephen C, Lester S, Bartlett KH (2005): Последующее исследование собак и кошек с бессимптомной инфекцией Cryptococcus gattii или носовой колонией. Med Mycol 43, 663-666.
Flatland B, Greene RT, Lappin MR (1996): Клиническая и серологическая оценка кошек с криптококкозом.J Am Vet Med Assoc 209, 1110-1113.
Fortes ST, Lazéra MS, Nishikawa MM, Macedo RC, Wanke B (2001): первая изоляция Cryptococcus neoformans var. gattii из местного дерева джунглей в тропических лесах бразильской Амазонки. Микозы 44, 137-140.
Гердс-Гроган С., Дейрелл-Харт Б. (1997): Криптококкоз кошек: ретроспективное исследование. J Am Anim Hosp Assoc. 33, 118–122.
Graham KJ, Brain PH, Spielman D, Martin PA, Allan GS, Malik R (2011): Сопутствующая инфекция комплексом видов Cryptococcus neoformans / gattii и Mycobactcerium avium , поражающая подкожную клетчатку и кость тазовой конечности у кошки .J Feline Med Surg 13, 776-780.
Hammond JJ, Glass EN, Bishop TM, Kent M, De Lahunta A (2011): Диагностика визуализации — внутричерепная криптококковая масса у кошки. Vet Radiol Ultrasound 52, 306-308.
Hunt GB, Perkins M, Foster SF, Barrs VR, Swinney GR, Malik R (2002): Назофарингеальные расстройства у собак и кошек: обзор и ретроспективное исследование. Сборник Cont Educ Practices Vet 24, 184-199.
Jacobs GJ, Medleau L, Calvert C, Brown J (1997): Криптококковая инфекция у кошек: факторы, влияющие на результат лечения, и результаты последовательных титров сывороточных антигенов у 35 кошек.J Vet Intern Med 11, 1–4.
Kano R, Fujino Y, Takamoto N, Tsujimoto H, Hasegawa A (2001): ПЦР-обнаружение гена Cryptococcus neoformans CAP59 из образца биопсии из случая криптококкоза кошек. J Vet Diagn Invest 13, 439–442.
Kano R, Hosaka S, Hasegawa A (2004): Первое выделение криптококка magnus от кошки. Mycopathologia 157, 263-264.
Кано Р., Китагават М., Оота С., Оосумит Т., Мураками Ю., Токурики М. и др. (2008): Первый случай системной инфекции Cryptococcus albidus у кошек.Med Mycol 46, 75-77.
Кано Р., Окубо М., Янаи Т., Хасегава А., Камата Н. (2015): Первая изоляция азол-устойчивого Cryptococcus neoformans от кошачьего криптококкоза. Mycopathologia 180, 427-433.
Karnik K, Reichle JK, Fischetti AJ, Goggin JM (2009): Результаты компьютерной томографии грибкового ринита и синусита у кошек. Vet Radiol Ultrasound 50, 65-68.
Krockenberger MB, Canfield PJ, Kozel TR, Shinoda T, Ikeda R, Wigney DI et al (2001): иммуногистохимический метод, позволяющий дифференцировать разновидности и серотипы Cryptococcus neoformans в фиксированных формалином тканях, залитых парафином.Med Mycol 39, 523-533.
Lester SJ, Kowalewich NJ, Bartlett KH, Krockenberger MB, Fairfax TM, Malik R (2004): Клинико-патологические особенности необычной вспышки криптококкоза у собак, кошек, хорьков и птиц: 38 случаев (с января по июль 2003 г.). J Am Vet Med Assoc 225, 1716-1722.
Lester SJ, Malik R, Bartlett KH, Duncan CG (2011): Криптококкоз: обновление и появление Cryptococcus gattii . Ветеринар Clin Pathol 40, 4-17.
Letendre J-A, Boysen S (2015): Синдром краниальной полой вены, вторичный по отношению к криптококковой гранулеме средостения у кошки.Может Ветеринар J 56, 365-369.
Lin X (2009): Cryptococcus neoformans : морфогенез, инфекция и эволюция. Infect Genet Evol 9, 401-416.
Lin X, Heitman J (2006): Биология комплекса видов Cryptococcus neoformans . Анну Рев Микробиол 60, 69-105.
Малик Р., Мартин П., Винни Д. И., Черч Д. Б., Брэдли В., Белленджер С. Р. и др. (1997a): Носоглоточный криптококкоз. Aust Vet J 75, 483-488.
Малик Р., Вигни Д. И., Мюир Д. Б., Грегори Д. Д., Лав Д. Н. (1992): Криптококкоз у кошек: клиническая и микологическая оценка 29 случаев и оценка лечения с использованием перорального флуконазола.J Med Vet Mycol 30, 133–144.
Малик Р., Вигни Д. И., Мюир Д. Б., Лав Д. Н. (1997b): Бессимптомное носительство Cryptococcus neoformans в носовой полости собак и кошек. J Med Vet Mycol 35, 27-31.
Martins DB, Zanette RA, França RT, Howes F, Azevedo MI, Botton SA et al (2011): Массивная криптококковая диссеминированная инфекция у иммунокомпетентной кошки. Ветеринарный дерматол 22, 232-234.
McGill S, Malik R, Saul N, Beetson S, Secombe C, Robertson I et al (2009): Криптококкоз у домашних животных в Западной Австралии: ретроспективное исследование 1995-2006 годов.Медицинская микология 47, 625-639.
Medleau L, Jacobs GJ, Marks MA (1995): Итраконазол для лечения криптококкоза у кошек. J Vet Intern Med 9, 39–42.
Meyer W, Castañeda A, Jackson S, Huynh M, Castañeda E (2003): Молекулярное типирование изолятов IberoAmerican Cryptococcus neoformans . Emerg Infect Dis 9, 189–195.
Норрис Дж. М., Белл Е. Т., Хейлз Л., Торибио Дж. А., Уайт Дж. Д., Вигни Д. И. и др. (2007): Распространенность инфекции вируса иммунодефицита кошек у домашних и диких кошек в восточной Австралии.J Feline Med Surg 9, 300-308.
O’Brien CR, Krockenberger MB, Martin P, Wigney D.I, Malik R (2006): Долгосрочный результат терапии для 59 кошек и 11 собак с криптококкозом. Aust Vet J 84, 384-392.
O’Brien CR, Krockenberger MB, Wigney DI, Martin P, Malik R (2004): ретроспективное исследование кошачьего и собачьего криптококкоза в Австралии с 1981 по 2001 год: 195 случаев. Med Mycol 42, 449-460.
Okabayashi K, Kano R, Watanabe T, Hasegawa A (2006): Серотипы и типы скрещивания клинических изолятов криптококкоза кошек в Японии.J Vet Med Sci 68, 91-94.
Pal M (1989): Cryptococcus neoformans var. neoformans и munia birds Cryptococcus neoformans var. neoformans bei Prachtfinken. Микозы 32, 250–252.
Paulin J, Morshed M, Armién AG (2013): Внутренний отит, вызванный Cryptococcus neoformans var. грубия в кот. Ветеринарный Патол 50, 260-263.
Sykes JE, Malik R. Cryptococcosis (2012): В: Greene CE (ed.): Инфекционные болезни собак и кошек. 4-е изд. Сент-Луис, Сондерс, Эльзевир, стр. 621-634.
Сайкс Дж. Э., Стерджес Б. К., Кэннон М. С., Герикота Б., Хиггинс Р. Дж., Триведи С. Р. и др. (2010): Клинические признаки, особенности визуализации, невропатология и исходы у кошек и собак с криптококкозом центральной нервной системы из Калифорнии. J Vet Int Med 24, 1427-1438.
Тисдалл П.Л., Мартин П., Малик Р. (2007): Скрытое заболевание у кошки с болезненными и опухшими скакательными суставами: упражнение в диагностическом мышлении и принятии клинических решений.J Feline Med Surg 9, 418-423.
Триведи С.Р., Сайкс Дж. Э., Кэннон М. С., Виснер Э. Р., Мейер В., Стерджесс Б.К. и др. (2011): Клинические особенности и эпидемиология криптококкоза у кошек и собак в Калифорнии: 93 случая (1988-2010). J Am Vet Med Assoc 239, 357-369.
Urban CF, Lourido S, Zychlinsky A (2006): Как микробы избегают уничтожения нейтрофилов? Cell Microbiol 8,1687-1696.
Для дальнейшего чтения:
Cardoso PH, Baroni FdeA, Silva EG, Nascimento DC, Martins Mdos A, Szezs W, et al (2013): Гранулема носа у кошек, вызванная Cryptococcus gattii типа GII. Mycopathologia 176, 303-307.
Castrodale LJ, Gerlach RF, Preziosi DE, Frederickson P и Lockhart SR (2014): Длительный инкубационный период для инфекции Cyptococcus gattii у кошек, Аляска, США. Emerg Infect Dis 19, 1034-1035.
Espino L, Barreiro JD, Gonzalez A, Santamarina G, Mino N и Vazquez S (2014): Внутричерепная эпидуральная эмпиема, вызванная Cryptococcus neoformans у 5-летнего кастрированного мужского пола европейской короткошерстной кошки. Ветеринарный врач 28, 1-16.
Pennisi MG, Hartmann K, Lloret A, Ferrer L, Addie D, Bélak S и др. (2013): Криптококкоз у кошек. Руководящие принципы ABCD по профилактике и ведению. J Feline Med Surg 15, 611-618.
дерматомикозов. Этиология. Патогенез. Клинические признаки. Диагностика. Лечение. Профилактика.
1. Инфильтративно-гнойный трихофитоз волосистой части головы вызывается:
1) Трих.виолончель;
2) Microsporum canis;
3) Pityrosporum orbiculare;
4) Trich.verrucosum;
5) Трич. рубрум.
2. Какие клинические формы микроспороза различают?
1) Плоскоклеточный;
2) хроническая;
3) Гладкая кожа;
4) Скальп;
5) Большие складки.
3. Какие лекарства используются для лечения дерматомикозов?
1) Гризеофульвин;
2) эмульсия синтомицина;
3) Тетрациклин;
4) Нистатин;
5) Преднизолон.
4. Антропофильный микроспороз гладкой кожи вызывают:
1) Трих. ментагрофиты;
2) Microsporum ferrugineum;
3) Pityrosporum orbiculare;
4) Candida albicans;
5) Трич. рубрум.
5. При каком заболевании чаще всего применяется исследование с помощью лампы Вуда?
1) Разноцветный лишай;
2) Эпидермофития стоп;
3) микроспороз волосистой части головы;
4) Rubrophytia;
5) Инфильтративно-гнойная трихофития.
6. Какие лекарства используются для лечения микозов волосистой части головы?
1) Кортикостероидные мази;
2) Гризеофульвин;
3) Крем Унны;
4) Мазь серная;
5) 2% -ная настойка йода.
7. Какие методы используются для диагностики зооантропофильного микроспороза волосистой части головы?
1) Микроскопическое исследование;
2) Культурное обследование;
3) Осмотр лампы Вуда;
4) йодная проба Бальцера;
5) Признак Безье-Мещерского (явление стружки).
8. Какие заболевания относятся к группе дерматомикозов?
1) Разноцветный лишай;
2) Эпидермофития стоп;
3) микроспороз;
4) Rubrophytia;
5) Трихофития.
9. Каковы показания для назначения гризеофульвина?
1) Поражение волосков грибковой этиологии;
2) Розовый лишай;
3) генерализованный рубромикоз;
4) Онихомикоз;
5) Экзематизация пораженных участков.
10. Зооантропофильный микроспороз волосистой части головы, вызываемый:
1) Трих. ментагрофиты;
2) Microsporum canis;
3) Pityrosporum orbiculare;
4) Microsporum ferrugineum;
5) Трич. рубрум.
11. Какие методы используются для диагностики онихомикоза стоп?
1) Микроскопическое исследование;
2) Культурное обследование;
3) Осмотр лампы Вуда;
4) йодная проба Бальцера;
5) Признак Безье-Мещерского (явление стружки).
12. Для какого заболевания характерен сотовый признак Цельса?
1) микроспороз;
2) инфильтративно-гнойный трихофития;
3) Разноцветный лишай;
4) кандидоз;
5) Руброфития.
13. Какие клинические формы микоза стоп вызваны трихомонадой. mentagrophytes var. Interdigetale различаются?
1) Опрелость;
2) Онихомикоз;
3) дисгидротическая форма;
4) Обобщенная форма;
5) Плоскоклеточно-гиперкератотическая форма.
14. Какие методы используются для диагностики паразитарного сикоза?
1) Микроскопическое исследование;
2) Культурное обследование;
3) Осмотр лампы Вуда;
4) йодная проба Бальцера;
5) Признак Безье-Мещерского (явление стружки).
15. Какие факторы больше всего способствуют заражению эпидермофитией стоп?
1) Наличие в доме больной кошки;
2) Использование общей обуви;
3) Использование общих полотенец, губок;
4) Использование общих головных уборов;
5) Детский возраст.
16. Какой наиболее типичный клинический признак микроспороза волосистой части головы (1 балл).
1) Шелушение;
2) Гиперемия;
3) Очаговый характер аффекта;
4) Волосы обламываются;
5) Корочки.
17. Какие мази применяют при микозах стоп?
1) мазь серная 10%;
2) Клотримазол;
3) Преднизолоновая мазь;
4) Мазь с нистатином;
5) Тетрациклиновая мазь.
18. Антропофильный микроспороз волосистой части головы вызван?
1) Трих. ментагрофиты;
2) Microsporum canis;
3) Pityrosporum orbiculare;
4) Microsporum ferrugineum;
5) Трич. рубрум.
19. Каковы источники заражения ребенка микроспорозом?
1) Собака;
2) Корова;
3) Кот;
4) Мужчина;
5) Лошадь.
20. Для лечения микроспороза волосистой части головы назначают Гризеофульвин в дозе:
.1) 22 мг в сутки;
2) 22 мг трижды в сутки;
3) 22 мг на кг веса тела трижды в сутки;
4) 22 мг на кг веса тела в сутки;
5) 2 мг на дозу.
21. Наиболее частый микроорганизм, вызывающий микоз кожи головы у детей:
1) Trichophytontonsurans;
2) Microsporum;
3) Эпидермофитон;
4) Candida albicans;
5) Pityrosporum orbiculare.
22. Мальчик 11 лет болен микозом волосистой части головы. Наиболее подходящая линия лечения:
1) Системная терапия грузиофульвином;
2) Местная терапия грузиофульвином;
3) Бритье волосистой части головы;
4) Сульфидный шампунь Seleneum;
5) Системная терапия нистатином.
23. Какой из следующих причин чаще всего вызывает онихомикоз?
1) Trichophyton mentagrophytes;
2) виды Candida;
3) Trichophyton rubrum;
4) Trichophytontonsurans;
5) Microsporum Ferrugineum.
24. Что из следующего подтверждает диагноз онихомикоз?
1) Клиническое наблюдение;
2) Приготовление гидроксида калия;
3) Культура;
4) Гистология;
5) Биопсия.
25. Онихомикоз:
1) заразная;
2) Грибковая инфекция ногтевого ложа;
3) Рецидивирующая инфекция;
4) Все верно.
26.Какой из них является наиболее частым возбудителем онихомикоза в умеренном климате?
1) Рецидивирующая инфекция;
2) дерматофиты;
3) дрожжи;
4) Формы;
5) Ничего из вышеперечисленного.
27. Какой из этих дерматофитов чаще всего ассоциируется с онихомикозом?
1) Trichophyton rubrum;
2) Trichophyton mentagrophytes;
3) Epidermophyton flocossum;
4) Trichophyton megninii;
5) Microsporum Ferrugineum.
28. Лечение онихомикоза пероральными противогрибковыми средствами обычно принимают за:
1) Несколько дней;
2) Несколько месяцев;
3) Несколько лет;
4) На всю жизнь.
29. Местная терапия онихомикоза особенно оправдана, когда:
1) Поражено менее 30% ногтевой пластины;
2) Поражено менее 50% ногтевой пластины;
3) Поражено менее 70% ногтевой пластины;
4) Поражение всей ногтевой пластины.
30. Что из этого неверно в отношении гризеофульвина как терапевтического средства от онихомикоза?
1) Его эффективность ограничена дерматофитами;
2) Синтезируется из некоторых видов пенициллов;
3) обладает фунгицидным действием;
4) Это больше не считается золотым стандартом лечения онихомикоза.
31. Что из этого назначается как пульс-терапия при онихомикозе?
1) итраконазол;
2) флуконазол;
3) Гризеофульвин;
4) Кетоконазол;
32.В фиксированной схеме дозировки тербинафин указан как
.1) 50 мг в день
2) 100 мг в день
3) 250 мг в день;
4) 400 мг в день.
33. Какая система доставки лекарств лучше всего подходит для лечения онихомикоза?
1) Кремовый;
2) Мазь;
3) Лак для ногтей;
4) Гель.
34. Пик заболеваемости микозом волосистой части головы приходится на:
.